Ca parte a moleculei are patru inele de pirol. Porfirine sunt foarte predispuse la formarea de compuși complecși cu metale. In uleiurile acestea sunt atât în stare liberă și sub formă de complecși cu vanadiu, nichel și fier.
Proprietățile chimice ale compușilor care conțin azot a) compus bazic (alcalin)
Piridină poate fi considerată ca benzen, în care gruparea -CH = atom de azot substituit. Și piridină și benzen sunt molecule care sunt substanțial hexagon regulat.
Prezența atomului de azot singură pereche de electroni conduce la faptul că piridina (și alte baze azotate - chinolină, izochinolină, acridină) prezintă proprietățile de amine terțiare. În primul rând, este proprietățile bazelor slabe. În soluție care reacționează cu apa, în principal
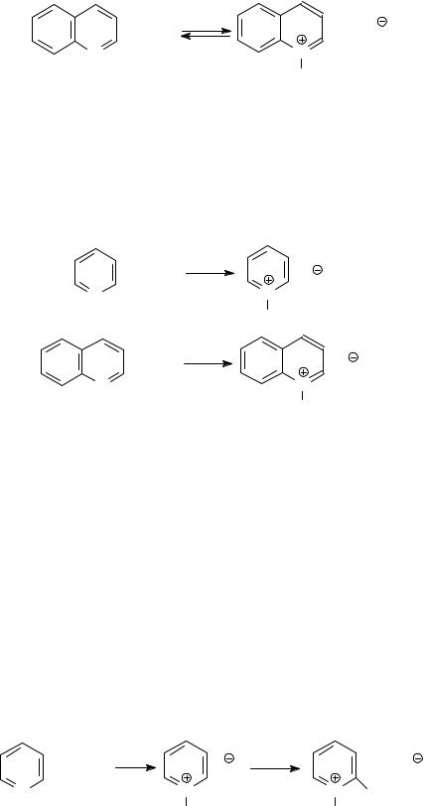
Concentrațiile de ioni de hidroxil este suficientă pentru a forma o varietate de hidroxizi de metale: Fe 3+. Co 2+. Sn 2+ și altele.
Compușii formează cu ușurință săruri cu acizi, cum ar fi acidul clorhidric, bromhidric, sulfuric și altele:
H piridinium
Sărurile sunt bine cristalizate și utilizate pentru izolarea și identificarea compușilor cu azot. Interesant, săruri acridină în soluții apoase au fluorescență verde, și după diluarea prin hidroliza continuă fluorescență într-o caracteristică albastră a acridinium liber.
Deoarece aminele terțiare, baza azotată reacționează cu halogenuri de alchil pentru a forma sarea corespunzătoare, care atunci când este încălzit, ca urmare a substituentului izomerizată tranziției la atomul de azot la atomul de carbon din poziția 2 sau 4 (dar nu 3):
La prelucrarea peroxid de hidrogen și acid perbenzoic, oxizi ai compușilor cu azot se formează în mediu acid acetic:
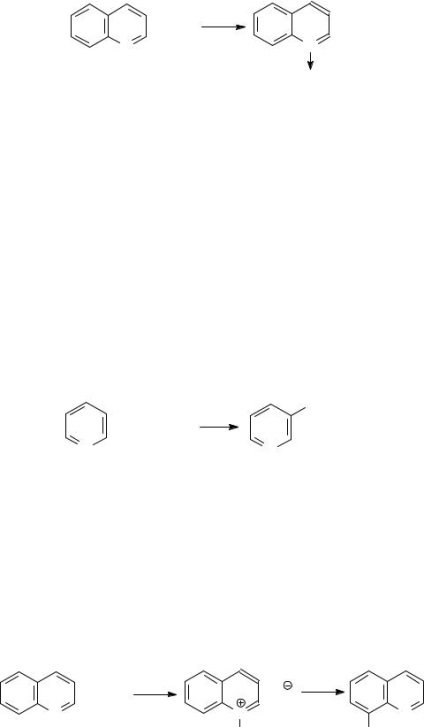
Un nucleu piridinic este prezent în moleculele de baze azotate menționate este supusă substituție electrofilă reagenti radicali nucleofili. Trebuie apreciat faptul că prezența epuizeaza de azot din inel cu densitate de electroni atom datorită efectului său puternic de inducție pozitiv, și poziția 2,4,6 în particular sărăcit. Prezența substituenților sau a altor donatori facilitează reacția de substituție electrofilă.
După încălzirea de piridină, timp de 24 de ore cu acid sulfuric fumans la 220-230 ° C, în prezența sulfatului de mercur format piridin-3-
Chinolina sau acridin cicluri, în plus față de piridină, inele benzenice sunt prezente mai active în reacțiile de substituție. Prin urmare, reacțiile de substituție continuă în acești compuși este mult mai ușor.
Acest efect de inducție atom chinolină azot conduce la o epuizare a densității de electroni 2,4 poziții de piridină și 5,7 - inel benzen. Prin urmare, agenții electrofili atacă în primul rând dispozițiile 8.6:
Reacția generală a compușilor azotați este capacitatea lor de a recupera hidrogen:
b) compuși azotați neutre
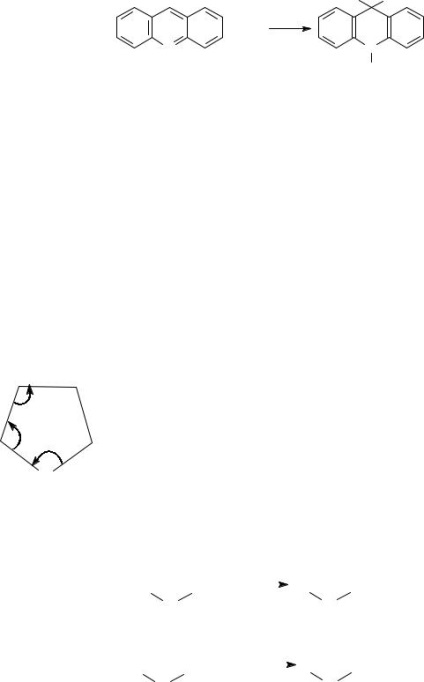
În acești compuși prezintă un ciclu cu cinci atomi cu atomul de azot într-o stare de hibridizare sp3 având un atom de hidrogen.
formarea sistemului electronic aromatic implică atât 4 π-
două legături C = C de electroni, și perechea de electroni unshared atomului de azot,
ceea ce conduce la formarea unui singur shestielektronnogo π-nor - structură aromatică similară cu benzen. Ca rezultat, inelul pirolic este plat, legături simple sunt scurtate. Structura inelelor pirolului reprezentate în schema (lungimea legăturii indicată în angstromi).
ca un compus neutru
interacțiune cu agenți de reducere activi, de exemplu,
potasiu metalic sau reactiv Grignard.
Când pirol condensat cu hidroxid de potasiu uscat și
substituție și formare pirrolkaliya hidrogen transportate:
(! Dar nu pirol) Pirrolkaly reacționează cu halogenuri de alchil cum ar fi iodura de etil, pentru a da pirolii substituiți:

Proprietățile de bază ale pirol, care amina secundară în mod formal mascate prin polimerizarea rapidă sub acțiunea unui acid.
O reacție interesantă calitativă pirol înroșire pin torta umezită cu acid clorhidric, în prezența vaporilor de pirol. Se presupune că acest lucru se datorează polimerizarea pirol într-un mediu acid.
Pirol este ușor redus cu hidrogen:
Pentru a continua descărcarea aveți nevoie pentru a asambla o imagine: