Măsurarea masei miezurilor cu un spectrometru de masă (dispozitive de separare a atomilor ionizați sau molecule în funcție de masele lor prin trecerea fascicule de ioni prin câmpul electric și magnetic) a arătat că masa de nuclee atomice nu este egală cu masa de repaus a nucleonilor constituente individuale, dar ceva mai puțin l. Acest lucru se datorează faptului că nucleonii din nucleu sunt puternic interconectați datorită forțelor nucleare. Pentru a separa nucleul de protoni și neutroni separați, este necesar să extindeți o anumită energie, numită energia de legare a nucleului.
Energia de legare a nucleului este determinată de magnitudinea muncii ce trebuie făcută pentru a împărți nucleul în nucleonii săi constituenți fără a le da energie cinetică. Din legea conservării energiei rezultă că atunci când se formează nucleul, trebuie eliberată o astfel de energie, care trebuie să fie folosită în timpul divizării nucleului în nucleonii săi constituenți.
Energia obligatorie a nucleului este diferența dintre energia nucleonilor liberi care alcătuiesc nucleul și energia lor în nucleu.
Folosind formula lui Einstein. obținem o expresie pentru energia de legare a nucleului:
Aici. - respectiv, masa de odihnă a nucleului protonic, neutron și atomic. Deoarece masele non-nucleelor sunt de obicei determinate experimental și atomii care sunt date în tabele, formula (22.3) pentru energia de legare poate fi transformată în expresie:
unde este masa atomului de hidrogen; este masa atomului elementului corespunzător. În această formulă, masa electronilor care intră în primul termen. este compensată de masa de electroni care împreună cu nucleul formează o masă.
Expresiile (22.3) și (22.4) fac posibilă obținerea unor valori practic identice ale energiei de legare a nucleului. Valoarea. care determină energia de legare a nucleului. se numește defect de masă. Defectul de masă caracterizează scăderea în masa totală a formării nucleului din nucleonii constituenți ai acestuia. În calculul practic Masele tuturor particulelor și atomilor sunt exprimate în unități de masă atomică (amu). O unitate atomică de masă corespunde unei unități atomice de energie (a.e.e.): 1 AUe. = 931.5016 MeV.
Energia de legare, care se referă la un singur nucleon, adică Energia totală de legare împărțită la numărul de nucleoni din nucleu se numește energia de legare specifică:
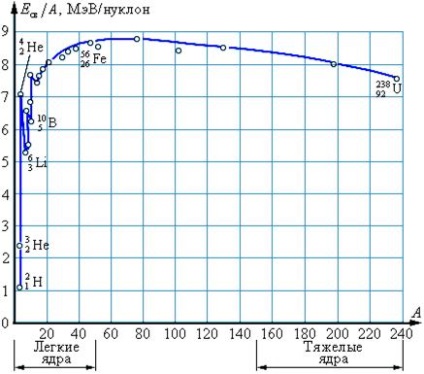
Figura 22.1 prezintă dependența energiei de legare specifică pentru diferite nuclee pe numărul de masă A. Caracterizarea diferitelor concentrații ale legăturilor nucleonice din nucleele diferitelor elemente chimice. Se poate observa din figura că energia de legare crește cu creșterea A în primul rând și apoi formează o secțiune practic orizontală la A> 40 și scade încet la A> 100; aceasta înseamnă că nucleele cu numerele de masă A, având valori de la aproximativ 50 la 80, pentru care energia de legare are cea mai mare valoare, sunt stabile din punct de vedere energetic. Nucleul elementelor din partea de mijloc a mesei periodice este cel mai durabil. În aceste nuclee este aproape de 8,7 MeV / nucleon. Odată cu creșterea numărului de nucleoni din nucleu, energia de legare specifică scade.
Nucleul atomilor elementelor chimice situate la sfârșitul sistemului periodic (de exemplu, miezul de uraniu) are ≈ 7,6 MeV / nucleon. Aceasta explică posibilitatea eliberării energiei în fisiunea nucleelor grele. În regiunea numerelor de masă mici, există "vârfuri" ascuțite ale energiei specifice de legare. Maximele sunt caracteristice pentru nucleele cu număr egal de protoni și neutroni (;), minime pentru nuclee cu numere impare de protoni și neutroni (;).
Pentru nucleele ușoare (hidrogen, litiu), procesul de fuziune este favorabil din punct de vedere energetic, adică sinteza nucleelor mai ușoare; pentru nucleele grele (uraniu, plutoniu) în anumite condiții este posibil un proces de fisiune. Aceste procese sunt practic utilizate în realizarea reacțiilor de fuziune termonucleară și în reacțiile fisiunii nucleare.
Datele despre energia obligatorie a nucleelor au făcut posibilă stabilirea unor regularități în structura nucleelor atomice.
Criteriul pentru stabilitatea nucleelor atomice este raportul dintre numărul de protoni și neutroni într-un nucleu stabil. Pentru valori mici și mijlocii Un număr de neutroni și protoni din nuclee stabile sunt aproximativ egale: Z ≈ A - Z. Z crește rezistența repulsiei Coulomb de protoni cresc proporțional Z · (Z - 1)
Z 2 (interacțiunea perechilor de protoni) și pentru a compensa această repulsie prin atracția nucleară, numărul de neutroni ar trebui să crească mai repede decât numărul de protoni.