Obiective lecție
- continua studiul valenta, afla pe baza cunoștințelor despre structura electronică a atomilor și bonding chimice, cum formulele compuse din substanțe.
obiectivele lecției
• Formarea: să continue să studieze valența să știe ce gradul de oxidare, să ia în considerare punctele de vedere, precum și să învețe cum să se determine gradul de oxidare al unui atom din compusul;
• învățământ: pentru a preda metode de sinteză și comparație, pentru a dezvolta abilitățile de lucru independent, să contribuie la dezvoltarea gândirii logice;
• Educațională: a crea un sentiment de toleranță.
termeni cheie
- Gradul de oxidare - taxa este condiționată atomi ce caracterizează numărul de perechi de electroni deplasate complet sau parțial sau electroni de la un atom la altul compuși chimici.
- Formula chimică - o structură simbol al substanțelor și a compoziției chimice prin caractere și simboluri ale elementelor chimice auxiliare și numerice.
verificarea temelor
1. în care există un molecule nepolare o legătură covalentă?
2) Într-o moleculă în formarea covalentă - legături nepolare formează legătura triplă?
• D) pentru numărul perioadei.
gradul de oxidare
În primul rând, să ne amintim ce valenta.
Starea de oxidare - o caracteristică importantă a stării unui atom din moleculă. Valenței este determinată de numărul de electroni neîmperecheați atomului numai în excitarea unui atom. element de valență mai mare, de obicei egal cu numărul de grup. Oxidarea compușilor cu diferite legături chimice formate în mod inegal.
Oxidarea moleculelor cu diferite legături chimice formate după cum urmează:
1. Compușii cu elementele de oxidare legăturii ionice este încărcătura de ioni. Un exemplu poate fi văzut în figura 1.
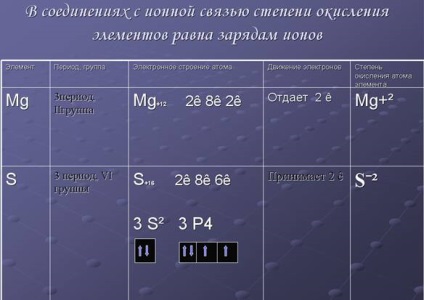
Fig.1. Ilustrarea gradului de oxidare a elementelor din compuși cu legături ionice.
2. în compușii cu legături covalente nepolare (în moleculele de substanțe simple substanțe) starea de oxidare este 0 elemente.
H20, SI20, F20, S0, AI0
3. Gradul de oxidare a moleculelor pentru a lega covalent molecule polare este determinat printr-o legătură chimică similară ionic.
Gradul de oxidare al elementului - este condiționat atom taxă în moleculă, în cazul în care se presupune că molecula este format din ioni.
Gradul de oxidare, în contrast cu valență are un semn. Ea poate fi pozitivă, negativă și zero. Figura 2 prezintă tipurile de oxidare.
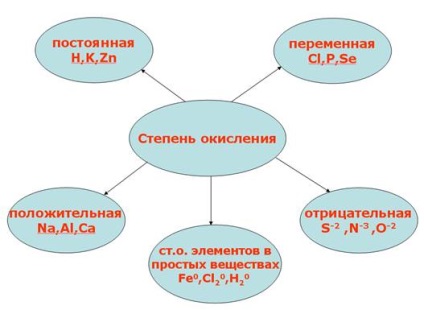
Fig. 2. Gradul de oxidare.
Valenței desemnate prin cifre romane simbol top elementul și gradul de oxidare este indicat prin cifre arabe, cu o taxă pe simbolul elementului (Figura 3).

Fig. 3. Desemnarea valența și starea de oxidare.
La unul și același element poate avea diferite grade de oxidare. Astfel, Figura 4 prezintă gradul de oxidare a sulfului.

Fig. 4. Gradul de oxidare a sulfului.
Acum, să ne uităm la definirea gradului de oxidare a oxizilor:
Starea de oxidare pozitiv egal cu numărul de electroni. care dat atom de date. Atom poate da tuturor electronilor de valență corespunzătoare numărului grupului în care elementul este, prezentând astfel un grad mai mare de oxidare (OF2 excepție).
Numărul de oxidare negativ egal cu numărul de electroni, care sunt luate atom conform (prezentat numai în nemetale). atomi metaloid atașat numărul de electroni care până la finalizarea stratului extern este lipsit, prezentând astfel o putere negativă.
Figura 5 prezintă exemple de grade mai mari și mai mici de oxidare.

Fig. 5. Gradul superior și inferior de oxidare.
valoarea oxidării între grad mai mare și mai mic de intermediari de oxidare numit (Figura 6):

Fig. 6. Starea de oxidare intermediară.
În compușii cu legături covalente nepolare (în moleculele de substanțe simple,) starea de oxidare este 0 elemente: H20, SI20, F20, S0, AI0
Pentru a determina gradul de oxidare a atomului din compusul trebuie să ia în considerare un număr de poziții (Figura 7).

Fig. 7. Dispozițiile care trebuie luate în considerare pentru a determina gradul de oxidare a atomului din compus.
Foarte curând, va fi introdus la reacțiile de oxidare-reducere:
Prepararea compusului cu formula
Există mai multe metode de preparare a compusului cu formula de oxidare, dar nota inițial algoritmul și, în general, prepararea acestora (Figura 8):

Figura 8. Algoritmul de desen oxidare formule chimice.
Să vedem cum să producă oxizi de formula:
Prima metodă de elaborare formula:
1. În primul rând elementul este scris cu o electronegativitate mai mic, al doilea cu o electronegativitate mai mare.
2. Un element scris în primul rând are o sarcină pozitivă, „+“, iar al doilea cu sarcină negativă „-“.
3. Specificați fiecare element de stare de oxidare.
4. Găsiți mai multe comune din valoarea gradelor de oxidare.
5. Se împarte cel mai mic multiplu comun al valorii gradului de oxidare și indicii obținuți atribuit în dreapta jos după simbolul elementului corespunzător. Figura 9 prezintă un exemplu al articolului:
Fig. 9. Exemplul 5 paragraful formule de compilare.
6. În cazul în care gradul de oxidare al unei chiar și - ciudat, ei sunt lângă pictograma la cruce din dreapta jos - înțelept, fără a „+“ și „-“. Exemplu de modul în care să execute elementul, prezentat în figura 10.
Fig. 10. Exemplul 6, paragraful compilare formule.
7. În cazul în care gradul de oxidare este o valoare chiar, au nevoie mai întâi să taie în jos, pe cea mai mică valoare a gradului de oxidare și a pus criss - cruce fără „+“ și „-“: C + 4 O 2. Un exemplu de modul în care să atragă astfel de compuși este dată în figura 11.
Fig. 11. Exemplul 7, punctul de compilare formule.
A doua metodă de preparare a formulei:
1. Notăm starea de oxidare N prin X, indică gradul de oxidare O: N2x O3-2
2. Se determină cantitatea de sarcini negative, pentru gradul de oxidare a oxigenului multiplica oxigen-index: 3 • (-2) = -6
3. molecula electric neutru a fost necesară pentru a determina cantitatea de sarcini pozitive: X2 = 2X
ecuația algebrică 4.Sostavit (Figura 12).
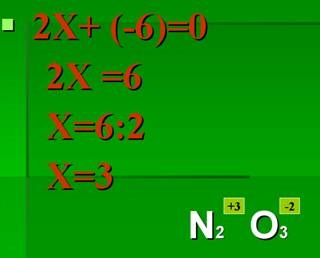
Figura 12. Întocmirea unei ecuații algebrice.
1. taxa de oxidare condiționat, în atomii elementelor chimice din compusul, care se calculează presupunând că toate conexiunile constau numai din ioni.
2. oxidare poate fi valori pozitive sau negative zero, care sunt de obicei plasate pe partea de sus a elementului simbol.
3. Starea pozitivă de oxidare egal cu numărul de electroni care date atom de date.
4. Numărul de oxidare negativ egal cu numărul de electroni, care sunt luate atom conform (prezentat numai în nemetale).
Unitatea de control
1. Care este gradul de oxidare?
2. Care sunt tipurile de oxidare?
3. Ce este o stare de oxidare intermediară?
4. Cum de a crea o formulă în articulații?
teme pentru acasă
Dă numele următorilor compuși binare. Cl2O7, Cl2O, ClO2, FeCl2, FeCI3, MnS, MnO2, MnO, MnCl4, Cu2O, Mg2Si, Na3N, FeS.
Scrieți formula substanțe, constând din următoarele elemente:
1. F și G
2. N și H
3. Zn și Cl
Regulile de determinare a gradului de oxidare
Sarcina acestei lecții este de a introduce un subiect, ca gradul de oxidare. Să rezuma cu tine, și încă o dată amintesc definiția gradului de oxidare.
Știm deja că starea de oxidare se numește atomii condiționate și o sarcină auxiliară a elementului chimic din compusul, care este calculat dintr-o astfel de propunere, în care toate ionice și covalente - compuși polari constau exclusiv din ioni.
Hotărârea pronunțată de gradul de oxidare a diferitelor elemente pot fi de ajutor:
• În primul rând, aspectul de clasificare a substanțelor chimice;
• în al doilea rând, la descrierea proprietăților substanțelor chimice;
• în al treilea rând, în prepararea compușilor cu formulele chimice și nomenclatorul acestora;
• În al patrulea rând, gradul de oxidare, și destul de des utilizat atunci când se lucrează cu oxidare - reacțiile de reducere.
In cele mai multe cazuri, gradul de oxidare a atomilor în materiale cu o structură complexă desemnată inițial de semn și apoi un număr. Numerele de desemnare poate fi 1, 2, -2 și altele.
Dacă ne imaginăm că, în mod ipotetic compusul este taxa de ioni, în acest caz, ar trebui să dea mai întâi numărul, apoi conectați-vă.
Dar pentru a găsi gradul de oxidare, există anumite reguli. Să aruncăm o privire mai atentă la aceste reguli.
Astfel, în determinarea gradului de oxidare a atomilor necesare respectați următoarele reguli:
• În primul rând, un simplu substanțe atomi grad de oxidare egal cu zero;
• În al doilea rând, suma algebrică a stări de oxidare în moleculă neutră este de asemenea zero. Dar pentru ionii este egală cu suma algebrică a taxei de ioni.
• În al treilea rând, practic toți compușii de hidrogen vor avea un grad de oxidare, care este egal cu 1, cu excepția hidruri sunt metale activi. Ei CO va fi egal cu -1.
• În al patrulea rând, dacă luăm în considerare atomii de oxigen din ei CO = -2 compuși. Apoi excepție va OF2 și peroxizi de metale și, în consecință, în acest caz, oxigenul CO este egal cu 2 și -1.
• În al cincilea rând, în cazul în care compușii complecși, sunt indicați cu atomul central.
• Regula următoare este un metal alcalin. Dacă luați elementele primului grup al grupului principal, CO = 1. Dar elementele din al doilea grup, care includ metalele alcalino-pământoase din compusul va avea o stare de oxidare +2 egal. Pentru SB aluminiu = 3, a = -1 pentru fluor.
• Dacă se consideră compus covalentă, atomul mai electronegativ indică întotdeauna gradul de oxidare cu semnul „-“. Dar, în compuși cu mai puțin electronegativ cu un semn „+“.
• Dacă luăm în considerare compușii ionici simpli, gradul lor de oxidare și să fie egală în mărime și semn al faptului că are o sarcină electrică.
Acum, o privire mai atentă la normele de stări de oxidare intermediare:

Dar trebuie remarcat faptul că toate aceste reguli care trebuie urmate atunci când avem de-a face cu o stare de oxidare constantă. În cazul în care un element chimic cu o variabilă, acesta depinde în general de ordinul și tipurile de atomi din acest compus.
studiu de caz
1. Vi se formula elementelor chimice. Se determină gradul de oxidare a acestor formule.
2. În această sarcină ar trebui să determine starea de oxidare prezentate mai înainte elemente care să chimice ale compusului binar cu formula.

3. Formulele Aici sunt prezentate. Care sunt conexiunile lor:

4. Numele acestor substanțe este necesară pentru a formula:
