Rutherford a sugerat modelul atom planetar, conform căruia atomul constă dintr-un nucleu încărcat pozitiv și electronii din jur. Analizând aceste experimente, Rutherford, de asemenea, a aratat ca nucleele au o dimensiune de aproximativ 10 -14-10 -15 m (aproximativ 10-10 m liniar atom dimensiuni).
Nucleul atomic este alcătuit din particule elementare - protoni și neutroni. Proton (p) are o sarcină pozitivă egală cu sarcina electronului și masa de odihnă p.t. = 1,6726 kg 1 836 10 -27 mine. în cazul în care mi - masa de electroni. Neutronul (n) - o particulă neutră repaus de masa mn = 1,6749 kg 1 839 10 mine -27. Protonii și neutronii sunt numite nucleoni (din nucleul latin -. Nucleus). Numărul total de nucleoni într-un nucleu atomic numit un număr de masă A.
Nucleul atomic se caracterizează prin taxa Ze. unde e = 1.6022 10 -19 linia de cablu merge taxa de protoni egal cu taxa de electroni, Z - taxa kernel număr egal cu numărul de protoni din nucleu și care coincide cu numărul de serie al elementului chimic din Sistemul periodic al elementelor.
Kernel-ul este notat cu același simbol ca un atom neutru :. în care X - simbolul elementului chimic, Z - numărul atomic (numărul de protoni din nucleu), A - numărul de masă (numărul de nucleoni din nucleu).
Deoarece atom neutru, sarcina nucleului și definește numărul de electroni din atom. Din numărul de electroni depinde de distribuția lor în stare atomică, care, la rândul lor, depind de proprietățile chimice ale atomului. În consecință, taxa pe nucleul determină specificitatea elementului chimic, adică. E. Stabilește numărul de electroni din atom, configurația cojile de electroni, mărimea și natura câmpului electric intra.
Masa nucleilor poate fi determinată foarte precis prin spectrometrie de masă - instrumentare separarea de câmpuri electrice și magnetice, fascicule de particule incarcate (ioni de obicei) cu specific diferit sarcină Q / m. măsurătorile Mace-spectrometrice au arătat că masa nucleului este mai mică decât suma maselor nucleonilor sale constitutive. Dar, din moment ce orice schimbare a masei trebuie să se potrivească cu variația energiei, rezultă că formarea miezului ar trebui să fie alocată o anumită energie. Din legea de conservare a energiei presupune contrariul: pentru a separa nucleul în părțile sale componente necesare pentru a petrece aceeași cantitate de energie care este eliberată în timpul formării sale. Energia care trebuie cheltuite pentru a împărți nucleul în nucleoni individuale, numită energia de legare nucleară.
Folosind ecuația lui Einstein care definește relația dintre masă și energie, este ușor de a determina energia de legare a nucleonilor în nucleu
unde mp. mil. mya - masa respectiv protoni, neutroni și nucleu. Tabelele nu sunt, în general nuclee de greutate mya, și atomii de masă m. Prin urmare, formula utilizată pentru energia de legare nucleară
unde mH - masa atomului de hidrogen. Deoarece mH mp mai mare suma pe mine. primul termen în paranteze pătrate include Z masa de electroni. Cu toate acestea, din moment diferit de masa atomică de masa m a Mya nucleu doar pe Z greutatea electronilor, calculele acestor două formule rezultat aceleași rezultate. valoare
Se numește defect de masă nucleară. Această valoare scade masa nucleonilor în formarea nucleului atomic.
Legare de energie este, de obicei, măsurată în electron volți (eV) este de 1 eV este numeric egal cu activitatea desfășurată de către forțele de câmp, atunci când se deplasează sarcina electrică elementară (taxa egală cu sarcina electronului) atunci când trec o tensiune de 1 V. Deoarece sarcina unui electron este de 1,6 10 - 19 CI, apoi 1 = 1,6 eV J. 10 -19.
atomi de masă și nuclee defect de masă se măsoară în general în unități atomice de masă (uam) 1 amu numeric egală cu 1/12 din masa izotopului de carbon 12 C, 1 uam = 1.6606 10 -27 kg. O unitate de masă atomică corespunde unității atomice a energiei (a.e.e.) = 931.5016 a.e.e. 1 MeV.
De multe ori, în loc de legare a energiei specifice dEsv de energie de legare - energie cu caracter obligatoriu pe nucleon. Ea este stabilitatea (durabilitatea) a nucleelor atomice, adică, Cu cât este mai dEsv. nucleul mai stabil.
energia de legare specifică depinde de numărul de masă al elementului A (fig. 4.1). Pentru nuclee ușoare (A 12 £) energia de legare specifică crește progresiv până la 6¸7 MeV, trece printr-o serie de salturi, apoi crește mai lent, la o valoare maximă de 8,7 elemente MeV cu A = 50¸60, și apoi, treptat,
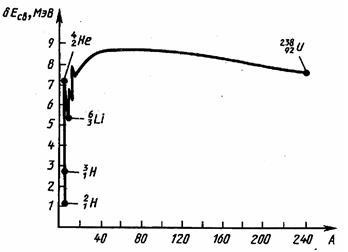
Scăderea energiei de legare specifică a trecerii la elementele mai grele datorită faptului că odată cu creșterea numărului de protoni din nucleu si creste energia repulsiei Coulomb. Prin urmare, legătura dintre nucleonii devine mai puțin severă, iar nucleele în sine mai puțin
puternic. Fig. 4.1
Fig. 4.1 că cea mai stabilă din punct de vedere energetic sunt mijlocul tabelului periodic al nucleului. nuclee grele și ușoare sunt mai puțin stabile. Acest lucru înseamnă că energic favorabile următoarele procese:
1) fisiunea nucleelor grele în brichetă;
2) fuziunea nucleelor ușoare într-una mai grea alta.
cantitate uriașă de energie eliberată atunci când ambele procese; Aceste procese sunt în prezent realizate practic (reacție de fisiune și reacția de fuziune).
Între componentele de bază ale nucleonilor, forțează mult mai mare decât forța de respingere Coulomb între protonii. Acestea sunt numite forțe nucleare. Forțele nucleare sunt o clasă de interacțiuni puternice. Forțele nucleare au următoarele proprietăți: forțele nucleare sunt atractive, acestea sunt rază scurtă de acțiune (efect apare numai la o distanță de 10 până la 15 m), acestea sunt caracterizate prin independența de încărcare (forțele care acționează între protonul și neutronul și doi protoni sunt egale în mărime), forțele nucleare specifice saturație (fiecare nucleonilor din nucleu interacționează cu doar un număr limitat de cel mai apropiat la acesta neutroni).
Forțele nucleare - .. Natura forței de schimb, adică particulele sunt transportate printr-un schimb între nucleonii care interacționează.