Alcoolii (alcooli), Org. Conn. care conțin în moleculă una sau mai multe. OH grupări hidroxil au așezat. atomi de carbon. Prin numărarea acestor grupuri sunt una disting (uneori termenul „alcool“ se referă numai la alcooli monohidroxilici), di- (glicoli), tri- (glicerol) și alcooli polihidrici. Alcooli având două grupări OH la un atom de carbon (gem-diol) este, în general instabilă. Nek- a portului. de ex. vnutrimol stabilizat. legături de hidrogen. stabil. Alcoolii pot conține grupări Hal, NH2. CHO și CO, COOH, CN (resp. Halo-alcooli, aminoalcoolii. Cetone Oksialdegidy și hidroxi. Oxi- acidului oksinitrily). Alcoolii alifatici pot fi RCH2 primar OH, R'R secundar și terțiar RR'CHOH. DREAM. Conn. cu grupa OH la o legătură dublă aparține enolatul. și la compuși aromatici de carbon. To-ring fenoli.
În conformitate cu nomenclatura IUPAC. Alcoolii produs prin adăugarea la numele titlurilor. hidrocarbură sufix „ol“ sau prefixul „hidroxi“ pentru comp corespunzătoare. cu amestec p-tiile, sau, în cazul în care gruparea OH este în catenă laterală, de ex. HOCH2 CH2 CH (CH2OH) CH2OH numit. 2-hidroximetil-1,4-butandiol. Mulți alcooli sunt referințe triviale. (A se vedea. Tabel.).

Alcoolii se găsește în natură sub formă de esteri (grăsimi. Ceruri. Uleiuri esentiale) si FREE. condiție. Astfel, 3-hexenol (t. Chemat. Alcool frunze) conținute în frunze și fructe verzi, uleiuri esențiale. alcool benzilic în ulei de iasomie. și alcool fenetilic, într-un ulei roz.
Proprietăți. Alcooli, lichide sau solide în insule, o bună solubilitate. la plural. org. p-celeration. Lower sol alcooli alifatici. în apă; alifatich mai mare. și alcooli arilalifatice solubilitate slabă. în apă.
Alifatich. C1-C3 alcooli au un miros caracteristic de alcool, C4 -S5 sufocant dulce miros, alcooli alifatici superiori și alcooli inodore, arilalifatice și terpenoide care conțin OH, cu miros floral-fructat.
Atomul de oxigen al grupării hidroxil este sp3 hibridizare. Lungimea medie a legăturii de 0,143 nm (C-O) și 0,091 nm (O-H). Atât polaritatea. grupe polare OH și. capacitatea sa de a forma legături de hidrogen contabilizeze relativ mare valoare p t fierbere și dielectric. alcooli permeabilitate.
Spectrele IR caracteristice alcoolilor. Benzile de absorbție se află în regiunea 3580-3670 cm -1 (Svob. OH grup). 3450-3550 cm-1 (vnutrimol. Associates), 3200-3400 cm -1 (intermoleculare. Associates). În UV și vizibile regiuni ale benzii de frecvențe nu este absorbit. Produsul chimic RMN. .. OH schimbare d 0,5-5,5 ppm semnal multiplicitate depinde de natura alcoolului: triplet da alcooli primari. dublet secundar, terțiar-singlet. OH a otritsat. inducție și îl pune. efect mezomeric. Taft constantă 1,55 s *, Hammet s constant meta 0,121, s abur - 0,37, -0.853.
La fel ca apa. alcooli prezintă insule de comunicare amfoteri. Amploarea pKa (apa. 25 ° C) timp de 15,1 CH3OH, C2 H5 OH 15.9 (CH3) 3 COH 19, (CF3) 3 COH 5,4.
Majoritatea p-tiile alcooli procedează cu ruptura de O-H sau C-O. Pentru alcooli sunt de asemenea caracteristice p-TION, în k-ryh a implicat un -H-atom (oxidare), b -H-atom (deshidratare). sau d atom -H (oxideze. ciclizare).
P-TION cu leafminer puternică. la-ter conduce fie la esteri ai unui m (k-vă în exces) sau esteri simpli (exces de alcool), de exemplu.:
C3 H7 OH + HOSO3 HC3 H7 OSO3 H + H2O
P-TION eterificare poate avea loc prin mecanisme SN 2 (R și R'-alchil primar) sau SN 1 (R-MPEM-alchil, alil, benzii), în funcție de ușurința de formare a carbocationului; pentru p-tiile care au loc mecanismul SN 1, utilizează condiții blânde (dil. la tine, pe-LO. t-py) pentru a preveni deshidratarea în olefine. Deshidratarea de miner puternic. k-m este în cazul alcoolilor primari sau secundari.
C2 H5 OH + CH3 CH = CH CHCNCH3 (OC2 H5) CH2CN
P-TION alcoolilor cu aldehide în prezența. . HCl, n - acidul toluensulfonic și alții Catalizatori duce la acetali, de exemplu:.
C2 H5 OH + SNOCH3 CH3 CH (OC2 H5) 2
În reacția alcoolilor cu un carboxilic-ter format esteri. p-TION este efectuată într-un alcool cu îndepărtarea simultană a apei în exces, în prezența. catalizatori (CI1, BF3 H2 SO4, etc ...); în cazul alcoolilor primari și secundari la catalizator activează, în cazul terțiar-alcool:

În reacția alcoolilor cu izocianați formate Ur-thanes, în interacțiune. cu HK1, SOCI2. PCI3 și colab OH este schimbat cu halogen (cel mai ușor de alcooli terțiari), de ex..:
ROH + R'NCO. R'NHCOOR ROH + SOCI2. RCL + HCI + SO2
Recuperarea alcoolului duce la hidrocarburi. Aminele N H3 acțiune -k (p-tskyu folosit ultima Prom-STi pentru producerea alifatich inferior amine.), de ex.:
Sub acțiunea agenților oxidanți (... Na2 Cr2 O7 KMnO'4 N-brom-succinimidă, etc.) sunt transformate alcooli primari la aldehide (și mai departe la a-you), secundare - cetonele (oxidarea alcoolilor secundari într-o p-TION și Oppenauer Aceasta duce la ke-tone); aceleași transformări pot fi transportate katalitich. dehidrogenarea alcoolilor în gaz (de ex., prin trecerea vaporilor de alcooli Cu, Ag, Cr, Ni) sau în fază lichidă (peste Rh, Ru, Os). Alcoolii terțiari rezistente la oxidare în mediu neutru și alcalin, într-un mediu acid eliminarea apei și separarea scheletului de carbon pentru a forma o cetonă sau o m cu un număr mai mic de atomi de carbon. Bal-IFPS folosit de multe ori katalitich. oxidarea alcoolilor cu oxigenul atmosferic (așa cum este obținută de la O CH2 CH3 OH, CH3 CHO și CH3 COOH, C2 H5 OH) și electrochimice. oxidare.
In oxidarea alcoolilor care conțin d -H-atom, ciclizarea are loc pentru a forma derivați de furan. de ex.:
În interacțiunea. C2 H5 OH cu hipohalogenit Na sunt formate, respectiv. cloroform. bromoform și Iodoform (așa-numitul galoformnaya p-TION ..):
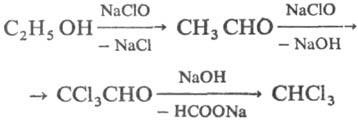
Analiză. Alcoolii da vopsite Conn. cu conexiune. Ce (IV), de ex. ammoniytseriygeksanitratom (NH4) 2 [Ce (NO3) 6]. Pentru a identifica alcoolii utilizând p-TION cu cloruri de acid benzoic sau 3,5-dinitrobenzoic la tine, sau cu fenil izocianat, ceea ce duce la formarea unui bine-esteri ai acidului benzoic de cristalizare la-vă sau uretani. Pentru cantitățile. care determină grupele hidroxil utilizate metoda Tserevitinova. ROH + R'MgX. ROMgX + R'H, un amestec este utilizat pentru cromatografie. metode.

Pentru alcooli, de asemenea, folosind reducerea comp carbonil. sodiu. amalgam lui. LiAlH4 în condițiile Meerwein-TION p-Ponndorfa-Verley, hidrogenare în prezență. catalizatori (Pt, Ni) sau electrolitici. de recuperare.
Pentru bal. produc butanol. 2-etilhexanol și penta-eritrolului folosind condensare aldolică. de ex.:
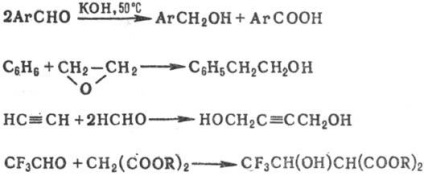
alcooli primari (r. H. aromatic), format pe p-TION Cannizzaro sau în interacțiune. benzen cu oxizi de alchenă în prezența. AICI3 într-o p-TION reacția Friedel-Crafts; Acetilena-p-TION de Reppe; hidroxiesteri, în condițiile de Knoevenagel p-TION, de ex.:
Dintre alcoolii Naib. efect toxic are metanol (100-150 ml doză letală) oxidat în organism la formaldehidă și formic la tine. Toxicitatea este alcool polihidroxilic scăzută, cu excepția organismului la toxic oxalic-tu deformării-glicol.
Producția mondială-alcooli de 30 Mill. Tone / an (1985).
Lit. Tedder John. A. Jubb lipsesc A. Industrial Organic Chemistry. per. din limba engleză. M. 1977; chimia organică totală. per. din limba engleză. t 2. M. 1982; Monick J.A. Alcooli. chimia lor, proprietăți și fabricarea, N.Y. 1968 Chimia grupării hidroxil, ed. de S. Patai, L. 1971; Kirk-Othmer enciclopedie, 3 ed. v. I, N .y. 1978. SK Smirnov.
