Sinyukhin V.N. Stetsyuk EA Arzumanov S.V.
Sindromul uremic este însoțit de acumularea în corpul pacientului a unui număr mare de diferite tipuri de compuși care sunt excretați în urină la oameni sănătoși. Aceste substanțe se numesc toxine uremice. Se crede că ele au un efect negativ asupra funcțiilor biologice ale corpului. Pentru comoditate, aceste conexiuni sunt împărțite în 3 grupe:
1. Compuși solubili în apă cu o greutate moleculară mică, prototipul căruia este ureea;
2. peptide mari cu o greutate moleculară mai mare de 500 Da, numite molecule medii, de exemplu beta-2-microglobulină;
3. Compuși înrudiți ai unei proteine, de exemplu, un fenol sau derivați de indol [1]. Fiecare substanță, pe care o numim toxinele uremice trebuie să îndeplinească criteriile relevante. Conform definiției clasice dată și descrise Mastry S. Bergstrom J. [2] și grupul EROTOX mai aprobat recent condus de Vanholder R. aceste substanțe sunt identificate chimic structuri prezente în fluidele biologice și care pot fi supuse calitativ și determinarea cantitativă a următoarelor caracteristici.
• Efectul toxic al acestor substanțe în intervalele de concentrație ale pacientului uremic determinat în țesuturi trebuie confirmat în experimente pe animale de laborator și în experimente in vitro;
• Concentrațiile utilizate în experimente trebuie să fie în concordanță cu cele la pacienții cu insuficiență renală cronică [3, 4]
TOXINE legate de proteine
Dintre toate toxinele până de curând, cea mai mică atenție a fost acordată toxinelor uremice asociate cu proteinele. Acest lucru sa datorat faptului că acestea nu sunt retrase în timpul dializei standard, iar legătura cu proteina nu permite realizarea efectelor lor toxice, deoarece este cauzată numai de fracțiunea liberă. Lucrările din ultimii ani au demonstrat prezența proprietăților toxice ale acestor substanțe - toxinele uremice în starea legată și, prin urmare, studiile au început să dezvolte metode de îndepărtare a acestora din corpul pacientului. În prima parte a acestei revizuiri, vom aborda clasificarea acestor substanțe și vom discuta despre posibilitățile de a le elimina sau de a reduce conținutul acestora în sângele pacienților.
Studiile intensive privind identificarea compușilor legați de proteine la pacienții cu insuficiență renală au început numai în ultimii ani. Acest lucru se datorează faptului că recent sa constatat că aceste substanțe interferează intens cu procesele metabolice de bază [5]. Tabelul 1 prezintă principalele substanțe uremice legate de proteine cu un efect toxic pronunțat.
Lăsați cele două substanțe care sunt date cea mai mare atenție în studiul toxinelor uremice - este para-crezol (p-cresol) și sulfat de indoxil. Concentrațiile serice ale acestor substanțe crește ca deteriorarea funcției renale și se corelează cu nivelul de GFR [7, 8, 9, 10]. Experimentele in vitro au demonstrat efectul lor toxic [11]. Sa constatat că aceste structuri sunt factori de risc pentru mortalitatea în cazul insuficienței renale cronice [8, 9, 10].
S-a stabilit că în intestin se formează sulfat de indoxil și sulfat de p-cresol. Când este expus la bacterii intestinale pe proteine nedigerate, se sintetizează un număr mare de indoli și fenoli. Acumularea lor duce la întreruperea multor funcții ale corpului uman. Acești doi compuși sunt prototipuri ale unei întregi familii de toxine uremice legată de proteine [12, 13].
Triptofanul este metabolizat în intestin prin flora intestinală la indol și după absorbția indoxil sulfat se formează în ficat. P-cresol provine din metabolismul tirozină și fenilalanină este format apoi acid 4-hidroxifenilacetic, în care decarboxilarea este sintetizat p-crezol [14, 15]. După trecerea prin mucoasa intestinală tsitozolevoy expuse sulfotransferazei sulfat format p-cresol. P-cresol este prezent in sange sub forma de conjugat (Fig. 1). In cele mai multe studii clinice, p-crezol a fost determinat după hidroliza acidă, rezultând într-o moleculă de sulfat p-cresol formează o moleculă de p-cresol, care a permis să judece conținutul principal uremic directă toxina p-cresol [16, 17].
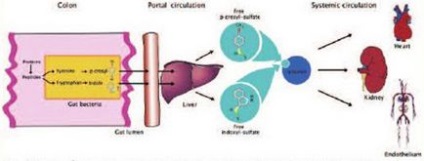
Fig. 1. Schema de formare a indoxilsulfatului și para-cresolului în corpul uman [13].
Ambele toxina excretat prin secreție tubulară tubulară renală, astfel încât acestea să se acumuleze în sângele pacienților cu insuficiență renală [18, 19]. Se crede că cele două substanțe au un efect dăunător direct asupra parenchimului renal prin inducerea inflamației datorită expresiei mărite citokine profibrotic, cum ar fi [20, 21], factorul transformator de creștere beta 1 (TFG 1).
Tabelul 1. Toxinele uremice și efectele lor biologice [6]
Se arată că administrarea șobolanilor cu sulfat de indoxil determinat dezvoltarea fibrozei renale [22], iar administrarea acestuia la șobolani cu creșterea tensiunii arteriale a dus la celulele de expresie de proteine transmembranara provocat celule imbatranire, însoțite de fibroză parenchimului renal [23].
Există o cantitate enormă de toxine care sunt direct legate de dezvoltarea afecțiunilor cardiovasculare împotriva uremiei. Acesta a fost mult timp demonstrat că p-cresol in vivo are efecte directe asupra funcției barierei endoteliale a proceselor de proliferarea celulelor endoteliale și repararea în rană, dar nu sa dovedit până în prezent efectul nociv al sulfatului p-cresol asupra celulelor vasculare in vitro [24, 25] .
Pe de altă parte, este cunoscut faptul că sulfatul de p-cresol în loc de p-cresol exercită efect proinflamator asupra leucocitelor nestimulate in vitro, sugerând un efect dăunător direct sulfat p-cresol asupra vaselor sanguine ale pacienților cu boli renale [26].
exprimat în plus profibrotic sulfat efect indoxil favorizează bolile vasculare cronice prin inhibarea proceselor de reparare în endoteliul și stimularea proliferării celulelor musculare netede [27]. Indoxil sulfat poate cauza disfunctii endoteliale au fost capabili de a provoca stres oxidativ si inducerea procesului de senestsentsii endoteliale [28]. rezultate paradoxale au fost obținute în studii recente care au arătat că, în contrast cu boli renale cronice, împotriva cărora sulfatul de indoxil exercitat un efect prooxidantă, are proprietăți antioxidante [29], în condiții fiziologice normale.
Până de curând, excreția din corpul compușilor asociate cu proteine a fost considerată o sarcină fără speranță. High-dializa nu a prezentat nici un avantaj de peste hemodializa standard adică aproape nu a fost în măsură să elimine aceste substanțe. In contrast, zilnic, a avut loc pentru o lungă perioadă de timp de hemodializă a dus la o scădere a conținutului acestor compuși în sânge [30]. Doar recent sa demonstrat că hemodializa optimă strategia convectiva poate afișa număr mult mai mare de toxine înrudite uremice proteine comparativ cu dializa cu un Hemodiafiltration standard de fond [31]. In experimentul acut a fost de a demonstra avantajele acestei tactici în comparație cu membranele foarte permeabile pentru hemodializă, hemodiafiltrare și postdilyutsionnaya au mari avantaje în comparație cu Hemodiafiltration preddilyutsionnoy [32, 33].
Sa constatat că postdilyutsionnaya Hemodiafiltration a redus în mare măsură predializați legate de concentrație de toxine de proteine uremice în comparație cu membranele foarte permeabile pentru hemodializă. Cu toate acestea, în cazul în care rezultatele experimentale acute au arătat o reducere apreciabilă a conținutului acestor substanțe, utilizarea prelungită a tehnologiei de dializă au arătat rezultate ambigue [34].
În prezent, cel mai remarcabil sorbent AST- 120, care nu numai că reduce concentrația de indoxil-sulfat [40], și alte uremic legate de proteine toxina [41], dar, de asemenea, permite să întârzie timpul de start al hemodializa program de la pacienți cu insuficiență renală cronică [42] și lent reducerea procesului de filtrare glomerulară [43], și mărește durata de funcționare a pacientului după inițierea terapiei prin dializă [44].
Trebuie menționat faptul că metodele de adsorbție extracorporală în acest sens sunt decisive. De interes sunt studiile privind separarea fracționată a plasmei la pacienții cu insuficiență renală cronică, urmată de adsorbția pe un aparat care amintește de funcția unui ficat artificial. La grupul de pacienți uremici sa demonstrat o absorbție pronunțată a toxinelor uremice asociate proteinei cu sorbenți speciali [45]. Cu toate acestea, terapia de sorbție a fost complicată de apariția trombozelor datorate eliminării simultane a factorilor antitrombotici din organism [46]. Dializa peritoneală în funcție de caracteristicile sale de clearance nu a demonstrat un avantaj față de hemodializa cu flux înalt [47]. Cu toate acestea, în dializa peritoneală, concentrațiile scăzute de toxine uremice legate de proteine sunt observate în sânge, în timp ce clearance-ul lor este scăzut [48]. Se crede că acest tip de dializă ar trebui să aibă o capacitate mai scăzută a florei intestinale de a produce toxine [49]. Transplantul de rinichi duce la scăderea concentrațiilor sanguine de p-crezol și indoxilsulfat, care se corelează cu nivelul de filtrare glomerulară a rinichiului transplantat [50].
Se acumulează o cantitate tot mai mare de informații despre efectul dăunător asupra sistemului cardiovascular și a altor organe ale pacientului cu CRF asociat cu proteina toxinelor uremice. Datele de laborator și clinice arată că există o corelație între concentrația acestor substanțe, evoluția clinică și rezultatul bolii. Eliminarea acestor compuși din corpul pacientului este strict limitată prin utilizarea hemodializei standard, dar poate fi optimizată prin utilizarea metodelor convective pentru îndepărtarea acestora. Se adaugă optimismul și dezvoltarea metodelor de influențare a metabolismului bacteriilor intestinale și a adsorbanților interstenți care elimină produsele activității vitale. Transplantarea rinichiului duce la o scădere a concentrației toxinelor uremice. Nu există nicio îndoială că concentrația toxinei uremice asociate cu proteina din corpul pacientului crește odată cu scăderea ratei de filtrare glomerulară.
2. Bergstrom J, toxinele Furst P. Uremic. // Kidney Int Suppl. 1978. Vol. 8. P. 9-12
15. Curtius HC, Mettler M, Ettlinger L. Studiul metabolismului tirozinic intestinal folosind izotopi stabili și spectrometrie de masă cromatografică gaz-spectrometrie. // J Chromatogr. 1976. Vol. 126. P. 569-580.