electrod standard de hidrogen - electrod folosit ca electrod de referință la diferite măsurători electrochimice și în celule galvanice. Electrodul pH (RE) este o placă sau sârmă de metal, bine absorbant de hidrogen gazos (frecvent utilizat platină sau paladiu), saturat cu hidrogen (la presiune atmosferică) și imersat într-o soluție apoasă. care conține ioni de hidrogen. Potențialul plăcii depinde [specificată] concentrației de ioni H + în soluție. Electrodul este standardul față de care potențialul electrodului de numărare reacție chimică definită. La o presiune de hidrogen de 1 atm. concentrația de protoni în soluție 1 mol / l și o temperatură de 298 K potențial VE este setat la 0 V. Când ansamblul celulei electrochimice definit de electrozii RE și reacția reversibilă are loc pe suprafața de platină:
adică, este fie de recuperare a hidrogenului, sau oxidarea acestuia - depinde de capacitatea reacției apărând pe electrodul determinat. Prin măsurarea EMF electrodului electrochimice în condiții standard (vezi. De mai sus) determina potențialul de electrod standard, determinat prin reacție chimică.
Sunt utilizate pentru a -uri măsura potențialul de electrod standard a reacției electrochimice, pentru a măsura concentrația (activitatea) a ionilor de hidrogen și orice alți ioni. VE aplicat, de asemenea, pentru determinarea produsului de solubilitate, pentru a determina constantele de viteză pentru anumite reacții electrochimice.
Cele mai importante cerințe pentru electrodul de referință:
1) Electrodul trebuie să funcționeze în intervalul de temperatură.
2) Stabilitatea.
3) reproductibilitatea rezultatelor.
4) Trebuie să fie compatibil cu topitura de testare.
5) Absența potențialelor staționare.
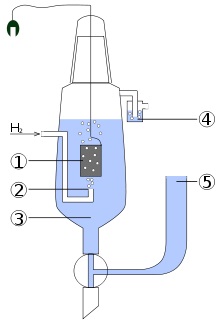
Schema de electrod standard de hidrogen:
- electrod de platină.
- Furnizat de hidrogen gaz.
- O soluție de acid (în mod tipic HCI), în care concentrația de H + = 1 mol / l.
- sigiliu de apă care împiedică pătrunderea oxigenului atmosferic.
- bridge electrolitica (constând dintr-o soluție concentrată de KCl), care permite atasarea a doua jumătate a celulei.
În ciuda complexității operațiunii (necesitatea unui flux constant de hidrogen gazos) electrodul de hidrogen a fost mult timp cunoscut.
- electrozi de hidrogen de proiectare proprii au fost lucrări un instrument central SP L. Sorensen. care a apărut ca rezultat al teoriei moderne a pH-metru (1909).
- In primele experimente de pe sonda intragastric pH-metrie pH a fost utilizat. JF McClendon. un electrod de referință în care electrodul de hidrogen a fost introdus în compoziția sondei pH în stomacul uman (1915).