Metionina. Acid neinlocuit cuprinde o grupă metil mobile care pot fi transmise altor compuși. Datorită acestui fapt, este implicat în sinteza de colină, fosfolipide metabolismul vitaminelor B 12 si acid folic. În reacțiile biosinteza proteinelor este metionină aminoacizi. El participă la procesele de neutralizare a toxinelor din ficat.
Metionina ( „atsimetion“) și derivații săi activi (ca substanță „ademetionină“ compus din medicament „Geptral“) este utilizat pentru prevenirea și tratamentul diferitelor boli ale ficatului ca factor lipotropic prevenirea acumulării de grăsime în leziuni toxice hepatice, ateroscleroza, si ca un antidepresiv pentru a îmbunătăți sinteza neurotransmițătorilor.
Acidul glutamic - este un precursor al acidului γ-aminobutiric (GABA), un neurotransmițător inhibitor al sistemului nervos (droguri „Aminalon“ „Pikamilon“). GABA joacă, de asemenea, un rol important în reglarea tonusului vaselor cerebrale circulației sanguine cerebrale. Neurotransmitatorul glutamat in sine este un aminoacid, care permite transferul de excitație în sinapsele SNC. In plus, glutamat este implicat în îndepărtarea amoniacului, sinteza bazelor purinice și pirimidinice, joacă un rol important în metabolismul altor aminoacizi. nevoia organismului de acid glutamic mai mare decât toți ceilalți aminoacizi.
Glicina este un neurotransmitator al acțiunilor inhibitoare ale SNC. Acesta îmbunătățește metabolismul în țesutul cerebral. Are un efect calmant. Normalizarea somn, reduce imbunatatit iritabilitate, depresie.
Cisteina este implicată în metabolismul cristalinului ochiului. De multe ori, încălcări ale cristalinului asociate cu lipsa de cisteină, astfel cisteină utilizată în stadiile inițiale ale cataractei.
preparare Complex de acid glutamic, cisteină și glicină „Vitsein“ este utilizat sub formă de picături pentru ochi.
Histidina - condiționat esențial aminoacizi. Folosit în tratamentul hepatitei, ulcere gastrice și ulcer duodenal.
Structura, proprietățile și clasificarea aminoacizilor și a proteinelor
Cerebrolysin - Hidrolizat substanta creier de porc care conține peptide cu greutate moleculară scăzută (15%) și aminoacizi (85%). Este utilizat în tulburări ale sistemului nervos central, leziuni cerebrale, hemoragiile, distonia vegetativa, etc.
Formulările pentru nutriție parenterală: poliamine (un set de 13 aminoacizi) Vamin (set 18 aminoacizi) vaminolakt (set de 18 aminoacizi corespunzătoare compoziției laptelui matern) gidrolizina (proteine sanguine hidrolizatul bovine) aminotrof (cazeină hidrolizată), Aminosol (amestec 15 aminoacizi), fibrinosol (hidrolizate sângelui fibrinei).
Proprietățile fizice ale aminoacizilor
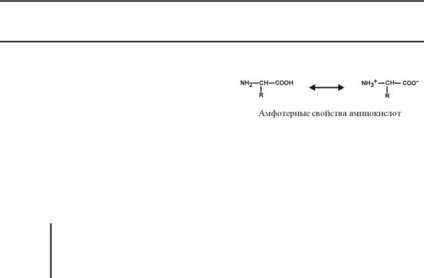
1. Sunt electroliți amfoteri. Aminoacizii combină proprietățile și
acizi și baze. Prin urmare, într-o soluție apoasă de aminoacizi se comportă ca - și ca bază donor de protoni - acceptori de protoni.
În cazul în care sarcina totală a aminoacizilor este 0, atunci această condiție este numită izoelectrică ei. Marii
masca pH-ul la care încărcătura de aminoacizi egal cu 0 este numit punctul izoelectric (pI, pI). punctul izoelectric depinde de structura radicalilor de aminoacizi:
o pI majorității aminoacizilor este situată în intervalul de pH de la 5,5 (fenilalanină) la
o pl amino acizi acizi - pI glutamat 3.2, pI 2.8 aspartat,
o pl aminoacizi esențiali - pI de histidină, pI arginină 7,6 10,8, pI 9,7 lizină.
Izoelektrichesaya punctul histidină îi permite să fie utilizat în sistemul tampon de hemoglobină în care este conținută într-o cantitate mare. Hemoglobina este ușor primește și trimite ioni de hidrogen ușor la cea mai mică Deplasările pH sanguin fiziologic (normal 7,35-7,45).
2. aminoacizi Charge depinde de pH-ul mediului.
Punctul de plecare pentru înțelegerea cauzelor responsabile la aminoacidul este valoarea punctului izoelectric. Situația este diferită de aminoacizi neutri, acizi și bazici.
Structura și proprietățile legăturii peptidice
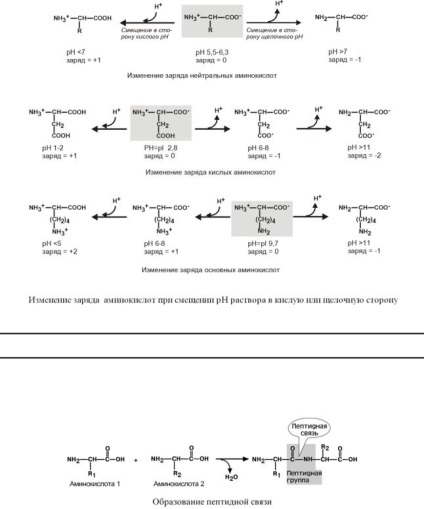
Aminoacizii pot fi interconectate legături numite peptidă. formând astfel o moleculă de polimer.
Legătura peptidică - este relația dintre gruparea α-carboxil a unui aminoacid și gruparea amino-α a unui alt aminoacid.
Dacă este necesar, apelați o peptidă de aminoacizi la toate numele adăugate la sufixul „-il“, numai ultimul aminoacid își păstrează numele neschimbată.
De exemplu, alan il -series il -triptof en -glutamin il sau -glits yn il y-cisteină (altfel numit glutation).
Prin peptida proprietăți obligațiuni includ:
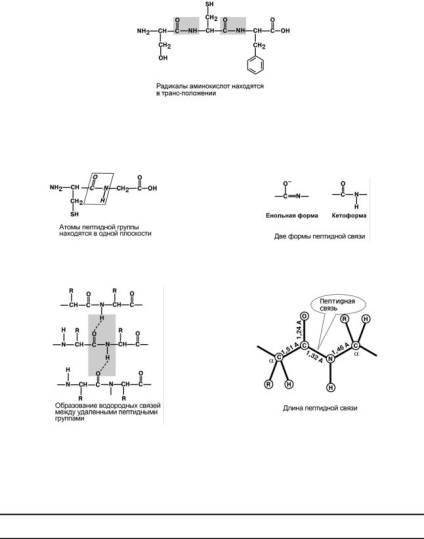
1. substituenți trans (radicali) de aminoacizi în raport cu legătura C-N.
Structura, proprietățile și clasificarea aminoacizilor și a proteinelor
Toți atomii sunt incluși în grupul de peptide sunt în același plan, atomii „H“ și „O“ sunt aranjate pe fiecare parte a legăturii peptidice.
3. Prezența formei formă cetonică și enolică Noy.
4. Capacitatea de formarea a două legături de hidrogen cu alte grupuri de peptide.
5. Legătura peptidică are caracter dublă legătură parțială. Lungimea sa este mai mică decât o legătură simplă, este o structură rigidă, iar rotația în jurul dificilă.
Dar, din moment ce, în plus față de o peptidă, proteină, există alte lanț de comunicare aminoacizi este capabil să se rotească în jurul axei principale, ceea ce dă o conformație diferită de proteină (aranjare spațială a atomilor).
CARACTERISTICI DE PROTEINE
o în țesut conjunctiv - colagen, elastină, cheratina,
o construirea membranelor și citoscheletului (integral și proteine de suprafață poluintegralnye) - spectrin (superficial, eritrocitare citoscheletului proteinei bazice), glicoforin (integral, fixează spectrin pe suprafață),