Mai puțin frecvente decât reacția de oxidare. Cu toate acestea, în cazul în care forma redusă a compusului este cel mai bine eliminat din organism, atunci legea de schimburi de reacție de acțiune în masă în direcția de recuperare.
- Recuperarea de aldehide și cetone la alcooli.
- Reducerea grupărilor nitro și azoaromatici.
- disulfuri de recuperare (clivaj lor reductivă pentru a forma tioli).
- Recuperarea legături duble compuși alifatici și aliciclici (de exemplu, ciclohexenă).
- Dehidroxilare (de exemplu, conversia catecholi la Monofenoli).
- Recuperarea atomilor valență variabilă (de exemplu, arsenites în arsenite, selenites la selenat).
- Reducerea ciclurilor aromatice (unele organisme anaerobe).
reacția de degradare (scindare)
- Hidroliza esterilor (de exemplu, alcaloizi din [atropina, cocaina] Multe pesticide [2,4-D, adică acidul diclorfenoxiacetic] Mulți compuși organofosforici).
- Hidroliza amide, hidrazide și nitrili (de exemplu, pesticide de degradare fenilamidă).
- Dezalchilare.
- Despicarea structurilor inelare.
Reacțiile degradării substanțelor organice exogene este foarte importantă pentru purificarea microbiologică a apei poluate, în special de substanțe aromatice, deșeuri industria alimentară, producția biotehnologică de agenți activi de suprafață și alți contaminanți.
În anumite situații, aceste reacții sunt moduri foarte effektiktivnymi de reducere a toxicității unor xenobiotice, cu toate că, în unele cazuri formate cancerigene mai periculoase.
Conjugarea mai studiat:
1. acetat (donor - acetil CoA, atsetiltrasferazy enzime).
2. Gly (conjugare glicină cu acidul benzen - unul dintre primii studiat reacțiile de biotransformare).
3. cisteină, glutation și alți compuși care conțin sulf.
4. Metilarea (de exemplu implicând metionină).
5. ornitina și arginină.
7. Deoarece riboza si glucoza.
8. acid glucuronic.
9. conjugare sulfat.
Separarea acestui grup de reacții, datorită importanței lor asupra mediului.
1. hidrolitice dehalogenată.
2. dehalogenarea reductivă.
3. dehalogenarea oxidativ.
4. Funcționarea microzomal
Microzomii - o vezicule morfológicamente închise în reticulul endoplasmic, care este transformat cu omogenizare tisulară. Veziculele Partea microzomale pot exista in celulele intacte in rezervoare si vacuole separate.
Compoziția chimică a fracțiunilor microzomale:
3 componente ale bubble microzomal:
1. Spațiul interior cu conținutul său,
2. membrană direct
3. Compus proteiformă sau neproteinacei ribozom sorbită pe suprafața exterioară a membranei.
membrană microzomala conține trei clase de proteine: enzime, proteine structurale și proteine secretate de ficat.
Sistemul monooxigenazică reticulul endoplasmic al celulelor hepatice, care cuprinde citocromul P-450 implicat în următoarele procese:
- inactivarea sau activarea agenților terapeutici;
- transformarea medicamentelor sau a altor substanțe organice în molecule foarte active, care pot avea efecte dăunătoare nedorite asupra celulei, induce moartea celulelor sau cauzează ADN mutant activ;
- biosintezei hormonilor steroizi (cel puțin, participă la diferitele etape ale sintezei steroizilor);
- metabolismul acizilor grași și derivații lor.
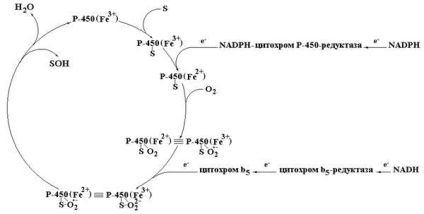
În varianta de realizare extrem de simplificată, schema generală a funcționării multienzimatic hepatice microsomale sistemul citocromului P-450 ca oxidază terminală este după cum urmează:
- în prima etapă a procesului există o interacțiune a substratului cu citocromul P-450, pentru a forma o dublă enzimă-substrat complex (interacțiunea citocromul P-450, cu un substrat de o natură diferită este însoțită de modificările spectrale corespunzătoare ce caracterizează natura suportului);
- într-o a doua etapă, rezultând complexul dublu enzimă-substrat, recuperarea prima sursă de electroni, care este NADPH și donor de electroni direct pentru citocromul P-450 - NADPN citocromului P-450 reductaza. Când ferri- (Fe +3) are loc această tranziție a citocromului P-450 forma a în Ferro (Fe + 2) forma a;
- Reducerea dublei complex de interacțiune primul electron creează condiții pentru complexul dual-enzimă-substrat cu o moleculă de oxigen pentru a forma un complex ternar - P-450-S-O2;
- recuperarea complexului ternar format donor de electroni al doilea care este un lanț de electroni de transport care cuprinde NADH, NADH-citocrom reductaza b5 și citocrom b5. Aceasta conduce la activarea oxigenului molecular. În care un atom este încorporat în molecula de substrat, iar cea de a doua formă de apă.
Schema de funcționare a sistemului monooxigenază al reticulului endoplasmatic al hepatocitelor (vezi. De mai jos).
Sistemul hidroxilare microzomal al ficatului metabolizeaza multe medicamente, substanțe cancerigene, anestezice și alte xenobiotice. Deoarece apar reacții de citocromul P450 microzomal hidroxilare, dezalchilare, N- și S-oxidare, precum și o varietate de alte procese. Toate au ca scop obținerea compușilor lipofili, nepolare în hidrofil, polar, care apoi sunt excretați cu ușurință. pluralitate de reacție Neutralizarea compuși străini sunt reduși la oxidare, hidratare și conjugare. Reacții foarte importante care apar în reticulul endoplasmatic al celulelor hepatice sunt procese de hidroxilare a compușilor aromatici, deoarece produsele acestor reacții joacă un rol important în procesele de necroză tisulară, intoxicațiile, carcinogeneza și mutageneza.
Citocromul P-450, constituie o familie de enzime furnizează metabolismul diferiților compuși lipofili atât origine endogenă și exogenă catalizează multe reacții, care includ:
- Reacțiile hidroxilare simple de atomi de carbon de grupe metil;
- introducerea unei grupări OH în alcanii metilen carbon;
- hidroxilarea inelelor aromatice pentru a forma fenoli;
- introducerea atom de oxigen în inelul aromatic și legăturile duble pentru a forma epoxizi. În acest caz, epoxizii pot rupe neenzimatic până la grupe alcool sau prin intermediul unui suplimentar hidrolază enzimă epoxid, adăugarea de apă la gruparea epoxi, derivați ai alcoolului;
- Reacțiile dezalchilare în care se introduce atomul de oxigen la C-H legătură, iar produsul a fost atât de instabil încât reoganizat într-un alcool primar, amină sau derivat sulfhidril;
- azot de oxidare, sulf sau fosfor, reacția dehalogenarea este de asemenea catalizată de citocromul P-450;
- familia enzimelor citocromului P-450 sunt capabile să scindeze legătura C-C și alcooli oxidanti la aldehide.
In multe cazuri, acțiunea citocromului P-450 rezultate în formarea compușilor farmaceutici cu activitate scăzută sau toxice, care sunt excretați ulterior ușor. La rândul lor nemodificată sau modificată citocrom P-450 xenobioticelor pot suferi modificări suplimentare care implică alte sisteme enzimice localizate predominant în ficat, formarea de produse care oferă mai puțin toxice și ușor excretat. Tabelul de mai jos prezintă o listă a celor mai importante enzime implicate in detoxifierea xenobioticelor.
5. Etapa a II-biotransformarea xenobioticelor -
Xenobioticelor având grupări reactive (-OH, -COOH, -NH2, -SH), vin în animale și ficat uman în reacția de conjugare.
În anumite situații, aceste reacții sunt metode foarte eficiente de reducere a toxicității unor xenobiotice, cu toate că, în unele cazuri formate cancerigene mai periculoase.
1. glucuronoconjugare cu acid glucuronic. Localizate în reticulul endoplasmatic. Introduceți substanțe cu acid glucuronic formează:
O-glucuronid: fenoli, acizi carboxilici alifatici, cetone, hidroxilamine;
N-glucuronoconjugați: carbamați, amide formând arii, sulfonamide;
S-glucuronid: formarea arylmercaptan, acizi dithiocarboxylic;
C-glucuronid: formarea fenilbutazona si altele.
Glucuronidă conjugare începe cu formarea de difosfat uridin (UDP-Glc) de la UTP și glucoză-1-fosfat. Apoi oxidate UDP-Glc dehidrogenază UDP-glucoză în prezența NAD + la acid UDP-glucuronic pentru a forma NADH. În final, reziduul a fost transferat glyukuronilny UDP-glucuronoziltransferaza pe xenobiotice cu UDP-release. Aceasta este o etapă cheie.