Acesta este un grup mare de substanțe - hidrocarburi, care corespund formulei generale
unde n este orice număr întreg nu egal cu 0.
Seria omologică de alcani a fost studiată de chimistul german Karl Schorlemmer. O întreagă serie de oameni de știință - chimisti - au contribuit la studiul reprezentanților concreți ai alcanilor.
Seria începe cu cel mai simplu alcan - metan CH4. Puteți cunoaște cei mai importanți reprezentanți ai alcanilor din tabelul 2. Toate hidrocarburile diferă una de alta pentru o anumită diferență omologică "CH2". Seria omologică de alcani, ca și alte substanțe, este condițional infinită. Până în prezent, sunt cunoscuți compuși care conțin un număr foarte mare de atomi de carbon.
Ultimii hidrocarburi, ca toți membrii aceleiași serii omoloage, au elemente structurale similare, principiile nomenclaturii și proprietăților chimice. Activitatea lor chimică scăzută, cauzată de o structură specială, a condus la unul dintre denumirile de clasă - "parafină", care simbolizează inerția lor.
Alcanii sunt larg răspândiți în natură și au o mare importanță industrială.
2. Structura alcaniilor:
Hidrocarburile limitate, fiind saturate, conțin în compoziția lor atomi de carbon care se află în starea de 1 valență a hibridizării sp3. Cu acest tip de hibridizare, norii hibrizi sunt aranjați în spațiu sub forma unui tetraedru. (Figura 1). Unghiul valent (distanța dintre axele pe care se află norii de electroni) este de 109 grade 28 de minute.
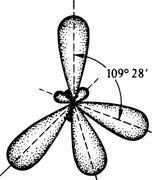
Fig. 1. Localizarea noriilor de electroni în prima stare de valență a atomului de carbon
perechi electronice, nu există abateri de la unghiul de valență în moleculele de alcani. Valența carbonului în hidrocarburi saturate, ca în toate celelalte substanțe organice, este IV.
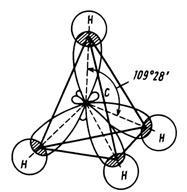
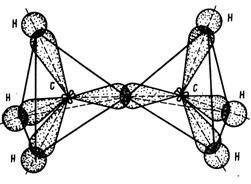
Fig. 2. Structura tetraedrică a moleculei de metan
Homologii metanului, în spațiu, au o structură mai complexă. Vârfurile tetraedrului sunt conectate. Figura 3 prezintă structura electronică a etanului.
Dacă luăm în considerare hidrocarburile cu un lanț mai lung de atomi de carbon, putem observa că moleculele de alcani din spațiu au o formă zigzagă (Figura 4).