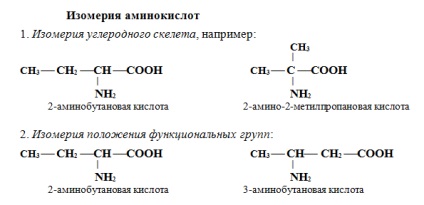
Conform nomenclaturii sistematice, numele aminoacizilor se formează din numele acizilor corespunzători prin adăugarea unei atașări a amino și indicând localizarea grupării amino în raport cu gruparea carboxil.
Adesea folosit, de asemenea, o altă metodă de construire nume de aminoacizi, conform căruia numele trivială prefixată amino acid carboxilic prezentând poziția literei amino a alfabetului grecesc. exemplu:
Pentru a-aminoacizii, care joacă un rol deosebit de important în procesele de activitate vitală a animalelor și plantelor, sunt folosite denumiri triviale.
Dacă există două grupări amino în molecula de aminoacizi, atunci numele său utilizează un atașament diamino. trei grupări NH2 - triamino etc.
Prezența a două sau trei grupări carboxil este reflectată în sufixul numelui -da sau acidul tricic:
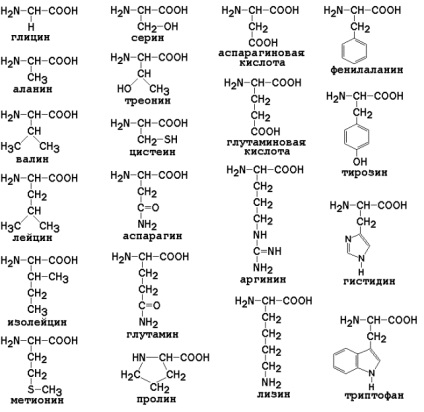
Toți-amino acizi cu excepția unei glicină H2N-CH2-COOH, conțin un atom de carbon asimetric (un atom) și pot exista sub formă de oglindă-antipozi.
Izomerismul optic al aminoacizilor naturali joacă un rol important în procesele de biosinteză a proteinelor.
Proprietăți fizice. Aminoacizii sunt substanțe cristaline solide cu un punct de topire ridicat. când topirea se descompune. Ei bine solubili în apă, soluțiile apoase sunt conductive din punct de vedere electric. Aceste proprietăți se explică prin faptul că există molecule de aminoacizi sub formă de săruri interne care se formează datorită transferului protonului de la carboxil la gruparea amino
Aminoacizii prezintă proprietățile bazelor datorită proprietăților de amino acizi și datorită grupărilor carboxil t.e.yavlyayutsya compuși amfoterici. In mod similar amine, ele reacționează cu acizi pentru a forma săruri de amoniu ale:
Ca acizi carboxilici formează derivați funcționali:
b) esteri
În plus, este posibil amino interacțiune și grupări carboxil într-o singură moleculă (reacție intramoleculară pentru g-, d- e- aminoacizi, etc.) și molecule diferite (reacție intermoleculară).
Semnificația practică este interacțiunea intramoleculară a grupărilor funcționale de acid e-aminocaproic, care este format ca urmare a e-caprolactamei - intermediar pentru producerea de nailon.
Interacțiunea intermoleculară a a-aminoacizilor conduce la formarea de peptide. Interacțiunea a doi a-aminoacizi produce o dipeptidă. Interacțiunea intermoleculară a trei a-aminoacizi conduce la formarea unei tripeptide, etc.
Fragmentele moleculelor de aminoacizi care formează catena peptidică sunt numite reziduuri de aminoacizi, iar legătura CO-NH este o legătură peptidică.
