Această problemă este interesantă, deoarece în prima etapă are loc o reacție, ale cărei produse participă la două reacții paralele.
Problema 3.8.
Determinați masa de nitrură de magneziu complet descompusă de apă, dacă s-a cerut 300 ml de soluție de acid clorhidric 4% (p = 1,02 g / ml) pentru a se sare cu produsele de hidroliză.
având în vedere:
volumul de acid clorhidric: Vp-ra (HC1) = 300 ml;
Fracția de masă a acidului clorhidric în acid clorhidric: (HCI) = 4%;
densitatea acidului clorhidric: pp-ra (HC1) = 1,02 g / ml.
Găsiți: masa de Mg3N2.
soluţie:
În starea problemei, sunt descrise mai multe reacții chimice consecutive.
Ambele produse din prima reacție vor reacționa cu acid clorhidric pentru a forma săruri.
Soluția acestei probleme trebuie realizată cu formularea unei ecuații matematice. Schematic, algoritmul poate fi reprezentat astfel:
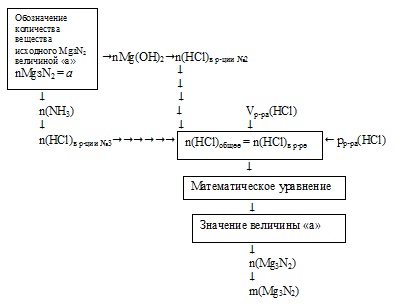
1. Să desemnem cantitatea de substanță1 a Mg3N2 originală ca "a": n (Mg3N2) = a mol.
Folosind valoarea "a" după cum se știe, din prima ecuație chimică determinăm cantitatea de substanță a fiecărui produs:
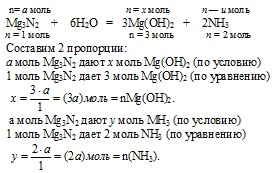
2. Pentru a doua reacție chimică, determinăm cantitatea de substanță HCI consumată pentru formarea sării cu (3a) mol Mg (OH) 2.

3. Pentru a treia reacție chimică, determinăm cantitatea de substanță HCI consumată pentru formarea sării cu (2a) mol de MH3.
4. Determinați cantitatea totală de HC1, consumată în reacțiile nr. 2 și nr. 3, pe baza rezultatelor de calcul din cele două operații anterioare.
n (HCI) total = n (HCI) în p-tinta nr. 2 + n (HCI) în p-tinta nr. 3 = 6a + 2a = (8a) mol.
5. Determinați cantitatea de HCI care a fost conținută în 300 ml dintr-o soluție de 4% (conform condiției):
6. Noi compunem ecuația matematică. Pentru aceasta, echivalăm cantitatea de substanță HC1 determinată prin calcul în conformitate cu ecuațiile chimice (de la 4 acțiuni) și valoarea găsită în pasul 5:
Rezolvind această ecuație matematică, găsim valoarea cantității "a":
Cantitatea "a", am indicat cantitatea de substanță din Mg3N2 originală. n (Mg3N2) = 0,042 mol.
7. Determinați masa substanței inițiale:
- Sunteți aici:
- principal
- sarcini
- EGE-chimie
- Determinarea masei de nitrură de magneziu | Cercetarea EGE de chimie