Concepte și definiții de bază
Obiectul termodinamicii este un sistem termodinamic - un corp macroscopic închis în spațiu sau un set de corpuri care se află în interacțiune termică și mecanică între ele și cu mediul. În mediul înconjurător se înțelege tot ceea ce nu este inclus în sistemul termodinamic. Suprafața imaginară sau fizică care separă sistemul termodinamic de mediul înconjurător se numește coajă a sistemului.
Metoda termodinamicii este fenomenologică (descriptivă) fără pătrunderea în structura materiei. Răspunsul sistemului la influențele externe este investigat, fără a se îndrepta spre cauzele acestui sau acel comportament al materiei, termodinamica nu interesează ipoteza structurii moleculare a materiei. Ne vom îndrepta spre teoria moleculare-cinetică pentru a calcula anumite proprietăți ale substanțelor, ale căror valori trebuie să fie luate din experiment.
Tehnologia termodinamică tehnică studiază problemele de transformare a căldurii în muncă în mașinile termice în termeni de eficiență maximă. Calculul termodinamic al motoarelor termice se bazează pe două principii de termodinamică, formulate sub forma unor afirmații despre imposibilitatea fundamentală de a construi motoare eterne de primul și al doilea tip.
Pentru descrierea cantitativă a comportamentului unui sistem termodinamic se introduc parametrii de stare - cantități care determină în mod unic starea sistemului la un moment dat. Parametrii de stat pot fi găsiți numai pe baza experienței. Abordarea termodinamică necesită ca acestea să poată fi măsurabile experimental folosind instrumente macroscopice. Numărul de parametri este mare, dar nu toți aceștia au o mare importanță pentru termodinamică. In cel mai simplu caz, orice sistem termodinamic trebuie să aibă patru parametri macroscopici: masa volumului M. V. presiunii p și temperatura T. Primele trei sunt definite simplu și bine cunoscute în cursul fizicii.
Se pot da cel puțin patru determinări ale temperaturii, a se vedea [1]:
temperatura - este o măsură a încălzirii corpului, adică sentimentul subiectiv de căldură sau frig;
temperatura - este indicația unui dispozitiv special numit termometru;
temperatura este o cantitate proporțională cu energia cinetică medie a moleculelor;
diferite combinații ale primelor trei definiții.
Toate aceste definiții nu au acuratețe și unicitate, spre deosebire, de exemplu, de definițiile de masă sau de volum. Cazul cu temperatură este unic în practica științifică - a fost prima dintre cantitățile fizice pe care am învățat să le măsurăm fără să știm ce este. Nici unul dintre termometre nu măsoară direct temperatura, ci unul sau alt efect asociat cu o schimbare a temperaturii. De exemplu, termometrele cu mercur, alcool sau gaz măsoară modificarea volumului cu o schimbare a temperaturii la presiune constantă; Termometrul de rezistență captează schimbarea rezistenței electrice cu o schimbare a temperaturii; Pirometrul conectează cu temperatura luminozitatea corpurilor încălzite la temperaturi ridicate etc. O determinare riguroasă a temperaturii și a scalei de temperatură în cadrul termodinamicii dă cea de-a doua lege a termodinamicii în legătură cu examinarea ciclului Carnot.
Primele instrumente pentru măsurarea temperaturii au fost proiectate de Galileo (c.1597) și s-au bazat pe o schimbare a volumului de gaze atunci când au fost încălzite.

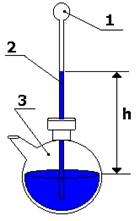
Figura 1.1. Termoscopul lui Galileo.
Principala dificultate în construirea termometrelor a fost alegerea scalei. Prima scară de temperatură a fost propusă în 1724 de către olandezul de sticlă dulce D. Farengate. Apoi au intrat în uz Scala Reaumur și Celsius. Și, în sfârșit, în 1848, fizicianul englez William Thomson (Lord Kelvin) a introdus o scară de temperatură absolută. numită și scala Kelvin. în care zero este considerat punctul de referință al temperaturii. când toate tipurile posibile de mișcare a particulelor din corp încetează teoretic. În rest, scara de temperatură absolută introdusă de Kelvin coincide cu scala Celsius. În fizica modernă, un punct triplu de apă este ales drept punct de referință. La scara Kelvin, temperatura de 273,16 K este atribuită punctului triplu de apă. Punctul de îngheț al apei (topirea gheții) are o temperatură de 273,15 K.