SINTEZA STEREOSELECTIVĂ
SINTEZA STEREOSELECTIVĂ. reacții, de preferință sau exclusiv conducând la formarea unuia dintre spațiile posibile. izomeri (vezi izomerismul). Astfel de reacții se numesc stereoselective. De exemplu, după reducerea 4-t-butilciclohexanonei I cu Na [BH4], alcoolul corespunzător se formează în cele bazice sub forma izomerului trans:
Reacțiile în care materiile prime sunt stereoizomeri transformându-se în stereoizomeric diferite produse menționate de stereospecifică. De exemplu, 2,3-dibromyantar format Nye al acidului IV sub forma treo (b) -pair (racemat), în timp ce acidul V fumaric (izomer trans), cu un bromurare de acid ma-leinovoy III (izomer cis) Aceleași condiții dau compusul IV sub forma unei meso-forme:
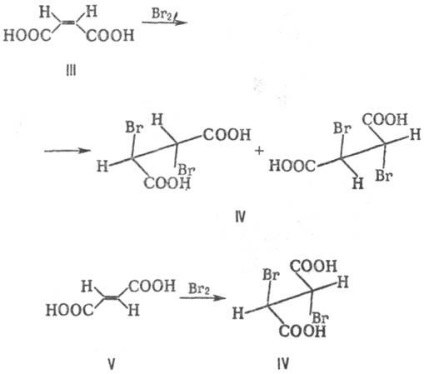
Toate reacțiile stereospecifice sunt în mod necesar stereoselective, în timp ce conversația nu este adevărată. De exemplu, ambii p-diastereomeri ai esterului etilic al acidului b-clorinamic, VI interacționează cu compusul organo-magneziu cu avantaje. formarea aceluiași compus VII. În consecință, această reacție este stereoselectivă, dar nu stereospecifică.
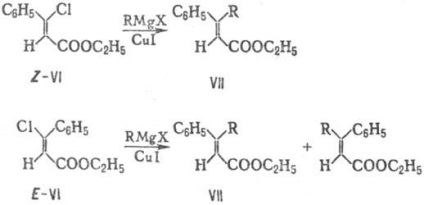
EXEMPLU reacție nestereoselektivnoy-hidratarea Z- și E-2-butenă VIII, care rezultă, în ambele cazuri la racemic. amestecuri de R- și 5-2-butanoli IX:
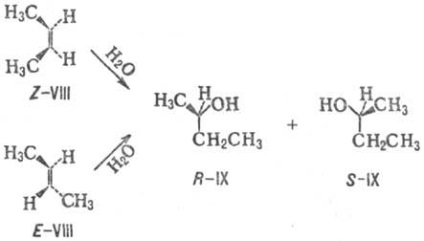
Pentru reacțiile care implică un compus care nu are stereoizomeri, conceptul de stereospecificitate nu poate fi aplicat. Reacția unui astfel de substrat nu poate fi decât stereoselectivă. De exemplu, adăugarea de brom în metil acetilenă X conduce la avantaje. formarea de trans-1,2-dibrompropan XI:
În mod tipic, există două tipuri de selectivitate, dintre care unul se referă la substrat (selectivitatea substratului), iar celălalt la produsele de reacție (selectivitatea produsului). Selectivitatea substratului expusă de stereoizomeri este subdivizată în diastereoselectivitatea substratului și enantioselectivitatea substratului. Enantioselectivitatea substratului în terminologia modernă se referă la transformările enantiomerilor cu viteze diferite sub acțiunea luminii circular polarizate sau non-racemice. reactiv chiral.
Diastereoselectivitatea substratului se datorează diferenței de reactivitate a diastereomerilor față de k. reactiv. Astfel, oxidarea cyclohexanols diastereomerice II și XII conduce la același produs XIII cu viteze diferite, cum ar fi 80% Kax acid acetic / keq = 3,2 pentru reacția următoare (ax-axial, eq-ecuatorial):
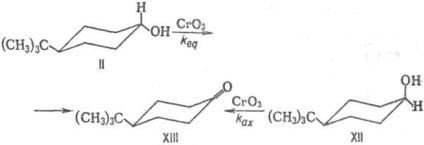
Diastereomerii pot fi transformați în diferite produse diametre dimensionale cu viteze diferite (k1> k2), cum ar fi, de exemplu, în debrominația 2,3-dibrombutanelor diastereomerice XIV:
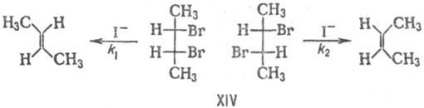
Diferența dintre ratele de reacție ale diastereomerilor poate fi atât de mare încât una dintre ele se dovedește a fi nereactivă. De exemplu, (b) -1,2-diclor-1,2-difeniletanul XV este dehidroclorurat în piridină la 200 ° C și izomerul său meso este inert în aceleași condiții.
Diastereomerii pot fi transformați în compuși non-diastereomeri, precum și la un compus cu diferite structuri, care este clar prezentat în clasic. un exemplu de rearanjare Beckmann pentru E și Z-oximele XVI:
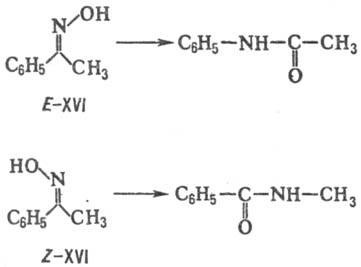
In 1971 clasificarea I. Izumi reacțiilor stereose lective bazate pe simetria substratului. Conform acestei clasificări, reacțiile care conduc la cantități inegale de stereoizomeri se numesc stereodiferențieri. În funcție de natura substratului la acest titlu adăuga prefixele „enantio“ și „dia-stereo“ (în cazul stereoizomeri), „enantiotopno“ și „diastereotopic“ (în cazul în grupuri diferite), „enantio FASD“ și „diastereofasno“ ( în cazul în care transformarea afectează laturile substratului).
Pentru enantiostereodifferentsiatsii apariție necesar impact asupra agentului chiral substrat, în timp ce pentru diastereodifferentsiatsii nu este necesar. . Cu alte cuvinte, cheia enantiodifferentsiatsii servește mediu (reactiv, solvent, catalizator), în timp ce un diastereodifferentsiatsii cheie prevăzută în moleculă (spații cu dificultăți efecte stereoelectronice; .., A se vedea stereochimie dinamic).
Formarea diastereomerilor ca produse de reacție implică în mod necesar stări de tranziție diastereomerice, ale căror energii nu sunt aceleași. Ca rezultat, diastereoizomerii sunt întotdeauna formați în cantități inegale. Prin urmare, ori de câte ori este posibilă formarea de diastereomeri, se poate presupune că acestea sunt obținute în cantități inegale. Raportul observat al produselor este controlat sau relativ diferit. ratele formării lor (stereoselectivitatea controlată cinetic) sau constanta de echilibru a produselor (selectivitate controlată termodinamic) sau ambele.
Factorii care controlează diastereoselectivitatea pot fi împărțite în stereoelectronice pur spațială (sterica). De exemplu, brom unește rezultate noi malei acid III în formarea de acid 2,3-dibromyantarnoy IV sub forma treo (b) -pair care este bine explicată pe baza mecanismului de reacție care apar exclusiv ca antiprisoedinenie (control stereoelectronice).
Reacția Diels-Alder între diene ciclice și dienofilele asimetrice în majoritatea cazurilor, se produce în principal ca endo-plus (control sterica):
Beneficii. formarea alcoolului axial termodinamic mai puțin avantajos XVIII în timpul reducerii ciclohexanonei XVII este rezultatul acțiunii coordonate a spațiilor. factori: obstacole sterice create pentru abordarea hidrură de ioni de către gruparea metil axială la atomul C-3 și cea mai mare parte a agentului reducător:
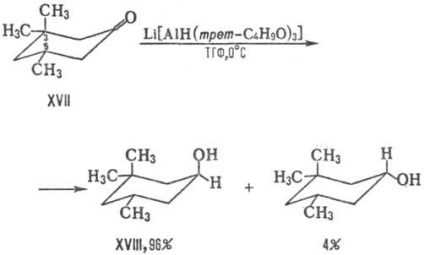
Termenii "stereoselectivitate" și "stereospecificitate" sunt uneori utilizați într-un sens ușor diferit. Astfel, unii cercetători numesc reacții stereospecifice cu mare (peste 98%) stereoselectivitate, altele propune aplicarea conceptului de selectivitate pentru a reflecta caracteristicile selecției începând de izomeri ai substratului, iar termenul-specificitate pentru a caracteriza fluxul reacției și compoziția izomerică a produșilor de reacție. Un caz special este SINTEZA STEREOSELECTIVĂ - sinteza asimetrică.
Literatură: Mislow K. Raban M. în carte. Probleme selectate de stereochimie, trans. cu engleza. M. 1970; Izumi I. Tai, A. Reacții de diferențiere stereo, Per. cu engleza. M. 1979; Nogradi M. Sinteza stereoselectivă, trans. cu engleza. M. 1989. E. L. Gaidarova.
Enciclopedii chimice. Volumul 4 >> La lista articolelor