Stronțiul se află în a cincea perioadă a grupului II din subgrupul principal (A) al tabelului periodic.
Se referă la elementele familiei s. Metal. Desemnarea - Sr. Numărul de serie este 38. Masa atomică relativă este 87,62 amu.
Structura electronică a atomului de stronțiu
Atomul stronțiu constă dintr-un nucleu încărcat pozitiv (+38), în interiorul căruia sunt 38 de protoni și 50 de neutroni, iar în jur, 38 de electroni se mișcă în cinci orbite.
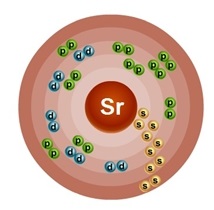
Fig.1. Schema schematică a atomului de stronțiu.
Distribuția electronilor de-a lungul orbitalilor este după cum urmează:
Nivelul energetic extern al atomului de stronțiu conține doi electroni, care sunt valenți. Diagrama energetică a stării de bază are următoarea formă:
Electronii de valență ai atomului de stronțiu se caracterizează printr-un set de patru numere cuantice: n (cuant principal), l (orbital), ml (magnetic) și s (rotație):
Specificați ce orbital atomic și de ce alegeți următorul electron în conformitate cu principiul celui mai mic de energie: 3d sau 4p, 5s sau 4d, 4s sau 3p, 4d sau 5p.
Umplerea orbitalilor cu electroni are loc în conformitate cu principiul Pauli, regulile lui Klechkovsky și Hund. Mai întâi, electronii sunt umpluți cu cea mai mică valoare a sumei (n + 1), unde n este numărul cuantic principal și l este numărul cuantal orbital. Dacă această sumă este aceeași pentru mai multe subsoluri, orbitalul cu cea mai mică valoare n este umplut primul.
Apoi, din cele două orbite (suma n + 1) 3d (5) și 4p (5) este indicată în paranteze, 4p-orbitalul va fi umplut primul; din 5s (5) și 4d (6) - 5s-sublevel; din 4s (4) și 3p (4) - 3p-sublevel; din 4d (6) și 5p (6) la 4d este un sub-nivel.