Histologie. Clasificarea originală a tipurilor histologice de rabdomiosarcom la copii, descris în 1958, combină o tumoare a anumitor tipuri de celule, cum ar fi embrionara, alveolar, botrioidnye si de celule polimorfonucleare. Un studiu al histologiei tumorii în IRS a adăugat la această clasificare primitivele mici celule de sarcoame I și II și forme nedefinite nediferențiate.
Tipurile favorabile includ embrionare, inclusiv varianta botryoidă, sarcomul Ewing extra-ejaculator și tipuri de tumori nediferențiate sau mixte. Din punct de vedere histologic, sunt luate în considerare tumorile celulare alveolare și anaplazice sau monomorfice (Tabelul 70-4). Caracterul histologic al tumorii, determinat la stabilirea diagnosticului, este luat în considerare în programele curative moderne și determină modificările metodelor de tratament, în special intensitatea terapiei.
Tabelul 70-4. Tipuri histologice de rabdomiosarcom

Tumorile embrionare. Tumorile celulelor embrionare constau din micoblaste mici, rotunjite, fuziforme. Acest tip de celule apare de obicei în tractul genito-urinar, precum și în cap și gât. Acesta este cel mai frecvent tip de celule observate la copiii cu rabdomiosarcom (Fig. 70-5).
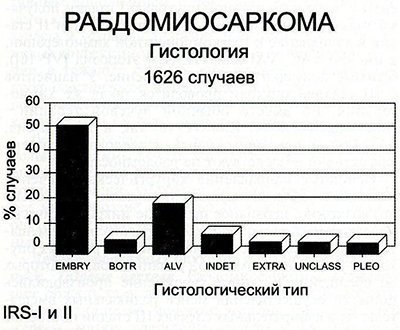
Fig. 70-5. distribuția tumorală de vedere histologic a 1626 de pacienti din studiu Rhabdomyosarcoma Intergrupului. Tipul fetale a fost cea mai frecventă - 54%. Tumorile alveolare au fost observate la 21% din cazuri. (Embry - embrionara, BOTR - botrioidnaya, ALV - alveolar, INTED - tumora vnekostnaya Ewing, UNCLASS - - nedefinit, EXTRA nu se încadrează în clasificarea, Pleo - Polimorf).
Mai mult de 60% din cazuri, conform datelor noastre, se referă la tumorile embrionare. Celulele mici rotunjite pot fi uneori dificil de diferențiat cu limfocitele, neuroblasturile și sarcomul extravehicular al lui Ewing, în special în studiul secțiunilor înghețate. Copiii cu tumori embrionare au cel mai bun prognostic. Varianta botrioidă a rabdomiosarcomului embrionar este observată cu localizare submucoasă.
Apoi, aceste tumori cresc în lumenul organului și arată ca un studiu macroscopic sub formă de mase polipiidice asemănătoare cu ciorchini de struguri. Tumorile botriotice se găsesc în vezică, vagin, uter, nazofaringe și, uneori, în canalul biliar comun și perineal. Tumorile botrioide reprezintă 5 - 6% din totalul rabdomiosarcomilor la copii. Prognoza este foarte favorabilă.
Tumorile nefavorabile din punct de vedere histologic. Formele adverse includ tumorile circulatorii alveolare, anaplastice și monomorfice. Rabdomiosarcomul alveolar reprezintă 20% din toate cazurile de rhabdomyosarcom la copii. Acest tip creste sub forma de fire cu grupuri de celule tumorale rotunde mici cu citoplasma eozinofilica abundenta.
Rabdomioblastele au o bandă transversală (40%) și uneori formează celule gigantice multinucleate sintetice. Cu toate acestea, prezența unei striatii transversale nu este o condiție necesară pentru diagnosticare. La copiii cu tumori cu celule alveolare observat translocatie cromozomiala intre cromozomii 2 si 13. Cea mai frecventă localizare - la nivelul membrelor, trunchiului și zona perianala. Cu toate acestea, tumorile alveolare sunt observate, de asemenea, în zonele caracteristice localizării primare a rabdomiosarcomilor.
Pacienții cu tumori alveolare prezintă cel mai grav prognostic, un procent ridicat de implicare a ganglionilor limfatici regionali, recidive tumorale, leziuni ale măduvei osoase și metastaze îndepărtate. Tipul anaplazic se caracterizează prin prezența unor nuclee hiperchromatice și polimorfe cu cifre bizare mitotice mărită. Tumorile tumorale celulare monomorfe sunt o leziune cu nuclei rotunzi foarte uniformi, cu margini proeminente.
Cu toate tipurile descrise de tumori sunt acum bine cunoscute și nu mai puțin recunoscute, dar în 10-15% din cazuri nu se poate determina exact tipul de celule, pentru ea „vag“. Microscopia electronică, metode imunohistochimice și ADN specific floutsitometriya cercetarea celulare proto-oncogena poate explica originea celulelor tumorale, și astfel să înțeleagă mai bine dependența de supraviețuire de tipul histologic al tumorii.
Radioterapia. Experiența timpurie IRS-I, majoritatea copiilor cu rabdomiosarcom aplicat doza de iradiere de 6000 F, cura a fost atins 85-90% din tumorile locale. Din păcate, rezultate similare au fost însoțite de o incidență inacceptabil de mare a efectelor adverse la distanță, cum ar fi „mikrotaz“ întârzierea creșterii scheletic, leziuni ale sistemului nervos central și dezvoltarea de tumori secundare, de multe ori în zona de iradiere.
Tratamentul ulterior (IRS-II și III) doze mai mici (4000 până la 5500 cGy în funcție de vârstă - mai puțin sau mai mult de 6 ani, doar câțiva pacienți au primit mai putin de 4000 cGy) a condus la o creștere a frecvenței de recurență locale și regionale (mai mult 30% din grupa II și III și 40% în grupa IV), în special în cazul în care dimensiunile tumorii primare au fost semnificative (> 5,0 cm). Excepțiile au fost copii, inclusiv piept, cu înfrângerea din grupa I, în care tumora a fost complet rezecate. Acești pacienți au o rată mare de supraviețuire în tratamentul a doua medicamente chimioterapie (actinomicină D și vincristină), radioterapia nu este necesară.
Cu toate acestea, în cazurile severe (grupele II și IV), radioterapia este o componentă foarte importantă a tratamentului, în special cu o astfel de localizare, care nu permite o rezecție locală extensivă a tumorii. Cu o aplicare adecvată, radioterapia ajută la reducerea frecvenței recăderilor locale în zona tumorii primare. Pacienții au fost tratați prin metoda iradierii hiperfracționale cu o doză de 110 cGy timp de 5 zile pe săptămână, de două ori pe zi (cu un interval între sesiunile de 6-8 ore).
Avantajul teoretic al metodei de hiperfracție este posibilitatea aplicării dozei adecvate (5800 cGy) astfel încât, ca rezultat al tratamentului, tumoarea să fie distrusă, însă țesuturile intacte normale rămân intacte. Scopul unei astfel de tactici este creșterea procentului de vindecare a tumorilor locale și regionale cu 10-15%, reducând în același timp riscul efectelor tardive nedorite asociate cu iradierea.
Unele localizări pot necesita o reducere și mai semnificativă a dozei de radiații (de exemplu, atunci când plămânul este iradiat - 1800 cGy, burtă-3000 cGy). Schimbarea schemei și a dozei de radiație este uneori necesară în cazurile în care se utilizează medicamente chimioterapeutice radio-potetice, cum ar fi actinomicina D și adriamicina.
În tratamentul pacienților cu sarcom de țesuturi moi brahiterapie este uneori folosit cu diferite grade de succes. Aplicație senzori interstițiale (granule sau tije) in vagin, vezica urinara, si alte locuri (de exemplu, mușchi scheletici) asigură o supraviețuire ridicată în unele cazuri, mai ales pentru tumorile foarte mari, cu bun efect local în zona tumorii primare.
Brahiterapia are următoarele avantaje: (1) la o anumită doză de radiații, efectul biologic crește; (2) patul tumoral este vizualizat direct; (3) mai multe oportunități de păstrare a țesuturilor intacte; (4) este posibil să se efectueze o scurtă durată de iradiere și (5) metoda poate fi aplicată ca supliment la iradierile externe convenționale. Principalul dezavantaj al brahiterapiei este o incidență crescută a complicațiilor ranilor.
KU Ashcraft, Т.М. titular