Acizi grași liberi: cheia înțelegerii rezistenței la insulină.
Acizi grași liberi: cheia înțelegerii rezistenței la insulină.
Acizi grași liberi.
Se formează acizi grași liberi (sau nu esterificați) ca urmare a hidrolizei trigliceridelor conținute în țesuturile grase. Acizii grași din plasmă sunt fie esterificați, fie în acest caz legați cel mai mult la albumină sau nu sunt esterificați și sunt într-o stare liberă. Acizii grași liberi (FFA) fac parte din lipoproteinele din clasa a 5-a. Acestea din urmă constau în acizi grași cu lanț lung, puternic asociate cu două zone specifice ale moleculei de albumină; atunci când nivelul FFA din plasmă crește, acestea ocupă zone suplimentare ale acestei molecule, dar legătura în acest caz este mai puțin stabilă. FFA sunt principalul substrat energetic al corpului. Acestea se formează în timpul procesului de lipoliză a trigliceridelor acumulate în celulele țesutului gras. Lipaza tisulară în aceste celule este sub control neuroendocrin, iar activarea sa este prin sistemul de adenilat ciclază. A doua sursă de plasmă FFA este hidroliza trigliceridelor conținute în lipoproteine sub influența lipoproteinelor lipază. Capacitatea mușchilor scheletici (și a altor țesuturi) de a-și ajusta metabolismul la substratul dominant în prezent se numește "sănătate metabolică bună" sau "flexibilitate metabolică". Este clar că buna "sănătate metabolică" este asociată cu sensibilitatea normală la insulină.
Schimbul de acizi grași liberi.
Timpul de înjumătățire al FFA este foarte scurt - de la 4 la 8 minute și se absorb ușor din plasmă de către celulele musculare ale corpului. Al doilea mod al metabolismului lor este absorbția ficatului și resinteza în trigliceride, care apoi pot fi transportate din ficat în VLDL sau oxidate în acetil-CoA. În condiții fiziologice, nivelul FFA din sânge poate crește și scădea foarte repede, satisfăcând nevoia organismului de a forma această formă de energie.
Fiecare minut 20-40% din FFA care intră în plasmă sunt eliminate - ele sunt oxidate, reesterificate sau transformate în alți acizi grași. În timpul odihnei, oxidarea are loc în principal în ficat și în inimă. și cu sarcini - în mușchii scheletici. în ultimul caz, proporția de FFA oxidabil crește de la aproximativ 20 la 60%.
Majoritatea FFA, capturată de celulele hepatice, este reesterificată prin formarea în principal a trigliceridelor. precum și fosfolipidele. pentru sinteza căruia, de regulă, se utilizează acid linoleic. În plasmă concentrațiile FFA se găsesc în intervalul de la 100 pmol / L până la 1 mmol / l și nivelul lor depinde puternic de momentul zilei. După fiecare nivel plasmatic al FFA masă scade, astfel ca insulina inhibă lipoliza în celulele adipoase, care a dus la formarea și FFA. În timpul nopții, concentrația de FFA în plasmă crește. Aceste fluctuații zilnice normale ale nivelurilor de FFA „ajustate“, aproape toate celelalte țesuturi, cum ar fi mușchi scheletici, care „comutator“, cu utilizarea glucozei (după-amiaza), cu privire la consumul de FFA (noaptea).
Unele cauze ale tulburării metabolismului FFA.
O încălcare esențială a schimbului de acizi grași liberi este creșterea lor cronică. Suprimarea cronică a nivelului de FFA poate fi cauzată de o varietate de cauze de tip alimentar și de stres. De exemplu, un exces de carbohidrați, la care sinteza de noi acizi grași începe de la un exces de carbohidrați. Întrucât 75-80% din glucoză este utilizată de o musculatură scheletică la o persoană sănătoasă, activitatea fizică a muncitorilor aflați în muncă grea poate împiedica dezvoltarea rezistenței "funcționale" la insulină. Lipsa activității fizice determină, de asemenea, o creștere a FFA.
FFA este un metabolit și o moleculă de semnal.
Numeroase studii din ultimii ani au arătat că, în primul rând, FFA nu este doar combustibil de înaltă energie, ci și molecule importante de semnalizare. Concentrația lor este un factor important de reglementare care afectează intensitatea utilizării glucozei în mușchi. Și, în al doilea rând, țesutul adipos - este de asemenea important organ endocrin care secretă un număr mare de factori, numit adipocytokines, care au un efect de sensibilizare sau la insulină (ea adiponectina si leptina), în particular, factorul de necroză tumorală - alfa (TNF-alfa) , rezista, etc.
Cu un număr excesiv de țesuturi adipoase, excesul de lipoliză are loc. În mod normal, eliberarea de FFA din țesuturile adipoase este strict reglementată, ceea ce asigură alte țesuturi cu o cantitate echilibrată de FFA, necesară pentru a-și satisface în mod adecvat nevoile energetice. Dar cu obezitate, astfel, cantitățile crescute patologic de molecule de semnalizare (în special, TNF-alfa) ajung în sânge, ceea ce duce la o întrerupere a homeostaziei metabolice. Astfel, primele evenimente care duc la o defalcare a mecanismului de acțiune al insulinei și debutul MI apar în mod specific în celulele adipoase și cu mult înainte de debutul toleranței la glucoză afectată.
Acizi grași liberi: cheia înțelegerii rezistenței la insulină.
Profilul acizilor grași liberi în ser variază în funcție de sex și vârstă, dietă, modificări ale stării hormonale; de exemplu, adrenalectomia sau castrarea duce la o schimbare a profilului LC. O schimbare a concentrației LC libere la rândul său duce la schimbări semnificative în cele două etape ale transferului informațiilor hormonale: legarea glucocorticoizilor la proteinele lor specifice de transport în plasmă și la receptorii de țesut.
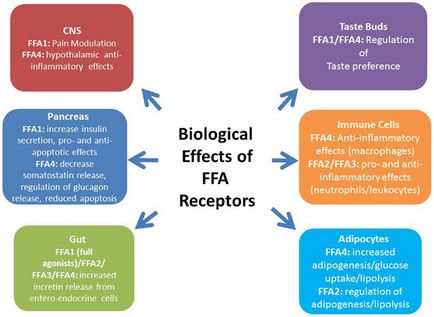
Din pozițiile moderne, acizii grași liberi nu mai sunt considerați substraturi pasive implicate în procesele metabolice. Acizii grași liberi sunt semnale metabolice importante și participanți la tulburările lipidice. Într-o serie de situații, ele se comportă ca molecule asemănătoare hormonilor, influențând transcripția genelor, care se leagă de un număr de receptori. Printre receptorii care se leagă la FFA / FFA sau derivații lor, un loc special este ocupat de receptorii activi ai proliferării peroxizomilor - PPAR. De asemenea, receptorul GPR120 cuplat cu proteina G, care este exprimat în cantități mari în intestin, funcționează ca un receptor pentru FFA acizi grași cu catenă lungă nesaturată. Stimularea GPR120 cu acizi grași liberi promovează secreția de GLP-1 și crește cantitatea de insulină circulantă.
Acizi grași liberi și sănătate.
literatura medicală străină acizi grași liberi (FFA), sau acizi grași ne-esterificați sunt formate prin hidroliza tri-gliceride conținute în țesutul adipos, denumit „lumină roșie pe tabloul de bord al miocardului.“ Creșterea nivelului lor plasmatice semnalează un pericol în creștere: la începutul sindromului metabolic, rezistenta la insulina mai tarziu, cardiomiopatie diabetică, și mai mult - boli coronariene. Mai mult, acest bec poate arde și va izbucni „bulb“ markerilor de necroză miocardică, indicând faptul că „punctul fără întoarcere“ a trecut. Astfel, nivelurile ridicate de FFA sunt direct legate de obezitate, adică "Aceste becuri încep să strălucească cu mult înainte de dezvoltarea punctului final", ceea ce face posibilă efectuarea efectivă a măsurilor corective.
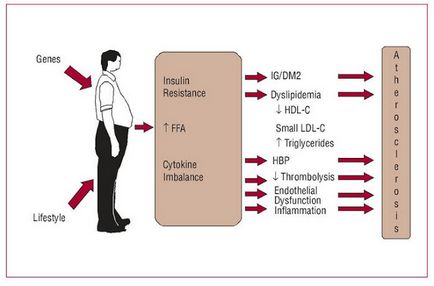
Numeroase studii recente arată în mod clar: niveluri crescute de acizi grași liberi, cauzate de un exces de tesut adipos - în cazul în care nu primul, atunci cel puțin una dintre principalele cauze ale IR. În mod repetat și în mod fiabil arată că majoritatea pacienților obezi, sindrom metabolic si diabetul de al doilea tip (tip 2), au niveluri crescute de FFA, ceea ce duce la multe TS tesuturi - adipos, mușchi, ficat și celulele endoteliale.
FFA - predictor independent al toleranței la glucoză și diabet 2. Astfel, fluxul crescut de acizi grași liberi din masa mare de celule adipoase, precum și tulburările în mecanismele de stocare a trigliceridelor și a mecanismelor de lipoliză în țesuturi, inițial în mod normal sensibile la insulina - aceasta pare a fi cel mai devreme manifestări ale anomaliilor care conduc la IR. În principiu, aceste încălcări sunt detectate înainte de debutul hiperglicemie postprandiale, sau la dezvoltarea hiperglicemiei de post. Într-adevăr, o creștere a nivelurilor plasmei postpauzice de FFA, poate cea mai veche indicație a unei viitoare încălcări a toleranței la glucoză.
Cum de a inversa acest proces?
Te descurci bine. Cu articolul dvs. m-ai salvat!
Taki îi place neclar. Mulțumesc.
Nu este clar în întregime numai momentul afinității receptorilor adipozi și musculari pentru insulină în obezitate și rezistența dezvoltată. Care receptor este mai probabil să fie atașat la insulină cu glucoză.