Adâncimea absolută a apariției nivelului apei subterane, măsurată în puțurile situate pe orice teritoriu, poate fi diferită. există această mărturie că masa de apă este complicată, caracterul, determinarea stratului impermeabil relief, modificați capacitatea de filtrare a rocilor în acest domeniu, condițiile de aprovizionare, cuplate cu supra-nostnymi rezervoare și râuri, activitatea umană și de alți factori.
Pentru a determina natura suprafeței apei freatice, în funcție de măsurare o singură dată a nivelurilor absolute ale markerilor în puțuri și tranșee, cartele construite și r și q-r și s o d și n c (fig. 144). Hydronzohypses sunt linii care conectează punctele cu semne absolute egale ale mesei de apă subterană. Poziția pe hartă a punctelor corespunzătoare hidroizogipelor corespunzătoare se găsește prin interpolare liniară simplă. Harta isohyps vă permite să rezolvați următoarele sarcini:
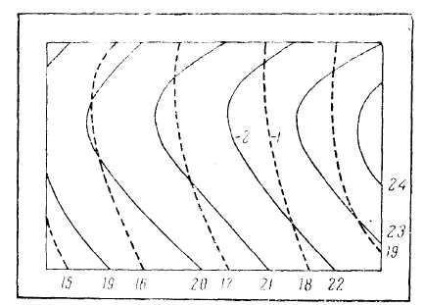
Fig. 144. Harta hidrosizuctilului sau a apei subterane:
1. Găsiți cele mai favorabile în relația hidrogeologică a amplasării structurilor sau a carierelor-
șanț cu apă. În acest scop, sunt selectate situri cu o masă de apă subterană.
2. Stabiliți direcția și panta debitului apei subterane în orice parte a suprafeței hărții. direcție
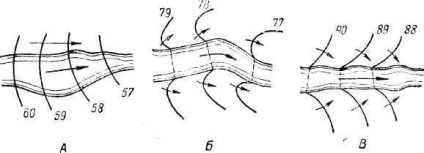
Fig. 145. Poziția hidroizogipsului la diferite rapoarte
apele subterane cu un râu. L - conexiune cu. râul este absent; B - râu
hrănește apele subterane; B - boii de pământ alimentează râul
fluxul în orice punct va fi definit ca o perpendiculare la hidropogipsie, îndreptată spre semne mai mici.
3. Pentru a determina raportul dintre apa subterană și corpurile de apă de suprafață și râurile (Figura 145).
Proprietățile fizico-chimice ale formării apei.
Compoziția apelor subterane include diverse săruri dizolvate, precum și componente gazoase. Au fost detectate peste 45 de elemente găsite în soluții sub formă de ioni diferiți. Cele mai importante sunt anionii Cl, SC> 4 2
și cationii Na +, K +. Ca 2+. Mg2 +. H +. Dintre gazele dizolvate în compoziția apelor subterane se întâlnesc cel mai adesea oxigen, dioxid de carbon și hidrogen.
Este acești ioni determină multe dintre proprietățile de apă, printre care cele mai importante sunt duritatea, alcalinitatea, salinitatea, agresivitate față de diferite materiale de construcții.
Mineralizarea și compoziția chimică determină toate proprietățile fizico-chimice de bază ale apelor.
Proprietățile fizico-chimice ale apei de formare sunt următoarele:
Densitatea formării apei: рв = 1,0 - 1,5 x 10 3 kg / m 3
3. Extinderea termică a apei de formare: αβ = (1,8 - 9) * 10-4 * C-1.
Compresibilitatea apei de formare: β = (2 - 5) * 10 -10 Pa -1.
Solubilitatea în apă în formarea apei: av = 1 - 5 m 3 / m 3.
Coeficientul volumic de formare a apei: bβ = 0,8 - 1,2.
Conductivitatea apei formării (depinde de salinitate și compoziția de sare de litiu): Rezistivitatea σ = 0,05 - 1,00 Ohm * m.
În hidrogeologia petrolului, conținutul de săruri în apă este împărțit în 4 clase: în stare proaspătă - până la 1 g / l; brânci - 1 - 10 g / l; Sare - până la 10 - 35 g / l; saramuri - mai mult de 35 - 500 g / l
Clasificarea chimică a apei de formare
Clasificările apelor naturale sunt foarte numeroase, dar foarte puține s-au răspândit. Cele mai multe clasificări se bazează pe compoziția de sare ionică și unele pe compoziția gazului. De la un număr apropiat de fiecare alte clasificări, care se bazează pe dominația cantitativă a diferitelor componente ionice-TION, întruchiparea cel mai convenabil și simplu LI Tolstikhina. Clasificarea distinge clasa de apă de anionul predominant și subclasa de cationul predominant (Tabelul 6).
Dezavantajul clasificării lui Tolstihin este lipsa unor clase și subclase de caracter mixt, care se găsesc adesea în natură.
În practica comercială, clasificarea VA Sulina este foarte folosită. Etichetarea apelor naturale sunt împărțite în patru tipuri în funcție de relația caracteristică dintre ionii de conducere (Tabel. 7) și apoi în grupe și subgrupe pe baza prevalenței diferitelor anioni și cationi. Astfel, conform clasificării, există și cloruri.
sulfat și hidrocarbonat. Numărul total de grupuri
este egal cu 12, dar în natură unele dintre ele nu apar.
Tabelul 6 Exemple de ape conform clasificării LI Tolstihin