Elementele de bază ale teoriei de frigere oxidativă a concentratelor de cupru
Ulterior, procesul trece în regimul de difuzie, viteza procesului fiind determinată în totalitate de rata de difuzie
În funcție de condițiile de transfer de temperatură și de căldură, poate apărea o anumită perioadă de oxidare în regiunea intermediară.
3. Condiții de punere în aplicare a diverselor moduri în primă aproximație poate fi judecat de cantitatea de energie de activare de oxidare sulfurat. Calculele arată că oxidarea sulfurilor cu eliberarea dioxidului de sulf caracterizat prin aceea regiune cinematic o energie de activare de 35 000-45 000 cal / mol, intermediar - 10000-25 000 cal / mol, difuzie - 3,000 la 8,000 cal / mol
Modul de bază al oxidării în timpul arderii este difuzia. Studiul mecanismului de oxidare a sulfurilor folosind metode moderne de cercetare, precum și datele privind mecanismul de oxidare dă motive să se presupună că procesul de oxidare începe cu adsorbția oxigenului pe suprafața sulfurii. Sub influența câmpului de forță al unui corp solid, molecula de oxigen se deformează sau disociază în atomi, rezultând oxigenul devenind mai activ. Interacționând cu atomii stratului de suprafață, el formează complexe instabile constând din metal, sulf și oxigen (MeSO, MeS02). Aceste complexe disociază cu formarea de oxid metalic.
Saturarea sulfurii cu oxigen adsorbit la sulfat "complet" este posibilă numai dacă acest proces are loc la temperaturi sub temperatura inițială de reacție a sulfurii inițiale cu sulfatul rezultat:
MeS + 3 MeS04 = 4MeO + 4S02.
Un exemplu de formare a sulfatilor stabili pe suprafata sulfurii poate fi procesele care apar in natura.
S-a desorbit sulful oxidat din disocierea sulfatilor metastabili. Procesul poate fi reprezentat prin următoarea schemă:
MeS + O2 ⇔ MeSO2;
MeS02 ⇔ MeO + SO.
Monoxidul de sulf este cunoscut ca un compus instabil și, în prezența oxigenului, este oxidat la anhidrida sulfuroasă
2S0 + O2 ⇔ 2SO2.
Anhidrida anhidră în anumite condiții termodinamice este oxidată la anhidrida sulfurică
2SO2 + O2 ⇔ 2SO3,
Constanta de echilibru a reacției de disociere a anhidridei sulfuroase este prezentată în Tabelul. 4.
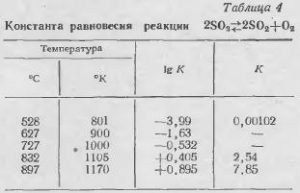
Anhidrida anhidră în contact cu MeO formează sulfat
MeO + SO3 ⇔ MeSO4
Reacția totală de ardere oxidativă poate fi scrisă sub forma următoarei ecuații
MeS + 1,5O2 = MeO + S02,
Astfel, produsul principal de oxidare a sulfurii în timpul procesului de oxidare - MeO, prin arderea sulfatizării în cuptor, trebuie să fie create condiții pentru a asigura formarea anhidridei sulfura. sulfați de metal pot fi preparate în cantități suficiente, în acele cazuri în care faza gazoasă va pSO3 o elasticitate mai mare echilibru presiune de disociere a sulfaților amestec de gaz (SO3, SO2, O2) sunt date pentru diferite sulfații în tabel. 5.
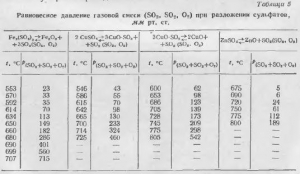
Rezultatul final al interacțiunii oxigenului cu sulfura poate fi judecat din magnitudinea modificării potențialului de reacție izobaric. Comparația valorilor calculate face posibilă determinarea direcției de reacție.
dependență Z și log K privind temperatura pentru reacțiile de oxidare finală sunt prezentate în tabelele 6, 7.
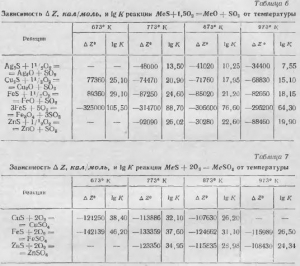
Chimia de oxidare a sulfurilor bazice
Pyrite FeS2. Când este încălzit într-un cuptor de calcinare, pirita disociază cu eliminarea sulfului elementar prin reacție
O parte din pirită sub acțiunea oxigenului din faza gazoasă este supusă oxidării directe
Fierul sulfuros, în funcție de cantitatea de oxigen din faza gazoasă, se oxidează la oxid de fier sau magnetit prin reacție
Pirita aparține numărului de sulfuri ușor oxidate, atunci când se încălzește decripta. Produsele de oxidare sunt Fe2O3, Fe3O4 și parțial Fe2 (SO4) 3,
Sulfurile de cupru Cu2S, CuS, CuFeS2. Sulfura de cupru inferioară este oxidată în funcție de reacțiile cu temperatura
Sulfurile de cupru mai mari, când sunt încălzite într-o atmosferă oxidantă, sunt oxidate fie direct, fie printr-o etapă de disociere:
Cea mai scăzută sulfură de cupru este unul dintre cele mai stabile sulfuri în timpul prăjirii și este semnificativ mai puțin expus la oxigenul din faza gazoasă. Sulfura de cupru mai mare disociază la temperaturi relativ scăzute. Calcopirită nu disociază complet și o mare parte din acesta rămâne în produsul prăjit nemodificat (50%) din produsul de oxidare a sulfurii de cupru este CuO, CUSO4, CuO * CuSO4.
Sulfura de zinc ZnS. Sulfura de zinc aparține tipului de sulfuri dificil de oxidare. În condițiile cuptorului de calcinare, se oxidează la sulfat de zinc și oxid prin reacții
Sulfatul de zinc al formării primare sau secundare sub încălzire trece în sulfatul bazic prin reacție
Sulfatul de bază este mai stabil și rămâne până la 800 °.
Astfel, produsele de oxidare a sulfurii de zinc sunt ZnO, ZnS04 și 3ZnO * 2S03.
Sulfură de plumb PbS. În oxidarea sulfurii de plumb, ca și în oxidarea sulfurii de zinc, se poate forma sulfat de plumb și oxid de plumb în funcție de temperatură;
Un plumb metalic poate întâmpla ca rezultat al interacțiunii cu sulfatul de sulfură de plumb și oxid, deoarece presiunea de echilibru PSO2 la temperaturi de calcinare este de 1 atm, dar datorită unei atmosfere oxidante în întregul cuptor se va transforma în oxid de plumb metalic. În consecință, produsele de oxidare sunt PbO și PbS04.
Sulfura de argint Ag2S este oxidată prin reacție
Cu încălzire lentă, este posibilă formarea de sulfat de argint:
Spre deosebire de oxid, sulfatul de argint este stabil până la 900 °. Prin urmare, produsul oxidării sulfurii de argint este argintul metalic.
Interacțiunea dintre compușii din diferite metale. În procesele de oxidare, împreună cu reacțiile de interacțiune a sulfurilor cu oxigenul din faza gazoasă, un rol important aparține reacțiilor de reacție a produselor de oxidare cu sulfurile inițiale sau produsele de disociere a acestora. Dintre astfel de interacțiuni, reacțiile dintre sulfuri și oxizi de fier mai mari ar trebui atribuite mai întâi.
Practica de oxidare
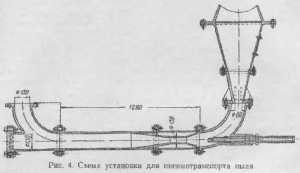
Principalul dezavantaj al proiectării cuptoarelor multi-core este un mecanism complex de supraîncălzire (opriri frecvente ale cuptorului datorită ruperii curbelor, mânerelor și, uneori, arborelui central). Practica pe termen lung a muncii, precum și studiile special concepute au permis extinderea într-o oarecare măsură a duratei de viață a mecanismului de supraîncălzire. Mânerele sunt în prezent fabricate din compoziție superaliaje: 28-30% Cr, nu mai mult de 2% Ni, 0,12-0,2% Mn, 0,5-1,7% Si, 1,542% C, restul fier, accident vascular cerebral Chugal de aluminiu (fontă conținând 9-13% aluminiu). Grosimea pereților brațelor este mărită în partea capului.
De asemenea, un dezavantaj semnificativ al cuptoarelor este prăbușirea prematură a păstăi, în special a celor paralele. Adesea, până la sfârșitul campaniei, cuptorul cu mai multe nuclee este transformat într-un cuptor suspendat. În scopul prelungirea duratei de viață a vetre chiar recomandat așezându-le pe chit refractar pentru a efectua următoarea compoziție: silicofluorură de sodiu 3%, 97% șamotă zdrobit, în stare păstoasă sticlă solubilă. Aplicarea sa la topitoria de cupru Krasnouralsk a făcut posibilă extinderea duratei de viață a păstăilor cu număr egal cu doi.
Trebuie remarcat faptul că utilizarea cărămizilor din cupru pentru căptușeala la nivelul actual al tehnologiei ar trebui considerată nerentabilă. 176 l de cărămizi de 26 de grade diferite sunt consumate pe căptușeala unui cuptor cu zece căi. Industria refractară este capabilă să producă beton care poate rezista la temperaturi de până la 1000 ° C. Trecerea la beton rezistent la căldură va permite prelungirea campaniei cuptorului și scurtarea perioadei de reparații.
Performanța cuptoarelor este prezentată în tabelul. 8.
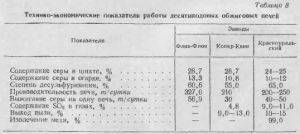
Compoziția pulberii și a prafului este prezentată în tabelul. 9
Pentru gestionarea corectă a procesului necesită chimic monitorizare constantă și compoziția metalurgică a încărcăturii, gradul de măcinare calcine compoziție, vid în distribuția temperaturii cuptorului depune o temperatură a aerului care iese din centrală a arborelui, cantitatea și elasticitatea aerului suflat în puț. În acest scop, cuptorul este echipat cu dispozitive de indicare și înregistrare.
Arderea concentratelor de cupru în patul fluidizat
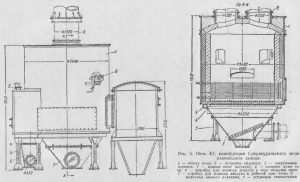
Vederea generală a cuptorului este prezentată în Fig. 5.
Carcasa cuptorului este realizată din tablă de oțel cu o grosime de 10 mm. Cadru cuptor simțind în principal, bolta de împingere, este o structură a grinzilor I-secțiune, fixată la partea inferioară a unei tije de fundație și cuiburi în partea superioară a distanțierului pentru a distribui uniform forțele pe șasiu.
Stratul refractar este realizat din beton rezistent la căldură cu un strat termoizolant de următoarele dimensiuni, mm:
În pereții laterali ai cuptorului există patru ferestre pentru instalarea căminelor. Gazele din cuptor sunt deviate printr-o conductă de ramificație din fontă într-o coloană verticală, căptușită cu un strat de căldură rezistent la căldură în interior. Partea inferioară a cuptorului este o placă solidă din beton armat, rezistent la căldură cu capete de aerare, așezată pe o foaie perforată de 14 mm grosime. Mai jos, sub aer sunt cutii de aer, în care este furnizat aer. Praful prins în cicloane, împreună cu cimentul, continuă să se transforme într-un cuptor care reflectă.