Alcaloizi de quinolin. conțin în moleculă restul de chinolină sau a unora dintre derivații săi. Includeți mai mult de 300 de reprezentanți. Izolată din plante 14 familii, precum și unele microorganisme și animale. Naib. ele sunt plante bogate din familia rutaceae (Rutaceae), mauve (Rubiaceae), paranoide (Zygophyliaceae) și compozite (Compositae).
Distingeți următoarea. Principalele alcaloizii de chinolină: 1) sunt chinoline simple (generale F-la I; R = H, OCH3 R '= alchil, arii), 4-chinolonele (II; R = H, CH3 R.' = H, alchil, arii. ) și 2-chinolone (III ;. R = H, CH3, R „= H, alchil, alchenil); 2) hemitepenoid și terpenoid triciclic. derivați de tip IV-X; B) furanohinoliny pentru a-ochi includ, în special, derivați diktamnina (XI; R = OCH3) și comp. tip XII; 4) alcaloizi dimerici, de exemplu. XIII. Alcaloizii cu quinolină sunt, de asemenea, uneori menționați ca un compus. altele decât cele care conțin chinoclidină chinolină reziduuri (în special, chinină), carbolină (ca în XIV), etc.; dar mai des sunt izolate într-o clasă separată de alcaloizi, specifice plantelor de anumite genuri, cinchona (Cinchona), nitrat (Nitraria).
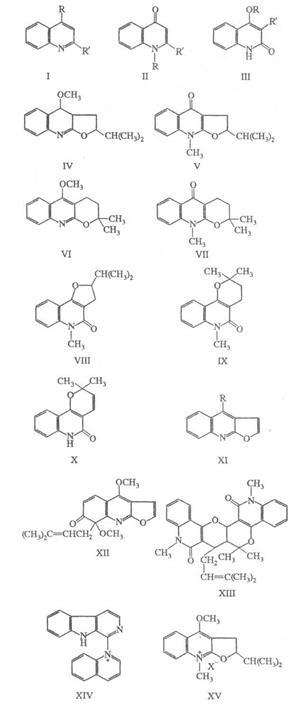
Fiecare grup de alcaloizi are proprietăți chimice caracteristice. și proprietăți spectrale. General Rel. L.A. conținând în pozițiile 2 sau 4 o grupare metoxi: a) capacitatea de a se izomeriza cu sarcina. cu CH3I în N-metil-2 (sau 4) -chinolone (de exemplu, IV este izomerizat în V, VI în VII); b) ușurința de hidroliză (dementație) într-un mediu alcalin sau acid, de exemplu. XI (R = OCH3) XI (R = OH). Natural și sintetic. Alcaloizii cuaternari de chinolină sunt precipitați sau încălziți cu piridină anhidră și transformați în bazele terțiare corespunzătoare, Compusul XV din IV.
2-chinolone, de ex. 4-metoxi-3-prenil-2-chinolonă [III; R = CH3. R '= CH2CH = C (CH3) 2] cu sarcină. cu conc. HCI sau HBr în CH3 COOH rece cu gheață formează alcaloizi chinoline triciclice de tip VII și IX.
Tipice p-TION Alcaloizi furanohinolinovyh (XI) -gidrogenoliz inel furan, pentru a forma un derivat W-etil-2-chinolonei (III; R = CH3 R „= C2 H5.).
Metodele spectrale sunt utilizate pentru a studia structura alcaloizilor chinolinei. Prin valoarea maximelor de absorbție în spectrele UV și UV și prin natura deplasării lor, în funcție de pH-ul mediului, se disting nu numai grupele de alcaloizi chinoline, ci și pozițiile substituenților. Spectrometria Mace face posibilă stabilirea apartenenței unui alcaloid la un anumit grup și diferențierea unor astfel de izomeri apropiați ca V și VII; VIII și IX. 2- și 4-chinolonele, precum și compușii izomerici V și VIII, VII și IX, se pot distinge de poziția și intensitatea integrală a benzii de absorbție în regiunea 1610-1665 cm-1 a spectrului IR. În cele mai multe cazuri, structura completă a alcaloizilor de chinolină poate fi judecată din spectrele RMN 1H și 13C RMN.
Alcaloizii chinolinei diferiți au proprietăți biogenetice diferite. predecesorii. Deoarece biosinteza chinină și derivați ai kynurenic la tine (I; R = OH, R „= COOH) este de la triptofan și alcaloizii de chinolină familia Rutaceae (comp. I-XIII, XV) - din acidul antranilic.
Alcaloizii cu chinolină au o gamă largă de proprietăți fiziologice. activitate. Majoritatea alcaloizilor au un efect calmant asupra centrului. sistemul nervos: unele dintre ele, de exemplu. flindersin (X), arată anti-fidant sv-va. În medicină, chinina și echinopsina (II, R = CH3, R '= H) sunt utilizați ca stimulent central. și periferice. sistemul nervos.
Chinina (C20 H24 N2 O2) - alcaloidul principal de scoarță de cinchona cu un gust amar puternic posedând proprietăți antipiretice și analgezice precum și o acțiune pronunțată împotriva paraziții malariei. Aceasta a permis o lungă perioadă de timp utilizarea chininei ca tratament principal pentru malarie. Astăzi, utilizate în acest scop, droguri sintetice mai eficiente, dar din diferite motive chinina își găsește aplicarea în prezent.
Chinina este un alcaloid conținut în scoarța diferitelor specii de cinchona. În această coajă, pe lângă chinină, chinidina, cinchonina, cinchonidina și un număr de alcaloizi sunt conținute. Structura moleculei de chinină include inele de chinolină și chinuclidină, legate de un grup de atomi - CH-OH. Quinina este un izomer al chinidinei. În practica medicală se utilizează clorhidrat, diclorhidrat și chinină sulfat. Baza chininei este dizolvată în alcool etilic (1: 1), cloroform (1,3), dietil eter saturat cu apă (1: 4), ușor solubil în apă. Clorhidratul de chinină se dizolvă în alcool etilic (1: 1), cloroform (1: 2), apă (1,23), ușor solubil în eter dietilic. Sulfat de chinină solubil în alcool etilic (1: 95), ușor solubil în apă (1,810), dietil eter și cloroform.
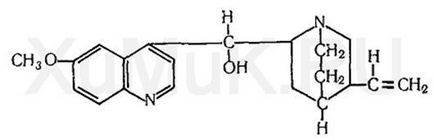
Chinina este extrasă cu solvenți organici din soluții apoase alcaline. Cantitățile maxime de chinină sunt extrase cu cloroform la pH = 10.
Aplicație. Acțiune pe corp. În funcție de doza acceptată de chinină, poate provoca depresie centrală a sistemului nervos, cefalee, amețeli, tulburări de vedere. Quinina excită musculatura uterului și crește contracția acestuia. De asemenea, cauzează o reducere a splinei. Quinina acționează asupra agentului patogen al malariei și este unul dintre medicamentele antimalarice eficiente. Este folosit pentru aritmii. Quinina este folosită în practica obstetrică pentru a stimula și întări activitatea muncii. În cazul unui supradozaj al porcului utilizat de femeile însărcinate, se poate produce avort.
Metabolism. În organism, chinina este metabolizată prin oxidarea ciclurilor chinolină și chinuclidinei. În acest caz se formează 2-hidroxichinină, 2'-oxichinină, dioxochinină. În timpul metabolizării, grupa vinilică din molecula chinină poate fi oxidată pentru a forma chinină. De asemenea, ciclul chinuclidinei poate fi oxidat pentru a forma acid hemocinic (acid 6-metoxi-chinolin-4-cetocarboxilic). Metaboliții și o mică parte din chinina nelegată sunt excretați din organism cu urină.
Test preliminar pentru prezența chininei în urină. Se adaugă 2 ml de urină în pâlnia de separare, care este bazificată cu soluție de amoniac, apoi se adaugă 4 ml de cloroform și se agită timp de 5 minute. Din faza apoasă se separă un strat de solvent organic, care se agită cu 3 ml de soluție de acid sulfuric 10%. Fluorescența albastră a fazei apoase indică prezența chininei în urină. Fluorescența devine mai pronunțată dacă extractul apos acid este iradiat cu lumină UV.
Detectarea chininei prin fluorescență. Soluțiile de quinină acidulate cu acid sulfuric au o fluorescență albastră. În prezența ionoclorului și a altor ioni în soluții, fluorescența chininei este slăbită.
Fluorescența chininei ca bază dibazică depinde de pH-ul mediului. În mediul acid, chinina are o fluorescență albastră. Într-un mediu alcalin (pH
9) chinina are o fluorescență purpurie. Produsele de oxidare cu chinină au o fluorescență galben-verde.
Executarea experienței. Soluția de testat este turnată într-un vas de porțelan și evaporată până la uscare. La un reziduu uscat se adaugă 4-5 ml de soluție de hidroxid de sodiu 0,1 N. soluție de acid sulfuric. Soluția rezultată este transferată într-un tub, care este iradiat cu raze UV. În prezența chininei, apare o fluorescență albastră a soluției. Din adăugarea a câteva picături de 0,1 N la acest lichid. soluție de hidroxid de sodiu, intensitatea fluorescenței albastre este slăbită și apoi (la pH
9) apare fluorescența violetă.
Dacă o soluție de chinină, se acidulează cu acid sulfuric, se adaugă câteva picături de apă de brom, diluat volum de zece ori mai mare de apă (pentru a finaliza stingerea fluorescenței), apoi se adaugă câteva picături de soluție 25% de amoniac până la bază, atunci apare fluorescenta galben-verde.
Reacția Talejohin. Din adăugarea de apă bromică în chinină și apoi în amoniac se formează un tacheochin verde, care se extrage cu cloroform:
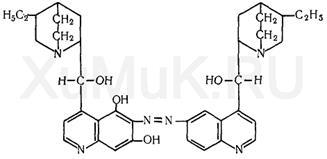
Realizarea reacției. Soluția substanței de testat se evaporă până la uscare. La reziduul uscat se adaugă 1 ml de apă. La soluția rezultată se adaugă, prin picurare, apă de brom (evitând excesul) până la o culoare ușor gălbuie. Din adăugarea a câteva picături de soluție de amoniac în soluția ușor gălbui, apare o culoare verde strălucitoare, care devine albastră atunci când reacția este neutră și devine roșie sau violet când se adaugă acidul. Când lichidul, care are o culoare verde, este agitat cu cloroform, acesta din urmă are o culoare verde.
Reproductibilitatea reacției este influențată de concentrația substanței de testat, de volumul de reactivi adăugați etc. Reacțiile interferează cu amidopirina, antipirina, cafeina,
Reacția eritrocinei. Câteva picături din soluția de testat se evaporă la sec, 1 ml de apă, acid sulfuric iliuksusnoy slab acidulată, picătură de apă brom și o picătură de soluție 10% de hexacianoferat (III) de potasiu. Lichidul rezultat este agitat bine, apoi amoniacul este adăugat în picătură până când are loc o reacție alcalină. În prezența chininei în soluția de testat apare roz sau roșu-violet culoare, care, când este agitată cu cloroform în veniturile din stratul de cloroform.
Detectarea chininei prin cromatografie. Pentru a detecta chinina, se utilizează o metodă de cromatografie într-un strat subțire de silicagel. În acest scop, se utilizează aceeași procedură ca și pentru detectarea morfinei (vezi capitolul V, § 34).
Petele cviniene de pe cromatogramă au o culoare maro-roz (Rf = 0,39 ± 0,01).