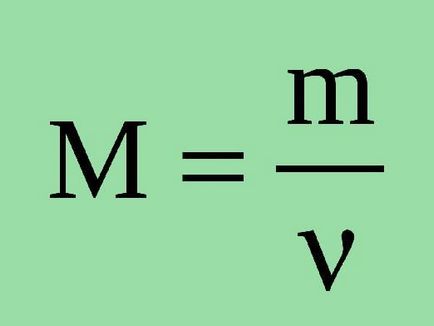
În chimie, nu se poate face fără masa de substanțe. Este unul dintre cei mai importanți parametri ai unui element chimic. Pentru a afla cum de a găsi o mulțime de materiale în diferite moduri, vă vom spune în acest articol.
În primul rând, trebuie să găsiți elementul dorit utilizând tabelul periodic, care pot fi descărcate de pe Internet sau achiziționat. numere fractionare sub semnul elementului - este greutatea sa atomică. Acesta trebuie să fie multiplicat cu indicele. Indicele indică, de asemenea, cât de multe elemente molecule conținute într-o anumită substanță.
- Când aveți o substanță complexă, este necesar să se înmulțește greutatea atomică a fiecărui element al substanței pe indexul său. Acum, se adaugă în sus greutățile atomice obținute de tine. O astfel de masă se măsoară în unități de grame / mol (g / mol). Cum de a găsi masa molară a substanței, vom arăta exemplul de calcul al greutății moleculare a acidului sulfuric și apă:
H2SO4 = (H) * 2 + (S) + (O) 4 * = 2 + 1 * 32 + 16 * 4 = 98g / mol;
H2O = (H) * 2 + (O) = 1 + 16 * 2 = 18g / mol.
masa molara de substanțe simple, care constau dintr-un singur element, am calculat tăinui în același mod.
Atunci când, de exemplu, cunoașteți volumul, presiunea, masa și temperatura în grade Kelvin (dacă este C apoi tradus), învață cum să găsească substanțele cu greutate moleculară pot, folosind ecuația lui Mendeleev-Clapeyron:
unde R - este universal postoyannaya- gaz M - este o (masa molară) molecular, amu
unde n - este numărul veschestva- m - este masa substanței. Aici este necesar pentru a exprima cantitatea de substanță utilizând cantitatea (n = V / VM) sau numărul Avogadro (n = N / NA).
M = P1 * Ek * (1000 / P2 * tk),
unde P1 - este greutatea solut, r P2 - este greutatea solventului, r Ek - această constantă cryoscopic a solventului, care poate fi găsit în tabelul corespunzător. Aceasta constanta este diferit pentru diferite tk zhidkostey- - această diferență de temperatură, așa cum este măsurată cu ajutorul unui termometru.
Acum știi cum să găsească o mulțime de materiale, fie că este vorba de simplu sau complex, în orice stare de agregare.