reacție nucleofilă. geterolitich. p-TION org. Conn. cu un nucleofil. agenți (nucleofile, din lat. nucleu-nucleu și greacă. phileo-like). K și y k l e de f și n și m includ molecule și anioni (Org. Și săruri anorganice.), La- participarea la p-TION este dată perechea sa de electroni la formarea noii legături. Caracteristica comună a reacțiilor nucleofilică, atac nucleofil de un centre de electroni cu deficit, culminând adăugarea de reactiv sau substituția unei grupări fugace, de exemplu. nucleofil. substituție la sat. atomi de carbon sau aromatic. nucleofil inel. atașare la gruparea carbonil sau alchene și alchine. nucleofil. substituție la atomul de carbon carbonil. nucleofil. substituție la atomul de fosfor.
Naib. a studiat p-TION și y k l e de f. s o m e d e n s y n a s a u. și m m o y l z e d p o și:
P-TION de acest tip este, în general, de asemenea, utilizat pentru calitate. și cantități. definiții care caracterizează reacția nucleofilă.
În aceste p-tiile nucleofili furnizând o Org X. particulă. perechea de electroni substrat. Pentru ieșire cu perechea sa de electroni Z titluri acceptate. y n k l e o p y g (lat. nucleu-core și-fugio fugă). Rata și mecanismul de nucleofil p-TION. înlocuire determinarea influenței nucleofil. reacție. capacitatea (sau nucleofil NOSTA „rezistență nucleofil“) reactiv X. rsakts nucleofugică. capacitatea (sau nucleofugică) natura grupului substrat Z. fugace și condițiile de p-TION (temp, p-ERATOR, presiune și așa mai departe. d.). Nucleofilicitatea, spre deosebire de o valoare bazicitate este cinetică, mai degrabă decât termodinamică, t. E. Suma. măsura nucleofil. reacție. Capacitatea este constanta de viteză pentru p-TION, nu constanta de echilibru.
Există două cazuri de limitare p-tiile nucleofili. înlocuire-Monopoli. proces SN 1 și bimolecuă (simultan) SN 2:

Mecanismul nucleofil. substituție depinde în principal de natura substratului și p-ERATOR. Astfel, SN 1 procese implementate în polar p-celeration (H2O, CH3OH, AcOH și colab.), Contribuind heterolysis C-Z și p-tiile substraturi. care conține terțiar, alilic sau ben atom zilny S. SN proces 2 mai puțin dependentă de p-ERATOR și Naib. caracteristic substraturilor cu atomul C primar
Când Monopoli. proces original, sub acțiunea ionizare p-ERATOR apare substrat pentru a forma trehkoordinats. carbocationului și nucleofug (această etapă determină în mod obișnuit viteza întregului proces), urmată de rapidă etapă de cuplare carbocationului cu un nucleofil. În acest caz, atacul nucleofilul la fel de probabile pe ambele părți, iar în cazul asimetric. reacție. centrul se observă de obicei, formarea racematului. Când Bimol. pyatikoordinats proces format. stare de tranziție, în care atacul nucleofil este realizată pe partea opusă a substituentului outgoing ceea ce conduce la o configurație de tratament, de exemplu. t. sunat. Walden inversiune (vezi. Stereochimie dinamic).
P-TION SN l are de obicei o ordine totala 1; viteza, de regulă, nu depinde de natura nucleofil și concentrația. dar mult depinde de nucleofug natura și p-ERATOR. Cinetica p-TION SN 2 descrie ur-niem ordinul 2 - primul substrat și pe primul nucleofilul. Viteza P-TION în acest caz depinde de concentrație. și de substanța chimică. natura nucleofil.
Este cunoscut de mai multe. se apropie de cantități. Evaluarea nucleofil. reacție. capacitatea de reactiv X: Pe baza corelației. Raporturile SN în 2- și procesele SN-1. Pentru p-tiile SN 2 în apă sau metanol Naib. ur folosit pe scară largă de Sven-Scott lg (k / k0) = S. n, unde k și k0 sunt constante de viteză p-TION resp substrat. cu nucleofil și apă. Sensibilitatea parametru S la modificările nucleofil substrat (S = 1 pentru standard CH3 substrat Br) și reactiv parametrul nucleofilicitate (Tabelul 1)..
VALOAREA Tabl.1.-PARAMETRILOR PENTRU nucleofil n unii reactivi (apă. 25 ° C)
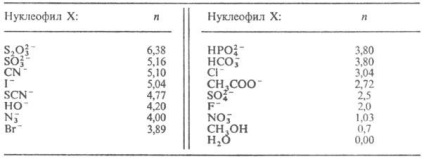
Pentru procesele de tip SN l corelațiile valide. ur-set lg Ritchie (k / k0) = N +. Acesta a fost obținut prin măsurarea vitezelor de p-tiile utilizând ca substraturi karbkatio nou stabilizate arilnymi trei substituenți fenilmetanovogo serie.
Parametrul nucleofilicitate N + a răspunsului. Capacitatea nucleofil în special p-ERATOR; apă în cantități similare N + n parametri.
Parametrii Valorile nucleofilicitate pot varia considerabil în funcție de reacția nucleofil. dar tendința generală a nucleofilicitatea este de obicei stocat. Astfel, aproape toate reacțiile nucleofile ale OH -. CN -. RS -. I - și Br - manifest înșiși nucleofili puternici și H2O, CH3 OH, F -. NO - 3. SO4 2- -ca slab.
Măsura nucleofugică poate servi solvoliză constanta vitezei (care curge prin SN 1 mecanism) substraturi similare. care diferă numai în natura grupării labile (tabelul. 2).

Prin „bun“ nucleofug includ org. sulfonat (Tosi-lat, mesilat, triflat), ftorsulfat- (FSO - 3) și anionul perclorat (ClO - 4). Covalent org. derivați ai acestor anioni sunt larg utilizate ca reactivi de alchilare substraturi extrem de activi în reacții nucleofile. Chiar mai bine nucleofugică particule de azot alkildiazonievyh sare (RN + 2), trivalent iod (grup de ex. ISl2), apa din protonate. alcool și eter de săruri trialkilokso și magneziu; Cu toate acestea alifatich. substraturi. care cuprinde în structura lor aceste grupuri, la sala T-D este de obicei instabil și sunt utilizate numai ca intermediari activi. generată direct în reacție. mediu.
Există mai multe. decembrie abordări teoretice. interpretarea conceptelor și nucleofugă nucleofilicitate și evaluarea factorilor care afectează valoarea lor. DOS. Factori - de bază (aciditate), polarizabilitatea. solvatare. efecte, cantitatea de potențiale de ionizare și oxidare. sterich. și electrostatic. efecte, prezența GRATUIT. perechi de electroni un atom. adiacent nucleofil. centrul de rezistența legăturii cu atomul de carbon. Trebuie remarcat faptul că nici o corelație directă cu SUCCESIUNEA nucleofilicitate unul dintre acești parametri nu este, de obicei, deoarece nu există nici o corelație între nucleofilicitate și nucleofugică; de ex. anion tiolat este RS - nucleofil bun, dar o bază slabă și un grup „rau“ labilă, hidroxid de anioni NO - bază -bune și nucleofil, dar grupul Părăsirea săraci. Anionii la cel mai puternic-t-percloric și trifluorometansulfonic - bun nucleofil Gl, și, în același timp, în măsură să demonstreze proprietatea nucleofil.
Nucleofil. substituție în alifatich. o serie de extrem de important pentru org. sinteză, permițând intenționat înlocuită cu o funcție. grupuri și scheletul de carbon al moleculei construite prin utilizarea unei C-nucleophiles (ex. metalloorg. Compuși).
H y k l e de f. s și u m e n e c o o m p o t h y d r I (substituție aromatică nucleofilă ..) este, de obicei, foarte dificilă și poate avea loc prin mecanisme "conexiune -. clivaj" sau prin interm. dehydrobenzene educație (Arin mecanism VSH):
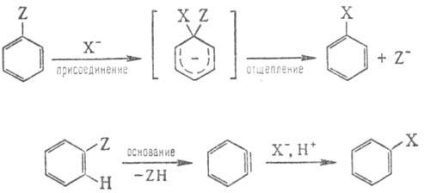
Mecanismul Aryne este de obicei implementat în p-tiile arii halogenuri cu baze puternice. de ex. NaNH2 în NH3.
Este foarte important pentru org. Sinteza p-TION și y k l e de f. n d uc a c e și n e n I s o m e d e n s u c a r b o n o m n o r o o t o m o y r l e p o n a:
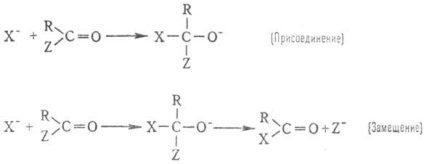
În anumite cazuri, procesul se oprește în etapa de cuplare, de exemplu. în HCN p-tiile cu aldehide și cetone pentru a da Cianhidrinele. În alte cazuri (de obicei, atunci când Z :. nucleofug bun exemplu halogen sau apă). Produsele de substituție formate. Aceste procese de tip includ practic importante p-TION de esterificare (p-TION acestea apar în prezența unui catalizator acid,): RCOOH + + R'OHRCOOR „+ H2 O și p-TION a derivaților carbonilici cu C-nucleofile care conduc la apariția de noi legături carbon-carbon.
H y k l e de f. EXEMPLU de la aproximativ f d și n e a la p și m n o D cu I h și g c e r o d u r c e r o d este de obicei posibilă numai în prezența moleculei de substrat electroni substituenți. Un exemplu este adăugarea de nucleofil. reactivi pentru a, b-a-nepredslnym acolo (de exemplu, apa.): CH2 = SNSOON + H2 ONOSN2 CH2COOH. Pentru cazul particular al nucleofil. conectarea la dubla legătură poate fi atribuită foarte important pentru org. Michael sinteza de reacție.
Lit. Hadson R. F. în carte. Reactivitate și de reacție căi. per. cu AFCL. M. 1977, p. 175-261; Carey F. Sundberg R. Curs avansat de Organic Chemistry. per. din limba engleză. M. 1981; J. March. Organic Chemistry. per. din limba engleză. M. 1987, vol. 2, p. 11-243; ibid, vol. 3, p. 5-45; Ibne-Rasa K.M. "J. Chem. Educ.", 1967, v. 44, № 2, p. 89-94; Stirling C.J.M. "As. Chem. Res.", 1979, v. 12, p. 198-203; Harris J. M. McManusS.P. Nucleofilicitatea, Wash. 1987.