Liquid nu este numai evaporare. La o anumită temperatură se fierbe.
Dependența presiunii vaporilor de temperatură. Starea de abur saturat, așa cum experiența (am discutat despre aceasta în paragraful anterior) este descrisă aproximativ prin ecuația de stare a unui gaz ideal (10,4), iar presiunea este determinată prin formula
Cu creșterea temperaturii, presiunea crește. Deoarece presiunea de vapori saturați este independentă de volum, prin urmare, aceasta depinde numai de temperatura.
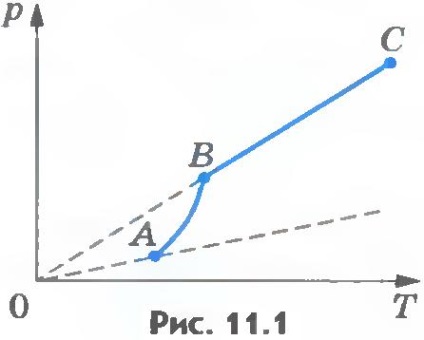
Cu toate acestea, dependența rn.p. de T. constatat experimental, nu este direct proporțional, ca într-un gaz ideal la volum constant. Cu creșterea temperaturii, presiunea vaporilor saturați de real crește mai repede decât presiunea gazului ideală (ris.11.1. Porțiune AB a curbei). Acest lucru devine evident dacă ne petrecem isochors gaz ideal prin (liniile punctate), punctele A și B. De ce se întâmplă acest lucru?
Când lichidul este încălzit într-un vas închis de lichid se transformă în vapori. Ca urmare, în conformitate cu formula (11.1) crește presiunea de vapori saturați nu numai datorită creșterii temperaturii fluidului, dar, de asemenea, datorită concentrației crescute de molecule (densitate) pereche. Practic, creșterea presiunii este determinată de creșterea concentrației cu creșterea temperaturii. Principala diferență în comportamentul unui gaz ideal și aburul saturat este că atunci când temperatura aburului într-un vas închis (sau schimbarea de volum la o temperatură constantă) variază în masa de vapori. Lichid este transformat parțial în abur sau în mod alternativ, aburul condensează parțial. nimic ca acest lucru se întâmplă să fie un gaz ideal.
Când tot lichidul sa evaporat, încălzirea suplimentară a vaporilor încetează să mai fie saturate, iar presiunea la volum constant va crește direct proporțional cu temperatura absolută (vezi. Ris.11.1. Porțiunea BC a curbei).
Se fierbe. Deoarece temperatura lichidului de răcire crește viteza de evaporare. În cele din urmă, lichidul începe să fiarbă. La reflux în întregul volum de lichid format în creștere rapidă bule de vapori, care se ridică la suprafață. Punctul de fierbere al lichidului rămâne constantă. Acest lucru se datorează faptului că tot lichidul furnizat la energia consumată pentru ao transforma în abur. În ce condiții începe să fiarbă?
Lichidul este întotdeauna prezența gazelor dizolvate eliberate pe fundul și pereții vasului, precum particulele de praf în suspensie în lichid, care sunt centre de vaporizării. Perechi de lichide, bule în interiorul sunt saturate. crește și bule cresc în dimensiuni, cu creșterea temperaturii, presiunea vaporilor saturați. Sub acțiunea flotabilitate plutesc în sus. Dacă straturile de lichid superioare au o temperatură mai scăzută în aceste straturi se produce condensarea vaporilor în bule. Presiunea scade rapid și bule colaps. Trantite are loc atât de repede încât peretele cu bule, cu care se confruntă, produce un fel de explozie. O multitudine de astfel de explozii micro creează un zgomot caracteristic. Când lichidul este suficient de cald, bule încetează să slam și plutesc la suprafață. Lichidul fierbe. Uita-te cu atenție fierbătorul pe aragaz. Veți găsi că aproape încetează să mai facă zgomot, înainte de fierbere.
la presiunea vaporilor saturați la dependența de temperatură explică de ce temperatura de fierbere lichid depinde de presiunea la suprafața sa. cu bule de vapori poate crește atunci când presiunea vaporilor din interiorul depășește cu puțin presiunea în lichid, care este compus din aer sub presiune pe suprafața lichidului (presiunea externă) și a presiunii hidrostatice coloanei de fluid.
Menționăm că evaporarea lichidului are loc la temperaturi sub punctul de fierbere, și numai de la suprafața lichidului la fierbere timp de generare a aburului are loc pe tot volumul de lichid.
Fierbere începe la o temperatură la care presiunea de vapori în bule în comparație cu presiunea în lichid.
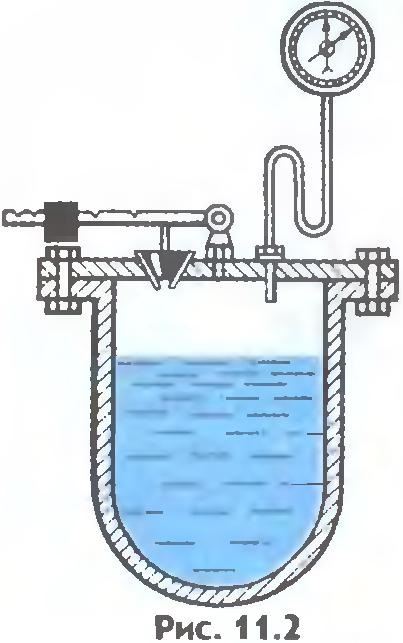
Cu cât presiunea externă, este mai mare temperatura de fierbere. Astfel, într-un cazan de abur la o presiune ajunge la 1,6 • 10 6 Pa, iar apa nu se fierbe la temperatura de 200 ° C În instituțiile medicale în vase închise ermetic - o autoclavă (ris.11.2) de apă clocotită are loc la presiune ridicată. Prin urmare, temperatura de fierbere lichid cu mult peste 100 ° C, Autoclavele folosite pentru sterilizarea instrumentelor chirurgicale și altele.
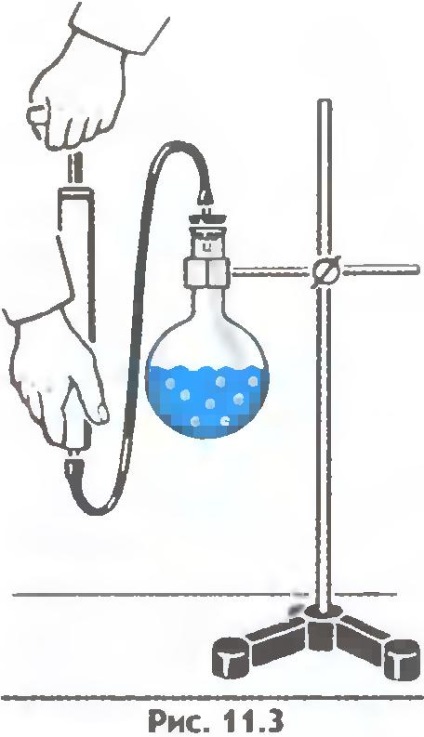
Pe de altă parte, reducerea presiunii externe, am deci scădea punctul de fierbere. Pompa de pompare a vaporilor de aer și apă din balon, poate provoca apă la fierbere, la temperatura camerei (ris.11.3). În cazul în care creșterea presiunii atmosferice scade munți, cu toate acestea, punctul de fierbere scade. La o altitudine de 7134 m (vf Lenin Pamirs) presiunea este aproximativ egală cu 4 • 10 4 Pa (300 mm Hg. V.). Apa fierbe acolo la aproximativ 70 ° C Gatiti carnea în astfel de condiții este imposibilă.
Fiecare are propria temperatura de fierbere lichid, care depinde de presiunea vaporilor. Cu cât presiunea de vapori, lichidul sub punctul de fierbere, deoarece la temperaturi mai scăzute presiunea vaporilor este egală cu atmosferică. De exemplu, la temperatura de fierbere de 100 ° C, presiune saturată de vapori de apă este egală cu 101325 Pa (760 mm Hg ..) și vapori de mercur - numai 117 Pa (0,88 mm Hg ..). Hg fierbe la o temperatură de 357 ° C, sub presiune normală.
Lichidul fierbe atunci când presiunea vaporilor saturați devine egală cu presiunea în interiorul fluidului.
.
1. De ce este de fierbere crește cu punct de presiune?
2. De ce este de fierbere crește substanțial presiunea vaporilor în bule în loc de creșterea presiunii prezente în aerul ei?
3. Cum să fiarbă lichidul, răcirea vasului? (Această întrebare nu este ușor.)
G.Ya.Myakishev, B.B.Buhovtsev, N.N.Sotsky 10 Fizică clasa
Planificarea lecțiilor în fizica. răspunsuri la teste, misiuni și răspunsuri despre cursuri, teme pentru acasă și să lucreze pe fizica pentru clasa 10
Dacă aveți corecturi sau sugestii la această lecție, vă rugăm să ne contactați.
Dacă doriți să vedeți alte ajustări și sugestii pentru lecții, uita-te aici - Forumul Educațional.