Stabilitatea sistemelor coloidale este capacitatea sistemului de a menține constantă dimensiunea particulelor dispersate și chiar distribuția acestora în mediul de dispersie.
Sistemele coloidale pot exista pentru o lungă perioadă de timp, un sisteme de dispersie stabilă sunt împărțite în două tipuri: cinetică (sedimentare-depunere) și agregate.
Kinetic determinata de capacitatea sistemului de a contracara sedimentare.
Agregat este abilitatea de a păstra intactă dimensiunea inițială a particulelor.
COAGULARE (lat. Sfasietor coagularea) caracteristice soluțiilor coloidale (sol) de proces, care cuprinde o fază dispersă într-o rolă sau în precipitat în solidificarea întregii soluții coloidale studen- gel. În ambele cazuri, există fuziune a particulelor individuale minut ale fazei disperse, coarsening lor sau de agregare.
Coagularea sub influența electroliți puternici.
soluțiile coloidale sunt foarte sensibili la prezența electroliților străine, coagulare poate fi cauzată de prezența unor cantități chiar mici de ele. De exemplu, coagularea are loc foarte repede, aproape imediat după formarea soluției, în cazul în care a fost primit în vase slab spălate care păstrate urme de săruri conținute în apa de la robinet. Cu toate acestea, în prezența unor cantități foarte mici de anumite soluții electrolit-to-a-gulyatora coloidal capabile să mențină stabilitatea agregatului. Cea mai scăzută concentrație de electrolit, provocând coagulare soluție coloidală limpede, se numește pragul de coagulare . Pragul de coagulare poate fi definită experimental gradual (de exemplu, dintr-o biuretă) adăugarea la testul sol soluție de electrolit ASC-la-ra atunci. O altă metodă de determinare a - prepararea unei serii de soluții electrolitice cu o concentrație uniformă în creștere, urmată de adăugarea la aceasta a aceluiași volum al soluției. Debutul coagulare poate fi observate vizual sau prin instrumente. Cel mai adesea, metodele optice sunt utilizate în aceste scopuri. În orice caz, pragul de coagulare poate fi calculat prin formula

coagulare Threshold este măsurat, de obicei, în mol / l sau mmol / l. Trebuie amintit că sensul fizic al acestei dimensiuni - cantitatea de electrolit (mol sau mmol) capabile de a provoca coagularea soluției coloidale 1 litru.
In afara de coagulare prag utilizate în chimia coloidală și valoarea inversă - coagulante capacitatea F:
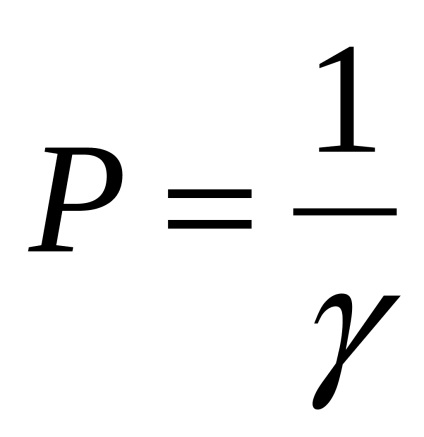
Dimensiunea P - l / mol sau l / mmol ce semnificație fizică corespunde volumului soluției, care poate fi coagulate (1 mol sau milimolar) electrolit.
prag de coagulare, și, prin urmare, capacitatea de coagulare sunt caracteristici aproximative, deoarece acestea depind de mai mulți factori - rata de electrolit plus coagulant, metoda de preparare a soluției, metoda de înregistrare, intervalul de timp dintre adăugarea electrolitului și punctul de fixare a temperaturii de coagulare evidentă și colab.
De obicei, Schulze-Hardy. Coagulante ion are taxa particule coloidale protiopolozhny, iar cea mai mare este, cu atât mai mult acțiunea de coagulare.
28) Clasificarea compușilor macromoleculari. Caracteristicile comparative ale soluțiilor DIU, coloidal și soluții adevărate. Cele mai importante clase de biopolimeri: proteine, acizi nucleici, polizaharide. Globular structura și fibrilare proteinelor. izoelectrică de stat. Punctul izoelectric al proteinei. Electroforeza.
Acest compus cu greutate moleculară IUD care prevaesht 1000 unități de masă de carbon sau AMU și macromolecule care sunt construite dintr-un număr mare de unități de monomer se repetă sau grupări moleculare.
IUDs au proprietăți nu numai soluții adevărate (auto-randomizare formează o soluție, stabilitatea termodinamică-lic, dispersibility molecular Omogen-Ness), dar și proprietățile soluțiilor coloidale (imposibilitatea unicitatii moleculelor de polimer pentru a pătrunde prin membrana semipermeabilă, presiune osmotică scăzută, viteză mică difuzie moleculară, împrăștierea luminii).
După cum sa menționat deja, nu există substanțe insolubile. Chiar și solide, care, cum ar fi, sunt insolubile - De asemenea, se dizolvă parțial, astfel formând particule minut într-o micele solvent. Aceste particule trec prin filtru. Ele sunt atât de mici și ușoare, care nu precipită. Astfel de particule (micele) numite coloid. O soluție - soluții coloidale.
Particulele coloidale pot fi luate în considerare în soluția cu fasciculul de lumină - raze reflectate și refractate apoi particulele coloidale devin vizibile cu ochiul liber. (Acest fenomen este denumit efect Tyndall).
Soluțiile coloidale de particule au o dimensiune de 0,1. 0,001 micrometri (microni).
Un alt nume pe scară largă coloizilor - coloizi. Pentru depozitare prelungită coloizilor devin gel (structura de gel este diferită de coloizilor poziție particulelor (micele) - sunt grupate în geluri).
Dar dacă gelul este încălzit, se va merge înapoi la Sol.
Coloizi, care trec în gel, dar conversia inversă este exclus - numitele suspensii. Dacă gelul se obține din nou sol - atunci este o emulsie.
Dacă turnați nisipul în apă și se agită bine, apoi nisip separat foarte repede de apă, și va fi în partea de jos a rezervorului. Dacă se amestecă praful cu apa, sedimentul va cădea prea, dar mult mai lent. In astfel de cazuri, este imposibil să vorbim despre o soluție, ca material de chastitsyrastvoryaemogo vizibile cu ochiul liber sau cu o lupă sau microscop. Acest amestec este eterogen. Amestecuri de acest tip, în care componentele pot fi separate prin simpla filtrare, de asemenea, menționată ca suspensii.
soluții adevărate - o singură fază de dispersii sunt caracterizate printr-o rezistență a legăturii ridicată între faza dispersată și mediul de dispersie. Adevărata soluție menține omogenitatea pe termen nelimitat. soluții adevărate sunt întotdeauna transparente. Particulele soluție reală nu poate fi văzut chiar sub un microscop electronic. soluții adevărate sunt bine difuzate.
starea fizică Componenta care nu se schimbă în timpul formării soluției, se face referire la solvent (mediu de dispersie), iar cealaltă componentă - solut (faza dispersă).
Pentru aceleași componente de solvent agregat de componente de stat este considerată, numărul care predomină în soluție.
În soluții de electrolit este în funcție de raportul dintre componentele electroliti sunt considerate ca fiind substanțe dizolvate.
soluții adevărate sunt subdivizate în:
· Tipul solventului: apos și neapos
· Tipul substanței dizolvate: soluțiile de săruri, acizi, baze, gaze etc.
· În ceea ce privește curentul electric: electroliți și non-electroliti
· La concentrația: concentrată și diluată
· În măsura în care limita de solubilitate: saturate și nesaturate
· Din punct de vedere termodinamic: idealul și realul
· Starea de agregare: gazoasă, lichidă, solidă.
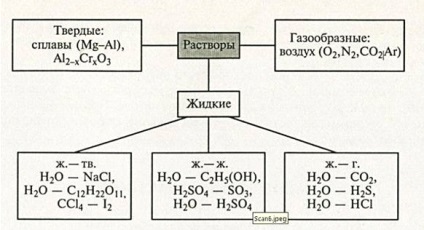
Cele mai importante clase de biopolimeri: proteine, acizi nucleici, polizaharide.
Proteine, biopolimeri macromoleculare monomeri care yavlyutsya aminoacizi.
Aminoacid-to-you organice care conține amminogruppu (-NH2), alcalino-eotoroy inerente Insulele de legare, și o grupare carboxil (-COOH), cu reziduuri acide (baze, k-m).
procesul de renaturare reface structura naturală a proteinei.
proces Denauratsiya tulburări structurii proteinelor naturale sub influența diferiților factori fizici și chimici (temperatură, presiune, acide, etc.), fără distrugerea legăturii peptidice (structura primară).
Funcțiile proteinelor: construcții, energeticheskkaya, protectoare, contractile sau cu motor, de rezervă, de transport, de reglementare, catalitice.
Nucleic biopolimerii acide complexe macromoleculare care monomerii sunt nucleotide. moleculă constă din resturile de nucleotide ale bazei azotoase, un monozaharide cinci carbon (pentoze) și acid fosforic.
Acidul nucleic este produșii de condensare ai fosfatului la voi, monozaharide (riboză, dezoxiriboză) și baze heterociclice.
Polizaharidele (S6N10O5) n - polimeri care conțin mai mult de 10 unități de monozaharide (glucoza, amiloza, etc. acetilglucozamin.), Printr-un simbol legături O-glicozidice. Ele fac parte din membrane celulare și organite, precum sunt furnizorii de energie. (Amidon, glicogen, celuloza).
compuși complecși: carbohidrați, proteine, glicoproteine, carbohidrați, lipide, glicolipide, complexul glicopeptidelor-murein, chitină, spre deosebire de moleculele de celuloză legate reziduuri de glucoză cu grupări care conțin azot și altele.
proteine globulare - au o formă sferică sau eliptică a moleculei (globulelor). În timpul formării globulelor de radicali amino hidrofobi sunt scufundate în regiunile interioare, radicalii hidrofili sunt situate pe suprafața moleculei. Atunci când interacționează cu faza apoasă radicali polari formează mai multe legături de hidrogen. Proteinele reținute într-o stare dizolvată din cauza sarcinii și hidratarea mantalei. In corpul proteine globulare îndeplini funcțiile dinamice (transport, enzimatice, de reglementare, de siguranță). Pentru proteine globulare includ:
Albumina - o proteina din plasma sangvină; Acesta conține mai multe reziduuri de glutamat și aspartat; depozitate la 100% saturație de sulfat de amoniu.
Globuline - proteine plasmatice; comparativ cu albumina obbladayut cu greutate moleculară mai mare și conține mai puține reziduuri glutamat și aspartat, se precipită la 50% sulfat de amoniu saturată.
Globular (sferică) - sferică compactă. Educație: hemoglobina, glicogen, pepsina, tripsina, pancreatina și altele.
Limited tumefiere: tranziția de la umflarea la dizolvare se produce sub anumiți factori (febră, etc.).
Fibrilare (liniar, ușor ramificat) ambalaj molecule -assimetrichnye: gelatină, celuloză și derivați ai acestora, colagen, poliacrilat de sodiu și altele.
Proteinele fibrilare - au o formă filamentoasă (fibrile). fibre de formă și fire. Între catene polipeptidice adiacente există multe reticulări încrucișate covalente. Insolubil în apă. Redevine soluție împiedică radicalii amino nepolare și reticulare între lanțurile peptidice. În corpul funcționează în primul rând funcția structurală, furnizează țesut rezistență mecanică.
Electroforeza-mișcare a particulelor de fază dispersată într-un câmp electric extern.
PH-ul la care proteina este in stare izoelectric se numește punctul izoelectric (pI).