După cum se știe, toate circumferențiale Rezumarea căldura procesului Q1 în lucru util este transferat numai (Q1- Q2) kcal, iar Q2 kcal este transmis la radiator. Q2 de căldură este dreaptă. Deși este necesar, pierderea de care ar trebui să depună eforturi pentru a reduce.
Să aflăm ce factori depinde. Să presupunem că echilibrul are loc ciclul Carnot (Fig. 5.9).
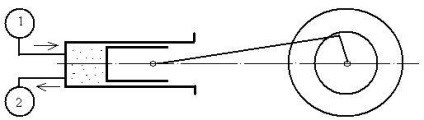
Fig. 5.9. Sistemul de organisme implicate în comisia
Pentru acest ciclu, sau =.
După cum puteți vedea, valoarea Q2 depinde de doi factori: relația și temperatura T2. Dacă temperatura este considerată o valoare constantă, pierderea Q. căldură depinde aproape exclusiv de raportul. Cu cât raportul, cu atât mai mare pierderea Q2.
Având în vedere relațiile mari de rol. În termodinamică a introdus o valoare deosebită, care depinde de această relație, și numit e n t r o n e și d.
Dacă procesul de echilibru furnizarea sau evacuarea căldurii este realizată la o temperatură constantă ca în ciclul Carnot, variația entropiei în astfel de procese să fie 1 kg corp
q - participarea la procesul de căldură;
T - temperatura la care are loc procesul.
In formula de mai sus s1 ia zero la T1 = 273 ° C, căldura specifică a apei luate pentru a fi de 1 kcal / kg # 8729; grad.
Sub lichidul entropie (apa) se înțelege creșterea entropiei 1 kg de apă având o temperatură de 0 ° C, în timp ce se încălzește la o presiune constantă la fierbere.
În cazul în care nu apa este adusă la fierbere, apoi entropia lui
unde T - temperatura finală a apei.
Entropia lichid de fierbere
Entropy saturat uscat cu abur este o creștere de 1 kg de entropie apă luată la 0 ° C, în timpul conversiei sale la presiune constantă în aburul saturat uscat.
Procesul de producere a aburului de apă clocotită are loc la o temperatură constantă; prin urmare, modificarea entropiei în acest proces poate fi găsit din ecuația
În acest caz (entropie abur uscat) (entropie lichidă); q = r - căldura de vaporizare) și T = Ts.
Este clar că entropia SX abur umed. pentru care q = XR, este egal cu:
Entropy abur supraîncălzit s reprezintă 1 kg creștere a entropiei apei luate la 0 ° C, în timpul conversiei sale la presiune constantă abur supraîncălzit.
In procesul la presiune constantă a temperaturii aburului supraîncălzit este crescută, astfel încât schimbarea de entropie în timpul supraîncălzirii este necesar să se calculeze prin ecuația
CPM - capacitate medie de căldură izobarice de abur supraîncălzit,
T - temperatura absolută a aburului supraîncălzit.
Din această ecuație, obținem