Acilarea este procesul de introducere a unei grupări acil în molecula compusului organic in loc de atomi de hidrogen sau un metal. RazlichayutS-, N- și O-acilare.
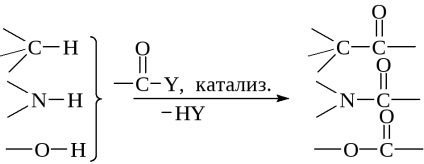
Agenții de acilare includ compus acil generală formulyR-CO-Y, în care R = alchil, arii, heterociclil; Y- grupare fugace = Hlg, R-COO-, OH, OR, NH2, NHR, NR2. și takzheN3. De asemenea, ca agenți de acilare folosit cetenă, dicetenă și altele.
Gruparea acil introdus într-o moleculă cu substanțe organice, cum ar fi tselyuvremennoy grupare protectoare labilă (cel mai frecvent -NH2), astfel încât uc să schimbe scheletul de carbon al moleculei și substanța care conferă proprietăți noi.
Acilarea este una dintre cele mai comune procedee pentru sinteza de medicamente și vitamine, precum și în sinteza precursorilor. Multe promedicamente includ grupări acil. In corpul uman, format ca deacilare substanță cu activitate biologică mai mare, care nu pot fi introduse direct în organism într-o doză mare datorită toxicității sau din alte motive.
Acilarea la C (c-acilare)
1. C-acilarea Friedel-Crafts arenelor Mecanism ketonov- -Sinteza aromatice și metode osuschestvleniyarodstvenno alchilat sub acilare Friedel-Crafts.
Mecanismul de reacție - substituția electrofilă, dar spre deosebire de reacția de alchilare - ireversibil.
Catalizatori de acilare - același material ca și cel al alchilării: acidul protic sau aprotic, alumină, silicagel, etc ...
Mecanismul de formare a particulelor electrofili:
Ca rezultat al interacțiunii catalizatorului cu particule de agenți de acilare electrofili formate:
- În primul rând, complexul bipolar, care este reactiv mai slab, dar mai probabil decât cation acylium liber.
- În al doilea rând, kationyatsiliya [RC = ORCO ], care sunt mult mai stabile decât alkilkationy (datorită distribuției mai uniformă a norilor de electroni de particule). Sărurile acylium pot fi izolați și oharakterizovany.Primerom sluzhitborftorid atsetiliyaCH3 CO BF4 -. Ele sunt generate ca un acid Lewis, și acizii minerali. Acizii organici în acizi minerali sunt transformați în ioni acylium mediu practic complet.
acid Lewis: În primul rând, formează specia activă; și în al doilea rând, care interacționează cu o cetonă format, și astfel sunt îndepărtate din zona de reacție cu produsul:
Cu toate acestea kolichestvokisloty Lewis ar trebui să fie de cel puțin 1 mol per mol de substrat.
Dacă, din orice motiv, o cetonă rămâne în reacție, reacționează cu catalizatorul sau acil cation particula secundară electrofilă. capabilă să reacționeze cu un substrat, având ca rezultat formarea de produse secundare de reacție:
Spre deosebire de arenovne acilare soprovozhdaetsyapoliatsilirovaniem alchilare. deoarece care rezultă cetonă este mai puțin activ decât substratul, iperegruppirovkami. deoarece cation acylium este mai stabil decât cationului de alchil și o reacție ireversibilă. Cu toate acestea, atunci când radicalii ramificați pot fi scindată și care rezultă CO în care carbocationilor și acilare alchilații Arene:
A) C-acilare de cloruri acide arenelor este larg utilizat în sinteza substanțelor medicamentoase. cloruri acide - agenții de acilare cei mai activi, dar, de asemenea, cele mai scumpe și toxice.
Condițiile de reacție (temperatură, timp, catalizator), activitate dependentă de substrat și clorură.
- Cu un substrat activ și acilarea arenelor cloruri și poate fi realizată fără catalizator:
- Cu toate acestea, cel mai adesea sinteza cetonelor efectuate în prezența unui catalizator puternic - clorură de aluminiu - la temperaturi joase:
- Când se utilizează clorura de zinc. reacția este condiții mai severe. Astfel, în fabricarea trankvilizatorafenazepama bromoanilină P- internă primul acilată la gruparea amino de la 100-160 ° C și apoi zinc masa de reacție zagruzhayuthlorid, iar temperatura a fost ridicată la 190-198 ° C Produsul este izolat și hidrolizat cu acid sulfuric diluat:
B) C-acilarea anhidride acide arenelor apare mult mai puțin frecvent reacționează cu molecula de substrat este doar jumătate din agentul de acilare, care este metoda suschestvennymnedostatkom. În acest sens, pentru acilarea este utilizat în principal anhidride acetic și ftalic, cel mai disponibil și mai ieftine.
- anhidridă acetică atsiliruyutatsidofobnye heterocicli cu cinci membri, cu un heteroatom, care, sub acțiunea acizilor minerali puternici sunt acidul protic razrushayutsya.Katalizatorami (de exemplu, acid fosforic) și acizi Lewis (clorura de olovaIV):
anhidridă ftalică în prisutstviihlorida arena atsiliruyutaktivnye zinc. de exemplu, fenol vsinteze fenolftaleină (indicator laxativ):
Reacția se realizează la 100-105 ° C În acest caz, după reacția de acilare a Cetona rezultată gidroksialkiliruet a doua moleculă de fenol.
Când acilarea mai puțin activă arenelor (benzen și omologii săi) ispolzuyutbolee catalizator activ. De exemplu, în acizi sintezebenzoilbenzoynyh care sunt sinteza syremdlya pornire antrachinonă și derivații săi, aluminiu ispolzuyutftalevy anhidridă prisutstviihlorida:

Clorura de aluminiu pentru această reacție sunt luate in exces (2-2,5 moli per mol de anhidridă ftalică). Reacția este de mare importanță industrială. De asemenea, ca benzen, cu anhidridă ftalică poate interacționa clorbenzenul, toluenul, naftalina, etc.
B) C-acilarea acizilor carboxilici datorită activității lor scăzut de asemenea rar utilizate ca anhidride. Un exemplu al acestei metode poate fi un mediu de închidere vkisloy inel antrachinona în exemplul de mai sus.
Suplimentar catalizator acid poate zinc bythlorid (sinteza geptilrezortsina):
2. Acilarea Gattermanu-Koch - sinteza aldehidelor aromatice (varianta C-acilare prin acilare Friedel-Crafts). Formilhlorid este un compus instabil. Cu toate acestea, ionul emuatsily corespunzător este format prin trecerea bezvodnyhoksida carbon (II) și acid clorhidric în amestec Arene, clorură de aluminiu și cupru (I):
Reacția intră în arenă. Activitatea în care nu reaktsiyahSE nizhegalogenbenzolov (hidrocarburi policiclice condensate, polyalkylbenzene și colab.). Fenolii nu reacționează. Inelul aromatic intra lishodnaformilnaya grup. aproape exclusiv la alin poziția deputatului existent.
aldehide Randament la 25-60 ° C, sunt, de obicei aproximativ 50-60%, dar cu creșterea presiunii (până la 3,9 MPa), acesta a crescut la 90%.
Substraturile sunt compus aromatic și heteroaromatic (incluzând o heterocicluri cu 5 atomi atsidofobnye) și olefine cu atom aktivirovannym hidrogen:

Sinteza 4. Reacția Reimer-Timana- a aromatici o-hidroxialdehide de fenol și cloroform într-o soluție alcalină (formilare prin alchilare). Yavlyaetsyadihlorkarben electrofil. care se formează prin reacția dintre cloroform cu un alcalin.
Substratul poate fi fenolii substituiți cu substituenți primul fel, naftoli și naftoli substituiți, chinolină hidroxi, tiazol, etc. precum și pirol, indol și heterociclii, cum ar fi:

5. reacția Kolbe-Schmidt - sinteza fenolat hidroxi aromatic și dioxid de carbon (C-acilarea anhidrida acidului carbonic) .În prezent, considerat că reacția are loc prin complexul pas obrazovaniya:
Procedeul se realizează într-o autoclavă. echipat cu un agitator cu palete și puternic sacou special pentru încălzirea cu abur de înaltă presiune. Anhidru fenolat de sodiu a fost încălzit la 180 ° C și sub presiune este introdus în dioxid de carbon autoclavă. Aceasta formează salicilatul de sodiu.
De asemenea, în această reacție fenoli, de asemenea, să reacționeze și aminofenoli. Astfel, editat de acid -aminofenola poluchayutp -aminosalitsilovuyu (PAS):
6. cicloalchene Acilarea și alchene. Particulele electrofile formate în condițiile de reacție acilarea arenelor sub acilare Friedel-Crafts poate reacționa cu alchenelor și tsikloalkenamipo mecanism plus electrofilă. Formată în compușii carbonilici-substituiți etom sunt instabile și, în anumite condiții, halogenhidric este scindat, apă etc. De aceea, prin reacția alchenele cu compuși acil, împreună cu aductul, produse și acilarea formate:
În multe cazuri, produsul de cuplare poate fi primar: