Chimie și Inginerie Chimică
Ar 0,9 CO2 0,04. Se determină compoziția aerului dizolvat în apă la 0 ° C Coeficientul de solubilitate a oxigenului în apă la 0 ° C 0.0489 azot 0,0235 argon 0,058 dioxid de carbon 1,713. [C.82]
La acea vreme, Dalton a arătat că solubilitatea gazelor individuale. într-un amestec cu alte, este direct proporțională cu presiunile parțiale ale acestora. și nu presiunea totală a amestecului. De exemplu, solubilitatea oxigenului în apă este de aproximativ două ori solubilitatea azotului (vezi. Tabelul. 7) și, prin urmare, aerul dizolvat în apă trebuie să fie mai bogată în oxigen decât aerul. [C.156]
Solubilitatea diferitelor gaze în apă, în condiții identice, variază în limite foarte largi. Astfel, nairimer la 0 ° C și presiune normală, 1 litru de apă se dizolvă HK1 823 g (sau 505 l) și numai 0,002 g H (0,022 L). Oxigenul este solubil în apă este de aproximativ de două ori mai mare decât azotul. De aceea, aerul dizolvat în apă este întotdeauna îmbogățit cu oxigen (conținând 34,1% în volum la 18 ° C în loc de 21,2% în atmosferă). Cu aceasta în apă pot exista numeroase și variate FO organisme vii rmy. [C.250]
Sub testarea normală a pompei cu palete într-un cadru închis în rezervorul 3 (fig. 3-25), set de suprapresiune. apă egal cu 5-10 m. Art. Aceasta elimină posibilitatea de a aerului aspirat prin conducta de alimentare cu scurgeri și de evacuare a aerului dizolvat în apă. în cazul în care conducta de alimentare are un vid, precum și posibilitatea de cavitație. Presiunea în conducta de alimentare 12. Presiunea măsurată de manometru pe pompa determina [c.225]
Dezavantajele acestor înălbitori ar trebui să includă o mai mare sensibilitate la fluctuațiile de temperatura apei de intrare și dizolvat în apă la aer. În cazul în care apa este furnizată încălzit mai mult decât strălucire cea anterioară apare precipitat a fost clarificat îndepărtarea apei din rezultatul convectie. înălbitori suspensie pot fi utilizate pentru separarea solidelor în suspensie și sedimente după coagulare cu condiția instalării apei reziduale de intrare pentru curățare, fără fluctuații semnificative de temperatură. care se realizează prin expunerea la apă în containerele intermediare sau aplicarea [c.126]
După cum se arată în [43], factorul determinant pentru concentrația inițială de bule numărabile sunt în condiții de presiune supraincarcarea flotație. Concentrația aerului dizolvat în apă înainte de gâtuirea afectează practic doar dimensiunea bulelor. Prin urmare, datele obținute într-un singur experiment, dimensiunea bubble poate fi extinsă la alte [c.98]
Mai mult, eliberând logaritmul, obținem o expresie pentru determinarea concentrației de aer dizolvat în apă la ieșirea din vasul de presiune NZ [c.150]
Cantitatea de aer dizolvat în apă în timpul flotație, și poate fi măsurată ca suma eliberată în stare gazoasă și care rămâne în soluție după gâtuirea prin dispozitiv special [24]. Dispozitivul este alcătuit din doi cilindri Lysenko 500-1000 ml capacitate, montate pe porțiunile conice ale scutului una față de alta. Cuplajele de cauciuc tub de sticlă plasate între ele calibrat cu o lungime de 300-400 mm și un robinet de la partea de sus a teului cu egalizare de tub inferior. [C.251]
Fenomenul de separare a gazelor dizolvate din lichide frecvent întâlnite în mediul înconjurător. De exemplu, dacă se toarnă într-un pahar cu apă de la robinet si se lasa sa stea un timp, atunci va exista bule de aer dizolvat in apa de pe pereții de sticlă. Dacă deschideți [C.24]
Volumul vasului de presiune este calculată pe 2-3 min ședere în cantitate de apă de aer dizolvat în apă este de 5% a debitului de apă purificată. vas de presiune echipat cu o supapă de siguranță. [C.350]
Motivul pentru care coroziunea locală este mai intens pătrunde în metalul decât coroziunea uniformă. este în continuare makropar acțiunea rezultată în urma localizare, datorită suprafeței neuniforme a șaibei metalice de aer dizolvat în apă. porțiuni metalice sub rugina primesc mai puțin oxigen decât curăța suprafața sa, și anozi de sacrificiu, astfel se formează makropar. În acest caz, fractura de metal. Este sub rugina se datorează acțiunii simultane a ambelor micro- și makropar. [C.332]
Extrem de neplăcut rezultat este o distrugere a pompei de cavitație. o primă roată lamă sub acțiunea șocurilor de presiune locale puternice care apar în timpul condensării la aceste suprafețe de bule de vapori. Simultan, materialul este supus coroziunii intensive. deoarece aerul dizolvat in apa continuta crescute (relativ la atmosferic) oxigen. Ca rezultat, suprafața este rugoasă, atunci spongioasă și sunt rapid distruse. [C.109]
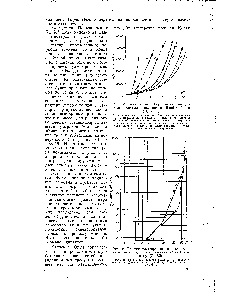
Fig. 56 prezintă grafice conform ecuației (131) care caracterizează dizolvarea aerului în apă având o temperatură de 20 ° la diferite presiuni (1 până la 7 kg / cm) și durata variabilă de saturație. Din aceste grafice se observă că la o presiune / = 1 kg / cm, cantitatea de aer dizolvat în apă variază ușor. fluid a deșeurilor la o presiune p = 1 kg / cm este aproape complet saturat cu azot, prin care oxigenul poate fi dizolvat numai în ea. [C.162]
Dacă eliminați aerul dizolvat în apă prin fierbere și, din nou, parțial se dizolvă, va exista un nou amestec îmbogățit oxigen gazos. Este ușor de calculat că după 6 cicluri amestecul de gaz va conține mai mult de 90% kislvroda (dar valoarea sa va fi, desigur, neglijabil în comparație cu inițială). [C.228]
În plus față de primarul Chisko într-o conferință de presă la care au participat Dr. Harold Schmidt de protecție a mediului de laborator. Dr. Schmidt a explicat că boala este cauzată de un exces de aer dizolvat în apă. aer dizolvat în exces. constând în principal din azot și oxigen, acesta trece prin branhii de pește și conduce la formarea de bule de gaz. În consecință, sângele peștilor scade mai puțin oxigen. Dacă se continuă în teche1ie câteva zile. peștele va muri. [C.92]
Pentru a calcula pompa de vid presupune că cantitatea de aer. să fie evacuat din proportsionalpo cantitatea condensatorului de apă de răcire și este exprimat prin formula 1 = 0,0 + C unde 0,02I / este volumul de aer dizolvat în apă. C cantitate de aer. aspirat prin scurgeri. [C.56]
Air are o temperatură de intrare a solubilității camerei IRI (20) și o presiune de 1 atm la 1 litru de apă se dizolvă 19,0 aer ly. (Cantitatea de aer dizolvat în apă scade cu creșterea temperaturii.) Pe măsură ce presiunea crește solubilitatea aerului dublu, de asemenea, este dublat. O astfel de ironortsionalnost între presiunea aerului și solubilitatea acesteia ilustrează legea lui Henry. care pot fi formulate manieră sleduyu1tsim la o temperatură constantă, presiunea parțială a uneia dintre componentele de soluții în fază gazoasă. în echilibru cu soluția proporțional cu concentrația componentului în soluție în concentrații nizpoy. [C.278]
Efectul aerului dizolvat în radiolizei apă a fost observată în primul studiu. pe această temă. Rios [1] și Fricke și Braunskomb [2] iradiindu Razele X degazat apa pura nu a arătat descompunerea sa, în timp ce prezența aerului dizolvat în apă este descompus pentru a forma H2, H2O2 și O2. Mai târziu, Allen [3] a arătat că electronii rapid. acțiune care ne este diferit de acțiunea razelor X radiație-chimice. descompus degazat apă pură, dar concentrația Ng și H2O2 format este foarte scăzută. Astfel, o presiune de hidrogen staționar. Potrivit lui Allen, dar pentru electroni, cu o energie de 1 MeV este de 10-20 mm Hg. Art. [C.7]
Deoarece apa se dizolvă mai bine oxigen și argon decât azotul, aerul dizolvat în apă cuprinde o concentrare mai mare a acestor gaze. decât în atmosferă. Deci, la 18 ° este format din 34,1% (vol.) Oz în loc să 21,27o în atmosferă. Ea are o mare biologicheskoeznachenie pentru organismele acvatice. [C.220]