Prima poziție este teoria moleculară-cinetică
Substanța constă din particule.
Molecule - este cea mai mică particulă dintr-o substanță care are proprietățile sale chimice de bază.
Molecula constă din atomi. Atom - cea mai mică particulă de materie, care nu este divizibil în reacții chimice.
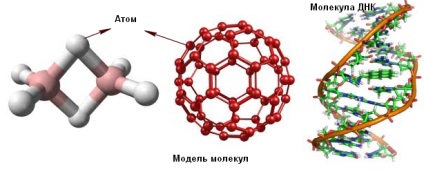
Multe molecule formate din doi sau mai mulți atomi deținute împreună prin legături chimice. Unele molecule sunt compuse din sute de mii de atomi.
A doua poziție a teoriei moleculare-cinetice
Moleculele sunt în mișcare aleatoare constantă. Această mișcare nu este dependentă de influențele externe. Mișcarea are loc într-un mod imprevizibil datorită coliziunii moleculare. Dovada este mișcarea browniană a particulelor (R.Brounom deschis 1827). Particulele sunt plasate într-un lichid sau gaz și să observe traficul imprevizibil datorită coliziunilor cu molecule ale substanței.
Dovezi de mișcare haotică este difuzie - penetrarea moleculelor substanței în interstițiile dintre moleculele altei substanțe. De exemplu, mirosul de aer odorizant, ne simțim, nu numai în locul unde a fost pulverizat, dar se amestecă treptat cu moleculele de aer din încăpere.
Statul de materie
În gazele, distanța medie dintre molecule este de sute de ori mai mare decât dimensiunea lor. Practic moleculele trece treptat și uniform. În urma ciocnirilor încep să se rotească.
În lichide, distanța dintre moleculele este mult mai puțin. Molecule efectua mișcarea de vibrație și de translație. Molecule prin mici intervale de tranziție bruscă la noua poziție de echilibru (observăm curgerea unui fluid).
Moleculele solide fluctuează foarte rar mutat (numai când temperatura crește).
A treia poziție a teoriei moleculare-cinetică
Între moleculele există forțe de interacțiune, care sunt de natură electromagnetică. Aceste forțe de ajutor pentru a explica apariția forțelor elastice. Când substanța este comprimată, moleculele mai aproape, forța de respingere dintre ele, atunci când forța externă amâna moleculele în afară (materialul intins) forță de atracție apare între ele.
densitatea materiei
Această valoare scalară, care este determinată prin formula
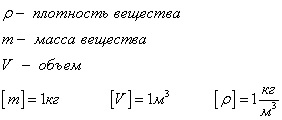
Substanțe de densitate - vezi tabel valori
Caracteristicile chimice ale substanței
numărul lui Avogadro NA - numărul de atomi conținute în 12g izotop de carbon
Cantitatea de substanță - un raport al numărului de elemente ale substanței la numărul lui Avogadro

1 mol de orice substanță conține același număr de particule, acest număr este egal cu constanta lui Avogadro.
Masa moleculară M - este masa molară a unei substanțe
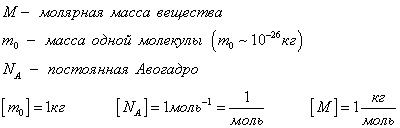
În cazul în care corpul include N m0 masa moleculară. greutatea
Concentrația de particule - numărul de particule în volumul
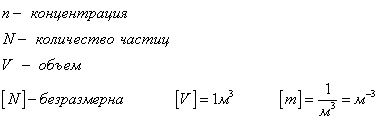
Puteți obține cu formula