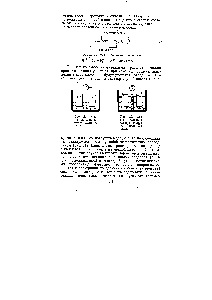
Punct de vedere istoric, primul element chimic sursă de curent a fost Volta fizician italian (1800). Elementul este format din alternativ plăci de cupru și zinc, separate prin distanțieri din pâslă îmbibată cu o soluție de acid sulfuric. Colecta un element, în loc de a folosi o cârpă pâslă sau hârtie de filtru. Calculați electromotoare maximă care poate fi obținută pe un singur membru secțiune. Fie ca lumina vine de la lanterna atunci când acesta este conectat la elementul Scrieți reacțiile la catod și anod. Să explice de ce, datorită separării cupru hidrogen gazos volți element de electrod are o tensiune de curent continuu. [C.354]

Considerăm că procesele care au loc în celula în timpul de descărcare de volți. [C.8]
Cu nivel tehnic astăzi de dezvoltare a celulei de combustibil, ne limităm aici la o discuție a elementelor reale. În același timp, amintiți-vă că deschiderea celulei Volta, care a servit ca prototip al unei celule de combustibil. cunoscut studiu condus de acțiune pantă curent electric. Galvani în 1791 postulat o relație strânsă între fenomenele electrice în razele electrice, pe de o parte, și a descoperit electricitatea animală în mușchii și nervii - pe de altă parte. Volta, pe de altă parte, a susținut că Galvani nu a arătat un animal. și energie electrică din metal. care, în opinia sa, acesta a fost obținut prin contactul a două metale diferite. El a fost cu siguranță dreptate în a spune că picioarele de broască în experiența istorică Galvani joacă rolul unui detector sensibil. dar tăgăduindu Volta de energie electrică a animalelor a fost greșit, deși aceasta este o concluzie greșită, și a condus la crearea unei celule electrochimice. cunoscut sub numele de electroplacare. Există mai multe elemente. Volta a primit foarte pilonii Volta. care au stat la baza bateriilor noastre moderne, cum ar fi bateriile Bacon (vezi. fig. 152), compania Allis-Chalmers (vezi. fig. 162-165), iar compania Union Carbide (vezi. fig. 4c și 1496). [C.462]
Element Volta este alcătuit din plăci de cupru și zinc imersat într-o soluție diluată de acid sulfuric. Datorită separării electrod de cupru hidrogen gazos (polarizare cm. 8.5) volți elementul nu are o tensiune constantă. A fost istoric, prima sursă de curent chimice. creat de fizicianul italian Volta (1800), sub formă de plăci alternativ de cupru si zinc, separate prin benzi de simțit îmbibat cu o soluție de acid sulfuric. [C.218]

Pentru fabricarea Volta necesitatea eclisă de zinc amalgamat. Curățați bine suprafața plăcii de zinc cu șmirghel, se clătește cu apă și apoi cu alcool și apă. Pune cipul într-o baie de saramură mercur timp de 5-10 minute (cu săruri de mercur pentru a efectua o coacere specială). Se spală cu apă și un electrod de zinc montat pe unul dintre pereții paharului bateriei. Pe peretele opus atârnat curățat placa de cupru. Se toarnă în sticlă 1N. Soluție de acid sulfuric. Conectați un voltmetru cu un consum mic de curent. Că în timp ce acolo scrie ecuații de reacție. având loc la electrozi. De ce placa de zinc amalgamiruetsya Care este forța electromotoare a elementului ce se utilizează alte celule de baterii [c.81]
Orice tsyya galvanică ca întreg nu este 1) echilibru. Elementul ireversibil este de obicei posibilă reacție chimică și circuit extern deschis (reacție 2n + N2504 elementul în volți). Dar reversibil (în sensul de mai sus) a circuitului în ansamblul său este departe de echilibru termodinamic. Dacă un astfel de circuit este închis pe rezistența finală și să se doteze. circuitul extern, un curent electric este de forță măsurabilă, adică. e. lanțul funcționează, se apropie ireversibil de echilibru. Circuit deschis rămâne doar temporar aproape neschimbat. De exemplu, în elementul deschis Daniel - Jacobi există o difuzie a Cu2 + ionilor prin soluția la electrodul de zinc în contact a electrodului de zinc cu ioni de cupru este un ireversibil (fără muncă) reacție deplasarea SO2 ionilor + din soluție cu zinc metalic, t E. Aceeași reacție, care este. sursa de curent atunci când se lucrează cu lementa. [C.519]
După inventarea primei celule electrochimice mai mult de cincizeci de volți elemente rămân singura sursă de curent electric în dezvoltarea lor sunt următoarele etape principale în utilizarea depolarizer 1833, care a făcut tensiunea celulei este yym mai stabil, folosind un 1836 g. Electrolit neutru, creșterea menținut sursele NOSTA curent. g. Dezvoltarea in 1865 celule cu un set depolyarizato solid, sporind astfel eficiența elementului. iso Bretenoux în 1888 g. Celulele uscate și, în final, aplicația 1914, în depolarizer ca oxigenul din aer. [C.13]
Un exemplu al unui element ireversibil poate fi un element de C 2n N2304 volți. Cu fluxul direct al procesului. t. e., în cazurile în care elementul prevede reacțiile actuale apar [c.378]
Să lucreze elementul Volta - primul din istoria celulei. nlasthshy de cupru și zinc (electrozii) sunt imersate în soluție 10% -nyl Ng804. Potențialul electrodului de cupru este mai mare decât potențialul de zinc. [C.167]
Surse chimice curente (1948) - [c.43]