ACETONĂ (lat acetum -. Oțet) (2-propanonă dimetil) CH3 COCH3. spun ei. 58.079 m .; acoperi bestsv. lichid cu miros caracteristic; m. pl. - 94,6 ° C, ... p.f. 56,1 ° C; d4 20 0,7920, nD 20 1.3588; 0.36 mPa.s (10 ° C) 0.30 mPa * s (30 ° C); 0,0237 N / m (20 ° C); tkrit 235,5 ° C, 4,75 MPa pkrit; 749.3 ° C p J / (kmol * K); H ° isp 29,1 kJ / mol (56,1 ° C) arde -1787kDzh H ° / mol N Mod ° - 216,5 kJ / mol ( gaz, 25 ° C) - 248 kJ / mol (lichid). Se miscibil cu apa si org. p-ERATOR ex. eter, metanol. etanol. esteri.
Acetona are toate chimice. St.-te alifatich caracteristic. cetone. Formele cristaline. Conn. cu hidrosulfit de metal alcalin. de ex. cu NaHSO3 - (CH3) 2 C (OH) SO3 Na. Numai. OxidanŃi puternici de ex. rr KMnO4 alcaline și crom-ta, acetona este oxidat la acetic și formic k-m, și mai departe - la CO2 și apă. Catalitica redus la izopropanol. amalgame Mg sau Zn, și Zn cu CH3COOH - la pinacol (CH3) 2 C (OH) C (OH) (CH3) 2. Atomii de hidrogen pot fi ușor înlocuite în halogenarea. nitrozare etc. Acțiunea clorului și acetonă alcalină convertit. în cloroform. să-ing interacțiune. cu acetonă pentru a forma hloretona (CH3) 2 C (OH) SS13. folosit ca antiseptic. Acetona oxidarea alcoolilor secundari în prezența. alcoolați A1 cetonelor (p-TION Oppenauer):
Acetona-bal sunt preim sti. t. sunat. Metoda cumen simultan cu fenolul din benzen și propilenă prin izopropilbenzenul (cumen) conform schemei:
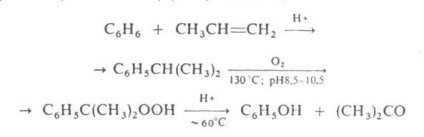
O serie de alte bal. Metodele de sinteză acetonă emană din izopropanol.
1. Oxidarea în faza de vapori (pisica - bloc metalic Cu, Ag, Ni sau Pt ..):
Randament ridicat de acetonă (aproximativ 90%) se realizează folosind Ag, depus pe piatră ponce sau argint mesh.
2. Avtokatalitich. oxidarea în fază lichidă la 90-140 ° C și 0,2-0,3 MPa
acetonă Randament: 95% din teoretic, H2 O2 87%.
3. Dehidrogenarea în faza de vapori, în prezența. ZnO, depus pe piatra ponce:
Gradul convertit. izopropanol în acetonă, la 225 ° C este de 84% la 380 ° C - 98% la 525 ° C - 100%. acetonă Randament aproximativ 90%.
New Ind. Procedeu pentru producerea de acetonă - oxidarea directă a propilenei în fază lichidă, în prezența. PdCl2 în p-ra mediu apos săruri Pd, Fe sau Cu, la 50-120 ° C și 5-10 MPa:
Randament: 90% acetonă. Valoarea gatului Roe proces reținut pentru producerea acetonei prin fermentarea amidonului sub influența bacteriilor Bacyllus acetobutylicus, transformă amidonul în acetonă și butanol (t. Chemat. Acetona fermentare). ., Etc metode cunoscute pentru producerea de:
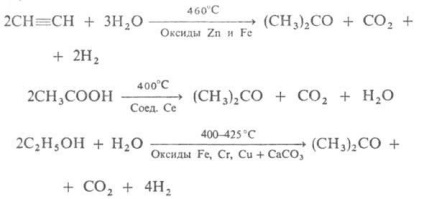
Vechi bal. Metoda de obținere uscată distilare acetonă (CH3 COO) 2 Ca - valoare pierduta.
Calitate. determinarea folosind acetonă colorate p-TION, de exemplu. cu dinitrobenzen, nitroprusiat de Na (reactiv Legalov); pentru a identifica - cristalin. derivați de acetonă, de ex. semicarbazonă (t. punct de topire. 187 ° C). Acetona determină cantitativ: 1) oximare:
HCl format este titrat cu alcali; 2) KMnO4 titrarea p-rom în mediu alcalin (în care acetona este oxidat la CO2 și H2O).
Acetonă - p-ERATOR org utilizat pe scară largă. in-in, mai întâi toate acetați nitrați și celuloză; din cauza toxicitate relativ scăzută este, de asemenea, utilizat în pishch. și Pharmaceuti. bal stimul; Acetona este utilizată ca materie primă pentru sinteza de anhidridă acetică. cetenă. diacetonalcool. oxid, mesitil, metilizobutilcetonă. metacrilat de metil. difenilolpropan. izoforonă și multe altele. conexiuni. Pro lume de aproximativ acetonă. 3 Mill. Tone / an (1980).
Pentru acetonă m. Aux. -20 ° C, t. AUTO APRINDERE. 500 ° C; CPV 2,15-13,00%. Acetona Inhalarea se acumulează în organism. pentru că eliminat lent din organism, pot exista cronice. otrăvire. MPC 200 mg / m 3.
===
App. Literatura pentru acest articol «Acetona». Kruzhalov BD Golovanenko BI coproducția de fenol și acetonă, M, 1963; Tedder John. A. Jubb lipsesc A. Industrial Organic Chemistry. per. din limba engleză. M. 1977; Kirk-Othmer enciclopedie, 3 ed. v. 1. N.Y. 1978, p. 179-91. Yu.N.Yurev.