Chimie și Tehnologie Chimică
În consecință, o persoană cu trei mese normale pe zi, regimul se schimbă de trei ori pe zi. Cu toate acestea, schimbarea regimurilor exprimate în mod clar, pentru că în timpul zilei între mese, mici (5-6 h), iar perioada post-absorbtivă abia are timp pentru a începe (în cazul în care nu au timp), așa cum vine ora mesei viitoare. O stare tipică postabsorbtivă este considerată starea dimineața înainte de micul dejun, după o pauză de zece ore în timpul mesei. O imagine mai grafică este dată de modelul ritmului de nutriție pe care E. Kant îl aduse la marele phprosophus german, a scris o dată pe zi. Într-o zi, depozitele de glicogen din organism sunt epuizate, gluconeogeneza devine singura sursă de glucoză, glucoza este folosită în primul rând de celulele nervoase. în timp ce aproape toate celelalte celule sunt furnizate cu energie prin oxidarea acizilor grași. precum și corpurile cetone formate în ficat din acizi grași. Vom păstra acest model în minte, având în vedere schimbarea regimurilor de schimb de energie. [C.400]
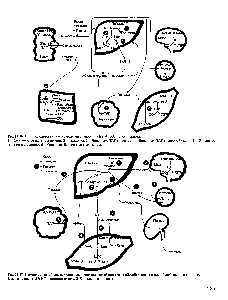
Fig. 11.17. Schimbări în metabolismul principalilor purtători de energie atunci când absorbantul este schimbat într-o stare postabsorbtivă. Aici și în Fig. 11.18 Organe CT - cetone. Acizi grași lichizi.
Printre aminoacizii. absorbită de creier, predomină valina. Capacitatea creierului de șobolan de a oxida aminoacizii cu un lanț lateral ramificat (leucină, izoleucină și valină) este de cel puțin 4 ori mai mare decât capacitatea corespunzătoare a mușchilor și a ficatului. Deși în starea postabsorbantă, cantități semnificative din acești aminoacizi sunt eliberați din țesutul muscular. ele nu sunt absorbite de ficat și putem presupune că locul principal al utilizării lor este creierul. [C.311]
În Fig. 30.10 prezintă modelul general al metabolismului aminoacizilor în starea postabsorbtivă. Aminoacizi liberi. în primul rând alanină și glutamină, intră în sistemul circulator din țesutul muscular. Alanina, care se pare că este principala formă de transport a azotului [c.311]
Când trece de la starea postabsorbtivă la starea absorbtivă sau după terminarea lucrării musculare, secreția hormonală se oprește și întregul sistem revine la starea inițială inactivă. Adenilat ciclaza și fosfolipaza C sunt inactivate. cAMP este distrus de fosfodiesteraza, care provoaca trecerea tuturor enzimelor cascade intracelulare intr-o forma inactiva. [C.148]
În timpul digestiei, insulina activează fosfataza pro-teină, care defosforilează piruvat kinaza, transformându-l într-o stare activă. În plus, insulina din ficat afectează numărul de enzime. inducerea sintezei piruvat kinazei și reprimarea sintezei PEP-carboxinazei. În consecință, reacția glicolitică a piruvatului fosfoenolpiruvat este accelerată prin digestie și încetinită într-o stare postabsorbtivă. [C.157]
La un ritm normal de hrănire, concentrația de glucoză din sânge este menținută la 60-100 mg / dl (3,3-5,5 mmol / l), datorită influenței a doi hormoni principali, insulină și glucagon. Insulina și glucagonul sunt regulatorii principali ai metabolismului atunci când se schimbă condițiile de digestie, perioada postabsorbtivă și postul. (Starea de postabsorbție este timpul după ce digestia este terminată înainte de următoarea masă, dacă mâncarea nu este luată într-o zi sau mai mult, atunci această condiție este definită ca post). Pentru perioadele de digestie este nevoie de 10-15 ore pe zi, iar consumul de energie are loc in timpul zilei. Prin urmare, o parte din purtătorii de energie în timpul digestiei este stocată pentru utilizare în perioada postabsorbtivă (Figura 11.14). [C.283]
Sinteza și secreția de insulină și glucagon de glucoza reglementate, iar în sens opus, cu creșterea concentrațiilor de glucoză din sânge, insulină crește secreția de glucagon și, invers, scade. În acest fel. concentrația lor în sânge se schimbă reciproc în timpul digestiei, concentrația de insulină este mare. Concentrația de glucagon este scăzută în starea postabsorbtivă, raportul fiind opusul. Cu toate acestea, trebuie remarcat faptul că modificările de amplitudine ale concentrației de insulină mai mult concentrația de insulină glucagon variază de circa 7 ori și glucagon - 1,5-2 ori. Efectul acestor hormoni asupra metabolismului insulinei stimulează, de asemenea, stocarea substanțelor în timpul digestiei și glucagonul - mobilizarea acestora într-o stare postabsorbtivă. De aceea, direcția proceselor metabolice nu depinde atât de concentrația absolută a hormonilor, cât și de raportul concentrațiilor lor [insulină] / [glucagon] (indicele insulină-glucagon). [C.268]
Pentru starea postabsorptivă sunt caracteristice [c.385]
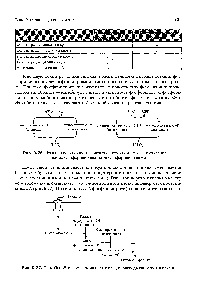
Fig. 9.27. Starea postabsorptivă de activare a descompunerii glicogenului în ficat
Comun pentru ritmul de nutriție umană - o masă de trei ori în timpul zilei cu două 6-7 ore și intervale de pauză de noapte cu durata de 10-12 ore după digestia carbohidraților orală masă amestecată se termină după aproximativ 2 ore, digestia grăsimilor și proteinelor -. 4, prin -5 h este o perioadă de digestie sau absorbantă. Aceasta este urmată de o perioadă postabsorbantă pentru o stare postabsortivă tipică, care ia starea de dimineață după somn înainte de micul dejun. [C.267]
Într-o stare postabsorptivă, concentrația de glucoză din sânge este de aproximativ 5 mmol / l (90 mg / dl). După masă, ca rezultat al absorbției glucozei din intestin, concentrația sa în sânge crește (hiperglicemie alimentară). Concentrația maximă de aproximativ 150 mg / dl este atinsă după aproximativ o oră și după aproximativ 1,5 ore concentrația de glucoză revine la nivelul postabsorbției. [C.268]
În reglarea primului ciclu, rolul principal aparține kinazei piruvate, a cărei formă fosforilată este inactivă, iar forma defosforilată este activă (Figura 9.31). În consecință, reacția glicolitică a piruvatului PEP este accelerată prin digestie și încetinită într-o stare postabsorbtivă. În ceea ce privește reacțiile acestui ciclu legate de gluconeogeneza (oxalacetat de piruvat FEP), atunci, probabil, ele apar cu o anumită rată în orice condiții. Aceasta se poate datora necesității de a menține o anumită concentrație de oxaloacetat în celulă. deoarece participă la multe procese importante. inclusiv ciclul citratului. [C.274]
În starea postabsorptivă, BIF este fosforilat, prezintă activitate fosfatazică, iar concentrația de 2,6-bisfosfat de fructoză scade. În consecință, activitatea 6-phosphofructo-1-kinaza, de asemenea, redus, iar ghivecele activitate-fosfa crește fructoză-1,6-fosfat, adică. E. direcție glicolitice este inhibată, iar direcția gluconeogenezei este activată. [C.275]
Sinteza acizilor grași și a grăsimilor este activată de alimente, iar dezintegrarea lor se face în postabsorbție și în post. În plus, rata de utilizare a grăsimilor este proporțională cu intensitatea muncii musculare. Reglarea metabolismului grăsimilor este strâns legată de reglarea metabolismului glucozei. Ca și în cazul metabolismului glucozei, hormonii insulină joacă un rol important în reglarea metabolismului grăsimilor. glucagon, adrenalină și procesele de comutare a fosforilării-defosforilării proteinelor. [C.306]
Fig. 10.23. Mobilizarea postabsorptivă de stat a grăsimilor depuse
Reglarea prin defosforilarea HMG-CoA reductazei este forma non-fosforilată activă (Figura 10.30, 3). Fosforilarea (inactivarea) implică adăugarea de glucagon la receptorul său pe suprafața celulară. și defosforilare (activare) - un semnal de insulină și receptorul său. Acest mecanism este o cascadă complexă de reacții. În acest fel. rata de sinteză a colesterolului se schimbă odată cu schimbarea stărilor absorbante și postabsorbtoare, deoarece insulina și glucagonul sunt implicate în reglementare. [C.315]
După primirea mâncării mixte, digestia carbohidraților se termină în aproximativ 2 ore, digestia fibrelor și a grăsimilor - timp de 4-5 ore această perioadă de digestie (perioadă absorbantă). Aceasta este urmată de o perioadă postabsorbtivă. La om, trei mese pe zi pentru perioade de digestie reprezintă 10-15 ore pe zi, iar consumul de energie are loc în decursul celor 24 de ore (cu o anumită scădere a orelor de somn de noapte). Prin urmare, o parte din purtătorii de energie în timpul digestiei este stocată pentru utilizare într-o stare postabsorbantă (Figura 15.2). [C.399]
Ficatul, țesutul adipos și mușchii sunt principalele organe asociate cu schimbarea regimurilor de stocare și utilizare a purtătorilor de energie. Comutarea metabolismului cu schimbarea perioadelor de digestie și a stării postabsorbante și menținerea concentrației de glucoză în sânge sunt furnizate de un sistem de mecanisme de reglementare. inclusiv hormoni de insulină. glucagon, adrenalină, cortizol. [C.400]
Munca musculară în timpul digestiei încetinește procesul de stocare, deoarece unele dintre produsele digestive provenite din intestine sunt consumate direct în mușchi. Într-o stare postabsorbantă, munca musculară stimulează mobilizarea stocurilor, în principal a grăsimilor. În reglementarea schimbărilor. asociate cu o schimbare în odihna si munca musculara. un rol important îi aparține adrenalinei. [C.400]
Concentrația de glucoză în sânge este determinată de echilibrul dintre ratele de intrare în sânge, pe de o parte, și consumul de țesuturi pe de altă parte. Într-o stare postabsorbantă, concentrația glucozei din sânge este în mod normal 60-100 mg / dl (3,3-5,5 mmol / l), o concentrație mai mare (hiperglicozemie) indică o întrerupere a metabolismului carbohidraților. După consumul de alimente sau o soluție de zahăr (încărcătură de zahăr), apare hiperglicozemia la persoanele sănătoase, hiperglicucozemia alimentară. De obicei, nu depășește 150 mg / dl și începe să scadă prin 1- [c.401]
Unul dintre simptomele bolii lui Isenko-Cushing este o scădere a toleranței la glucoză, adică depășirea normei hiperglicozemiei după mâncare sau încărcare cu zahăr. În cazuri severe, hiperglicozemia apare și în starea postabsorbtivă. Concentrația de glucoză din sânge poate depăși bariera renală și apoi există o glucozurie. Această afecțiune se numește diabet de steroizi. Scăderea toleranței la glucoză și hiperglicozemia sunt asociate cu creșterea catabolismului proteinelor și gluconeogenezei din aminoacizi. [C.404]
Gena de insulină din genomul uman este reprezentată de o singură copie. Insulina se formează în celulele insulelor pancreatice. Transformarea proinsulinei în insulină (vezi figura 4.19) are loc în complexul lamelar și granulele secretoare. În acest fel. granulele secretoare conțin (și secretă de la ei) insulina și peptida C în cantități echimolare. Glucoza stimulează secreția de insulină. În Fig. 15.6 arată modificări ale concentrației de insulină în sângele unei persoane după ingestie. Concomitent cu stimularea celulelor p la secreția de insulină, secreția de glucagon din celulele a insulelor pancreatice este inhibată. Glucagonul din sânge în starea postabsorbtivă este conținut într-o concentrație foarte mică - aproximativ 150 pg / ml în perioada postabsorbtivă, concentrația fiind chiar mai mică - aproximativ 70 pg / ml. [C.405]
A doua fază durează aproximativ o săptămână. Mobilizarea grăsimilor continuă, concentrația acizilor grași în sânge crește de două ori comparativ cu starea post-absorbție (Figura 15.10). Formarea corpurilor cetone în ficat și concentrarea lor în sânge crește. Ca rezultat, viteza de reacție a decarboxilării neenzimaice a acidului acetoacetic cu formarea acetonului devine apreciabilă [c.410]
Sinteza redusă și depozitarea glicogenului și a grăsimilor. În cazul diabetului, indicele insulină-glucagon este redus. Acest lucru se datorează nu numai unei scăderi a secreției de insulină. dar, de asemenea, cu o creștere a secreției de glucagon (insulina inhibă secreția de glucagon). În mod normal, insulina nu numai că stimulează procesele. Caracteristic pentru perioada absorbantă, dar elimină și efectele glucagonului. În absența insulinei, efectele glucagonului nu sunt eliminate. În consecință, stimularea proceselor de depozitare este slăbită, iar stimularea mobilizării resurselor este întărită, atât de mult încât ficatul, mușchii, țesutul gras, chiar și după masă, funcționează într-o stare postabsorbtivă. În acest caz, produsele digestive, precum și metaboliții lor, în loc să fie depozitați sub formă de glicogen și grăsimi, circulă în sânge. Probabil, într-o anumită măsură, apar procese ciclice costisitoare cum ar fi glicoliza simultană și gluconeogeneza sau sinteza și descompunerea grăsimilor etc. [c.412]