Fierul este un element al celei de a patra perioade a grupului VIII din subgrupul secundar (B) al mesei periodice.
Se referă la elementele familiei d. Metal. Denumirea este Fe. Numărul de serie este 26. Masa atomică relativă este 55.849 amu.
Structura electronică a atomului de fier
Atomul de fier constă dintr-un nucleu încărcat pozitiv (+26), în interiorul căruia sunt 26 de protoni și 30 de neutroni, iar aproximativ 26 de electroni se mișcă în patru orbite.
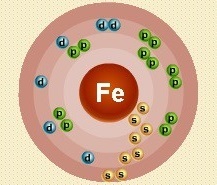
Fig.1. Schema schematică a atomului de fier.
Distribuția electronilor de-a lungul orbitalilor este după cum urmează:
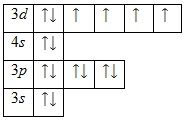
Diagrama energetică a stării de bază are următoarea formă:
Exemple de rezolvare a problemelor
Formula electronică a elementului are un capăt ... 3p 3. Scrieți întreaga formulă electronică a acestui element și determinați numărul său de serie în tabelul periodic. Universitatea Mendeleev.
Formula electronică completă va arăta astfel:
Numărul secvenței elementului poate fi găsit prin adăugarea tuturor electronilor atomului, indiferent de orbitalul pe care îl ocupă. Deci, acesta este cel de-al 15-lea element - fosfor.
Determinați numărul de electroni nepartiți în atomii din următoarele elemente: a) magneziu; b) mangan; c) brom.
a) Configurația electronică a atomului de magneziu:
1s 2s 2p 2s 6s 2s
Nu există electroni nepartiți:
b) configurația electronică a atomului de mangan:
În atomul de mangan există 5 electroni nepartiți:
c) configurația electronică a atomului de brom:
În atomul de brom 1 un electron neparat: