Termenul "pH" este o transformare matematică a concentrației ionilor de hidrogen (H +). Arată cum apa este acidă sau de bază. Litera "p" înseamnă "putere - putere" sau "exponent", iar pH - ul este definit ca un logaritm zecimal negativ din concentrația de ioni de hidrogen. O schimbare a pH-ului cu o unitate înseamnă o schimbare de zece ori a concentrației de ioni de hidrogen. De obicei, intervalul de modificări ale pH-ului este de 0-14 unități, dar poate depăși aceste limite. La 25 ° C, pH 7,0 este un indicator neutru, în care concentrațiile de ioni de hidrogen și ioni de hidroxid (OH -) sunt aceiași (fiecare 10 - 7 mol / l). Condițiile devin mai acide atunci când pH-ul scade, și mai mult atunci când - crește.
pH-ul apelor naturale
Apa clară, în contact cu aerul atmosferic, are o reacție acidă de aproximativ 5,6, deoarece dioxidul de carbon se dizolvă în apă și formează acid carbonic. Acest acid disociază cu ionul de hidrogen (H +) și bicarbonat (HCO3-):
CO2 + H2O = H2CO3 = H + + HCO3 -
Apele naturale nu sunt niciodată curate, deoarece apa este un solvent excelent. Unele gaze sau substanțe solide sunt dizolvate în admisie, iar unele dintre ele afectează pH-ul. Bicarbonatul și carbonatul (CO3 2) sunt ioni încărcați negativ (anioni), care se găsesc de obicei în apă. Aceste anioni de bază provin de la calcarul dizolvat și cresc pH-ul. Bicarbonații și carbonații sunt responsabili în principal de această proprietate a apei ca "alcalinitate" sau, cu alte cuvinte, capacitatea apei de a neutraliza acizii.
Interacțiunile chimice dintre dioxidul de carbon, ionii de hidrogen și anionii, care formează alcalinitatea și proprietățile tampon ale celor mai multe ape naturale, provoacă o gamă de fluctuații ale pH-ului de 6-8,5. În absența absorbției și îndepărtării dioxidului de carbon, pH-ul inițial al apei la contactul cu atmosfera depinde de alcalinitatea acesteia. Apa cu alcalinitate scăzută are un pH inițial la limita inferioară a acestui interval și cu o alcalinitate ridicată - la limita superioară a intervalului.
Deși alcalinitatea determină pH-ul inițial, dizolvarea și eliberarea dioxidului de carbon determină creșterea sau căderea acestuia. Reacția de mai sus, în primul caz, este îndreptată spre dreapta, iar în cel de-al doilea - spre stânga. Severitatea reacției depinde de cantitatea de dioxid de carbon și de alcalinitate, care determină proprietățile tamponului și ușurează efectele dioxidului de carbon.
Un indice ridicat de hidrogen în iaz este o problemă
Activitatea biologică subacvatică controlează concentrația dioxidului de carbon în majoritatea apelor de suprafață, inclusiv iazul. Toate organismele vii respira continuu și eliberează dioxid de carbon. În după-amiaza, folosind energia soarelui, algele și plantele subacvatice o utilizează în timpul fotosintezei. Rata relativă a respirației și fotosintezei în iaz determină acumularea sau eliminarea CO2. și, în consecință, o scădere sau o creștere a pH-ului. Nivelul activității respiratorii depinde de temperatura apei și a biomasei de plante, animale și microorganisme în apă și sedimente de fund. Nivelul activității fotosintetice depinde în principal de intensitatea luminii solare, a biomasei vegetale și a temperaturii apei.
În după-amiaza, fotosinteza se desfășoară, de obicei, mai activ decât respirația, astfel încât concentrația de dioxid de carbon scade, iar valoarea pH crește. De îndată ce soarele coboară dincolo de orizont, fotosinteza scade și se oprește complet. Deoarece activitatea nocturnă persistă, pH-ul începe să scadă. A doua zi, fotosinteza începe din nou, iar ciclul de 24 de ore se repetă. Majoritatea mediilor apoase au aproximativ nivelul echivalent de activitate fotosintetică și respiratorie, astfel încât fluctuațiile pH-ului sunt scăzute. Cu toate acestea, atunci când plantele și algele cresc rapid, se elimină mai mult dioxid de carbon în fiecare zi. Ca urmare, pH-ul creste la nivele ridicate seara si poate chiar sa ramana ridicat in timpul noptii. Aceste condiții pot dura câteva zile, până când fotosinteza scade sau respirația crește.
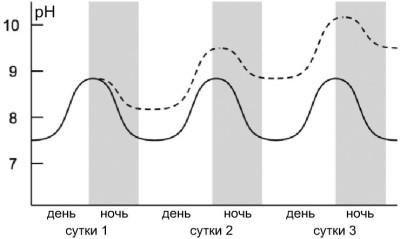
Problema pH-ului ridicat este adesea observată în iazurile de păsări și destinată cultivării creveților de apă dulce (Macrobrachium rosenbergii). Este asociat cu practica de aplicare a îngrășămintelor în timpul pregătirii rezervorului pentru sedimentare. Îngrășămintele asigură o creștere rapidă a fitoplanctonului, care utilizează toate dioxidul de carbon. Din păcate, stadiile incipiente de dezvoltare a crustaceelor și a peștilor sunt extrem de sensibile la efectele toxice ale valorilor ridicate ale pH-ului. Fry nu este capabil să se deplaseze în zone mai adânci, cu o aciditate mai ridicată.
În ciuda faptului că un pH ridicat este de obicei observat într-un iaz recent umplut și fertilizat, iazurile în care a trecut florarea au fost supuse și acestui flagel. Activitatea fitoplanctonului din iazurile fertilizate are adesea un caracter ciclic - perioade de înflorire și dispariție. Când un număr mare de celule algre mor, putrezirea duce la eliberarea de nutrienți și stimulează o nouă înflorire. Când plantele cresc repede, captarea dioxidului de carbon poate provoca o creștere a pH-ului, până când comunitatea fitoplanctonului ajunge la un nou echilibru.
Episoadele prelungite ale creșterii indicelui de hidrogen sunt observate în principal în iazuri, unde algele filamentoase domină între vegetație. De obicei, aceste iazuri au apă curată, permițând lumina soarelui să pătrundă adânc în grosime și să provoace o fotosinteză intensă sub apă sau pe suprafață.
În iazurile de acvacultură, această problemă apare foarte des, iar cu atât este mai gravă, cu atât este mai mare rigiditatea generală și cu atât mai mare este alcalinitatea (moderată, ridicată). Motivul pentru acest lucru este neclar.
Rezolvarea problemelor cu pH ridicat
Controlul valorilor ridicate ale indicelui de hidrogen din iazul de acvacultură este complex și nu are o practică specifică și de succes. Dificultățile sunt legate de faptul că conceptul de "pH ridicat" acoperă nu numai aspectele chimice, ci și interacțiunile complexe ale proceselor chimice și biologice. Din punctul de vedere al chimiei, această problemă poate fi rezolvată cu ușurință prin adăugarea de acid. Cu toate acestea, procesele complexe de schimb de dioxid de carbon vor rămâne aceleași, astfel încât cauzele nenorocirii nu vor dispărea nicăieri. Adăugarea de acid va permite scăderea pH-ului pentru o perioadă de timp, dar va crește din nou până când condițiile de mediu vor fi schimbate.
Rezolvarea pe termen lung a problemei în iaz implică probleme de biologie a rezervorului. Este necesar să se reducă la zero utilizarea zilnică a dioxidului de carbon. Acest lucru se poate realiza prin reducerea activității respiratorii fotosintetice sau crescute. Dar este dificil de influențat metabolismul comunității de iazuri, deoarece procesele biologice au un impuls ecologic semnificativ. Se bazează pe condițiile prestabilite de mediu care conduc agresiv la un anumit rezultat de mediu. De exemplu, atunci când un iaz nou umplut conține multe substanțe nutritive, primește lumină puternică a soarelui și are apă caldă, va exista cu siguranță o dezvoltare a unei comunități biologice care va crește pH-ul mediului. Este dificil să schimbi aceste condiții. În general, este mai bine să prevenim apariția unei probleme decât să încercăm să o rezolvăm.
Umpleți și gătiți iazul cât mai curând posibil
Probleme cu o valoare mare a seară a indicelui de hidrogen apar, de obicei, în primele câteva săptămâni după umplerea iazului de acvacultură. În acest moment, substanțele nutritive pentru plante, formate din furaje și îngrășăminte, provoacă o creștere rapidă a algelor. Pe de altă parte, biomasa organismelor respiratorii este relativ scăzută. După prima explozie de înflorire, pH-ul seara scade, deoarece există un echilibru între formarea și îndepărtarea dioxidului de carbon. Odată cu îmbătrânirea iazului, materia organică începe să se acumuleze (în special în sedimente). Gloarea și producerea de dioxid de carbon ajută la reducerea valorilor pH-ului maxim.
În consecință, pentru a minimiza problema pH-ului ridicat, iazul trebuie preparat cât mai curând posibil, de preferință cu câteva săptămâni înainte de stocare. Acest lucru nu este întotdeauna posibil, deoarece unele animale, pentru a evita pierderile cauzate de insecte de pradă sau pentru a cădea pentru o perioadă de abundență de alimente naturale, ar trebui populate imediat după umplerea și fertilizarea iazului. De exemplu, prăjiturile unei prăjituri de strih striped trebuie să fie stocate într-o perioadă de mulțime de rotifere. Rotifer este mâncarea preferată pentru prăjituri, iar vârful numărului de populații este observat la scurt timp după introducerea îngrășămintelor. Cu toate acestea, atunci când este posibil, stocarea ulterioară, până la prima înflorire, va ajuta la prevenirea pierderilor asociate cu un indice de hidrogen ridicat.
Rigiditatea și echilibrul alcalinității
De cele mai multe ori se pune problema unei valori ridicate a pH-ului în iazuri, unde alcalinitatea totală (cantitatea de bicarbonat și carbonat în apă) depășește duritatea (cantitatea de calciu și magneziu în apă).
De exemplu, iazurile pentru cultivarea creveților de apă dulce de la Universitatea din Mississippi, Starkville, au valori ridicate ale pH-ului la sfârșitul primăverii. Duritatea și alcalinitatea iazurilor de alimentare cu apă subterană este de 30 mg / l CaCO3 și, respectiv, 90 mg / l.
Lipsa rigidității în ceea ce privește alcalinitatea poate fi corectată prin introducerea gipsului (CaSO4). Se recomandă efectuarea acestei proceduri înainte de depozitare, în primăvară, după umplere.
Pentru a echilibra aproximativ valorile de rigiditate și alcalinitate, va fi necesară următoarea cantitate de gips: x = (duritate-alcalinitate) * 2.
De exemplu, dacă duritatea este de 30 mg / l CaCO3. și alcalinitatea a 90 mg / l de CaCO3. au nevoie de 120 mg / l de gips. În aceste condiții, vor fi necesare 1400 kg CaSO4 pentru 1 hectar de corp de apă de 1,2 metri adâncime. Aceasta este o cantitate mare de gips, dar fructele muncii persistă pentru o lungă perioadă de timp, deoarece calciul este foarte încet spălat cu ploaie.
Creșterea calciului din iaz va ajuta la scăderea valorii pH-ului și va ajuta hidrobionica să răspundă mai bine la săriturile din indicele de hidrogen și al altor factori de stres ai mediului. Concentrația relativ ridicată a acestui ion este, de asemenea, utilă pentru crustacee (de exemplu, creveți de apă dulce), care pierd calciul în timpul molării.
Cu toate acestea, beneficiile utilizării gipsului sunt controversate.
Introducerea alumului sau materiei organice
Acizii dificili de a reduce semnificativ indicele de hidrogen, deoarece apa din iaz este de regulă tamponată de baze (alcalinitate). Pentru o reducere semnificativă a pH-ului, este necesară o cantitate mare de acid. În plus, acidul este o soluție temporară care afectează efectul, dar nu și cauza.
Pentru a reduce pH-ul, tratarea apei de urgență poate fi efectuată cu alum (Al2 (SO4) 3). Este un remediu sigur, relativ ieftin care reacționează în apă sub formă de acid. În plus față de efectul său principal, alum este, de asemenea, un floculant și îndepărtează algele prin precipitare. Ie reduc biomasa algelor și, prin urmare, activitatea fotosintetică. Alum contribuie, de asemenea, la reducerea indirectă a indicelor de hidrogen prin eliminarea fosforului, un element biogen important.
Sulfatul de aluminiu nu are un efect permanent și poate necesita mai mult de o aplicare, până la dispariția unei porțiuni semnificative a plantelor. Datorită varietății factorilor din mediul acvatic, în special alcalinității, este imposibil să se evalueze cu exactitate efectul alumului. Supradozajul poate provoca o acidificare severă și chiar mai periculos decât pH-ul inițial ridicat.
Experiența practică dictează prudența utilizării alumului. Trebuie să începeți cu o doză mică de 10 mg / l, cu o adăugare treptată de 5-10 mg / l. Această substanță nu poate fi adăugată în apă cu o alcalinitate totală mai mică de 20 mg / l de CaCO3. deoarece chiar și o cantitate mică din aceasta va duce la o acidificare periculoasă a mediului.
Un mod sigur, pe termen lung de a reduce pH-ul este adăugarea de dioxid de carbon. Concentrația sa crește după introducerea porumbului organic, solului sau a făinii de bumbac. Putrezirea materiei organice conduce la eliberarea de CO2. Metoda nu va scădea imediat pH-ul, dar este sigur și relativ sigur. În general, aplicarea unei cantități de 17 kg / ha de organice timp de o săptămână va împiedica creșterea indicelui de hidrogen la un nivel nedorit. Această cantitate poate fi adăugată împreună cu doza zilnică de îngrășăminte. Doza zilnică totală de materie organică nu trebuie să depășească 56 kg / ha. Procesele de decădere, în timpul cărora se eliberează dioxid de carbon, consumă de asemenea oxigen, astfel încât să-i reducă concentrația la un nivel alarmant. Concentrația oxigenului dizolvat trebuie măsurată regulat și iazul trebuie aerisit dacă este necesar.
Suprimarea creșterii plantelor
Îndepărtarea rapidă a dioxidului de carbon în timpul creșterii rapide a plantelor este cauza pH-ului ridicat în iaz. Așteptând momentul în care viteza lor de dezvoltare va scădea, așa cum este descris mai sus, este o opțiune bună. Cu toate acestea, dacă este necesar să se reducă rapid indicele de hidrogen, viteza de creștere a biomasei vegetale este redusă de erbicide sau prin limitarea cantității de lumină care penetrează.
Folosind erbicide pentru a controla algele sau plantele superioare, va fi posibilă rezolvarea problemei pH-ului ridicat. Dar beneficiile acestei proceduri nu sunt adesea în valoare de risc și de cost. Putrezirea plantelor pierdute din erbicide conduce la foametea oxigenului și la acumularea de dioxid de carbon și amoniu. Unele erbicide sunt, de asemenea, relativ toxice pentru hidrobionții juvenili. Produsele cu cupru, de exemplu, au o linie relativ slabă între concentrația care ucide planta, iar concentrația care ar distruge puietului de pește și creveți. Controlul valorilor ridicate ale pH-ului prin suprimarea creșterii plantelor intră în conflict cu obiectivele urmărite în aplicarea îngrășămintelor. Acesta din urmă este însoțit de formarea hranei naturale în iaz pentru a-și crește productivitatea. Prin urmare, utilizarea erbicidelor pentru scăderea pH-ului este o soluție slabă.
În principal, trebuie introduse erbicide pentru a înlocui un tip de plantă cu altul, mai de dorit. De exemplu, pardoseala de alge filamentoase acționează adesea principala cauză a valorilor ridicate ale pH-ului în iaz, care a fost recent umplut cu apă și este destinată pentru cultivarea de crevete și puiet de pește. Aceste alge sunt nedorite, deoarece complică munca cu rezervorul, în special hrănirea și colectarea animalelor. Unele erbicide sunt utilizate cu grijă pentru a distruge algele filamentoase, spre deliciul fitoplanctonului.
Mai sigur, dar mai puțin eficient decât tratamentul cu erbicide, este restrângerea accesului la lumină. Una dintre metode a fost testată într-un iaz. Acesta include un colorant special pentru controlul creșterii buruienilor, care pătează apa în lumină albastră și reduce transmiterea luminii. De obicei, colorantul este eficient timp de câteva săptămâni. Cu toate acestea, moartea algelor din coloana de apă contribuie la dezvoltarea unui covor de alge filamentoase la suprafață. O altă metodă de reducere a transmisiei de lumină este aerarea continuă a rezervorului și agitarea sedimentului de jos.
Creștere bruscă a pH-ului
O creștere neașteptată a indicelui de hidrogen exercită stres sau chiar poate ucide animalele acvatice. Această problemă se remarcă la scăderea pH-ului în intervalul considerat a fi fiziologic acceptabil. Studiile efectuate de Centrul pentru Acvacultura Națională a Apelor Dulci din Stoneville, Mississippi, au demonstrat o susceptibilitate ridicată a somnului de canal la o creștere bruscă a pH-ului. Fry se poate adapta la apă cu o valoare a pH-ului aproape optimă (7,5-8,5) și rezistă modificărilor neașteptate ale indicatorului cu 4 unități mai mici. Cu toate acestea, indivizii mor când valoarea este cu 1 unitate mai mare decât intervalul. Creșterea de 1,5 unități ucide 50% dintre persoane și cu 2,2 unități - 100%.