sistem aperiodic de elemente chimice
Echipament: sistemul periodic al elementelor-ing chimice (grafic de perete și de masă pe studenți sută de cristale), tabla magnetica cu semne magnetice, care servesc ca ecran de joc, cardul cu sarcinile, masa de fixare a răspunsurilor, lucrări creative ale studenților din diferite discipline.
Înainte de a începe: La prima lecție profesorul anunță tema lecției viitoare - KVN, clasa de divizibil cu trei echipe (în acest caz, sunt luate în considerare și îi place personale ale elevilor, dar puterea echipei ar trebui să fie aproximativ egal-ximativ). Fiecare echipă alege un capitan (un student cu o cunoaștere temeinică a subiectului). În viitor, căpitanii își pregătesc echipele, iar profesorul lucrează cu căpitanii. Alegeți un juriu format din trei persoane care vor ajuta profesorul să urmeze jocul. Profesorul urmărește elevii la ceea ce trebuie să știe și poate generaliza lecția. Pentru a face acest lucru, clasa pune întrebări pe care să le acorde atenție. Există, de asemenea, posibile subiecte pentru re-enactments, deoarece scrierea abstractelor este o condiție importantă pentru participarea la joc.
Rezumatele, rapoartele sunt efectuate în mod voluntar, dar băieții știu că cine va scrie un raport interesant va fi încurajat și vor fi luate în considerare puncte suplimentare la numărarea rezultatelor jocului. De regulă, aproape toți elevii se bucură să facă această muncă cu plăcere și să primească o mare satisfacție deja pentru că au învățat ceva nou și au împărtășit cunoștințele lor cu profesorul și colegii de clasă. Fiecare echipă are un titlu, un logo, un motto și pregătește un salut și temele.
Profesorul recomandă copiilor de școală o literatură suplimentară disponibilă în bibliotecă și biroul chimiei. Memorii sunt atârnate în sala de clasă.
Cunoștințele necesare pentru echipe în timpul KVN
2. Descoperirea legii periodice și a sistemului periodic.
3. Semnificația fizică a numărului ordinal al elementului, numărul grupului, numărul perioadei în sistemul periodic de elemente chimice.
4. Care este perioada? Periodicitatea? De ce proprietățile elementelor se schimbă periodic?
5. De ce proprietățile elementelor se schimbă brusc la sfârșitul unei perioade și în tranziția la perioada următoare?
6. Formularea modernă a legii periodice în lumina teoriei structurii atomului.
7. Înțelesul legii periodice.
8. Listează faptele pe care le cunoști, care în timpul vieții tale au confirmat corectitudinea legii periodice.
9. Listează oamenii de știință-chimisti - confirmatorii legii periodice.
10. Caracterizarea elementului pe poziție în sistemul periodic al elementelor chimice.
1. Marea lege astăzi.
2. Viața și munca.
3. Semnificația legii periodice pentru știință și tehnologie.
4. Confirmarea legilor fundamentale ale filosofiei pe baza unui sistem periodic de elemente chimice și a structurii atomului.
Fiecare echipă se află pe un rând separat, condus de capcină. Pe tabloul magnetic afișat atașat emblemele și numele echipelor.
După fiecare activitate de pe tablă, rezultatele sunt marcate. Până la sfârșitul lecției, toate rezultatele vor fi vizibile, iar profesorul împreună cu elevii vor putea să tragă o concluzie care tip de muncă și ce echipă a provocat cele mai mari dificultăți (profesorul notează lacunele cunoașterii în cunoștințele studenților despre subiect).
Profesor. În istoria științei lumii, numele unor oameni de știință celebri sunt imprimate, ale căror descoperiri au contribuit la progresul cunoașterii despre natură, stăpânirea secretelor sale și utilizarea lor în beneficiul omenirii. În istoria cunoașterii umane, multe exploatații. Dar foarte puține dintre ele pot fi comparate cu ceea ce sa făcut. Mărimea fetelor științifice ale lui Mendeleev nu numai că nu este șters de timp, ci continuă să crească. Și nimeni nu poate spune dacă conținutul uneia dintre cele mai mari generalizări din știință - legea periodică - va fi vreodată epuizat până la sfârșit.
Legile naturii, descoperite de om, sunt diferite. Ele sunt greu de comparat unul cu altul. Dar legile sunt comparabile în cea mai importantă - dacă este posibil, predicția unei noi predicții a necunoscutului. Legea periodică în acest sens nu este egală în istoria științei.
Da, ne vom aminti de geograful mai mult decât o dată, Ce a mers taiga în vechile zile, El a dat nume râurilor fără nume, Numele inventate pentru dealuri. Dar de o sută de ori a descoperit că legea este mai importantă decât chimistul, că a investit eforturi considerabile și numele planetelor, zeilor, țărilor și popoarelor într-o singură masă unită pentru totdeauna.
Mulți oameni de știință au prezis existența și au descris elemente chimice necunoscute și proprietățile lor, bazate pe legea periodică, care a devenit "Star Chas" al unuia dintre cei mai mari oameni de pe planeta noastră.
În timpul salutării, fiecare echipă trebuie să-și prezinte numele, deviza și logo-ul.
Participați toate echipele. Profesorul pune întrebările. Primul care răspunde este cel care a ridicat mâna cea mai rapidă. Pentru un răspuns corect, complet - trei puncte, pentru adăugare - un punct.
În viitor, fiecare sarcină corectă este estimată la cinci puncte și o adăugare într-un punct.
1. De cine și când a fost descoperită legea periodică
2. Unde sa născut. Cine erau părinții săi?
3. Originea numelui Mendeleyev.
4. Unde am studiat. Ce voia să devină? De ce nu a reușit acest lucru?
5. Ce instituție de învățământ superior ați absolvit?
6. Cine și unde a lucrat Mendeleev în timpul descoperirii sale?
7. În ce an și pentru ce motiv ați eșuat?
8. Cum este citită legea periodică potrivit lui Mendeleyev?
9. Formularea modernă a legii periodice.
10. Ce confirmări ale legii periodice, cunoscute chiar și în timpul vieții lui Mendeleyev, știți?
11. Care este motivul unei schimbări netede și abrupte a proprietăților elementelor chimice în perioadele sistemului periodic de elemente chimice?
12. În ceea ce vedeți semnificația legii periodice pentru știință, tehnologie, industrie?
Răspunsurile sunt date la sfârșitul acestui scenariu.
Căpitanii de echipă merg la bord și trag un cartuș cu o sarcină.
1. Indicați elementul nr. 15.
2. Indicați elementul nr. 17.
3. Descrieți caracteristica elementului nr. 13.
Planul de elaborare a caracteristicilor unui element
1. Poziția elementului în tabelul periodic: numărul de ordine, masa atomică relativă, grupul, subgrupul, perioada.
2. Structura atomului, gradul de oxidare.
3. Afilierea la clasa metalică, nemetalică, element de tranziție.
4. Formula oxidului superior și natura sa.
5. Formula hidroxidului superior și caracterul acestuia.
6. Compus hidrogen volatil.
În timp ce echipele îndeplinesc colectiv sarcina, din fiecare echipă o persoană este chemată să efectueze următorul concurs.
În ce ecuații de reacții chimice este coeficientul! "Plasat incorect?
Rezultatele sarcinilor colective și individuale sunt rezumate. Rezultatele sunt reflectate în tablă.
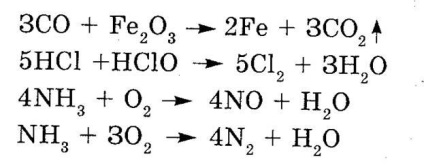
Pe placă sunt atașate trei foi și jumătate din formule. Este necesar să completați formulele. Câștigătorul este cel care îndeplinește rapid și corect sarcina.
Este necesar să indicați cu semnul → slăbirea proprietăților metalice și îmbunătățirea proprietăților nemetalice în următoarele cinci elemente. Explicați motivele pe care sunt aranjate semnele.
Sunt rezumate rezultatele Concursului Căpitanilor.
Ce elemente chimice sunt numite după oamenii de știință, în memoria succeselor astronomiei. în cinstea orașelor, în cinstea țărilor și a continentelor? Scrieți numele și numerele de serie ale acestor elemente. Sarcina este limitată de timp: cine va numi elementele mai mari în timpul alocat? (Răspunsurile sunt furnizate pe pagina.)
Rezumați lecția.
Cea mai bună echipă este recompensată. În plus, toți membrii echipei primesc ratinguri. Evaluările sunt oferite fiecărui elev de către întreaga echipă. Profesorul urmărește îndeaproape jocul și, la rândul său, face și note în timpul lecției. Evaluarea profesorului și scorul afișat de echipă, de regulă, coincid. Băieții sunt foarte parțiali între ei: nu vor lăsa jos persoana leneșă, dar vor aprecia lucrarea bine făcută. Căpitanii echipelor sunt remarcați în special de către profesor, deoarece au efectuat cea mai dificilă lucrare în timpul pregătirii și în timpul lecției.
3. În genealogia compilată în 1880, este scris: "Numele de familie a fost adesea dat de învățătorii școlii spirituale; fa-milia Mendeleev a fost dat tatălui său atunci când a schimbat ceva, deoarece un proprietar învecinat a schimbat caii și așa mai departe. Profesorul, în conformitate cu co-sunetul "Eu îl dau", a intrat, de asemenea, în tatăl sub numele de Mendeleyev. "
4. În vara lui 1850, Mendeleev a depus documente la Academia de Medicină și Chirurgie din Sankt Petersburg. Cu toate acestea, anatomia sa dovedit a fi dincolo de puterea unui tânăr impresionant: nu a putut suporta primul test - prezența în teatrul anatomic. De la o carieră medicală trebuia să fie abandonată. Mama a sugerat un alt mod - de a deveni un profesor.
5. În 1855, Mendeleev a absolvit în mod strălucit Institutul Pedagogic Șef din Sankt Petersburg cu o medalie de aur.
8. Proprietățile corpurilor simple, precum și formele și proprietățile compușilor de elemente, se află în dependență periodică de greutățile atomice ale elementelor.
9. Proprietățile elementelor chimice și ale substanțelor simple și complexe formate de ele sunt într-o dependență periodică de magnitudinea sarcinii nucleului atomilor elementelor.
10. În 1871, Mendeleev a descris proprietățile elementelor necunoscute, numindu-le condiționat "eka silicon", "eka boron", "eka aluminiu". În mai puțin de patru ani, la fel ca la Paris, tânărul om de știință de Boibardan a descoperit galiu (1875).
Chimistii se agita!
La urma urmei, galiul a fost unul din trei,
Se așteaptă descoperiri în avans!
Și, după aceea, de sub pământ,
Brusc, scandiumul a fost găsit în Suedia,
Lumina germaniului a fost extrasă
(desigur, în Germania).
Apoi sa adăugat masa,
În el au apărut particule noi.
Glorificați, confirmați legea
Descoperind vremurile viitoare.
Galiu - Mendeleev ea a prezis „eka alumino-TION“, a fost urmată de deschiderea chimistul suedez „eka bor» - scandiu în 1879 și deschiderea «EKA siliciu» - Germania în 1886.
Mendeleev scrie: "Lecoq de Boiboardan, Nilsson și Winkler. Consider că sunt adevărați fortifiatori ai legii periodice. Fără ei, nu ar fi fost recunoscut într-o asemenea măsură. așa cum sa întâmplat acum. "
11. Motivul unei schimbări netede a proprietăților elementelor chimice în perioade este schimbarea treptată a numărului de electroni la nivelul electronic extern sau pre-existent. Proprietățile spasmodice ale elementelor chimice se schimbă atunci când se deplasează de la o perioadă la alta. Motivul este apariția unui nou nivel electronic. Treptat, acumularea de modificări cantitative la limita perioadelor conduce la un salt calitativ în proprietăți.
12. Legea periodică a permis oamenilor de știință să prezinte o serie de fapte și fenomene care predetermină dezvoltarea teoriei structurii materiei. Cu ajutorul legii periodice, a fost posibilă prezicerea și descoperirea elementelor chimice noi, inclusiv a celor transuranice. Legea periodică și sistemul periodic de elemente chimice au avut o importanță deosebită pentru descoperirea izotopilor radioactivi folosiți pe scară largă în tehnologia modernă, medicină și agricultură. Legea periodică a jucat un rol important în crearea unei teorii moderne a structurii atomilor. În plus, legea periodică și a sistemului periodic al elementelor Chemic-cal pronunțat legile generale ale naturii: transformarea cantității în calitate, este o singură lege-TION și lupta contrariilor, negarea negației, legea universală de dezvoltare a spiralei.
Răspunsuri În cinstea orașelor:
№ 12 - magneziu (Magnesia - oraș în Grecia);
Nr. 39 - ytriu (Ytterbi este un oraș nu departe de Stockholm);
Nr. 67 - Holmium (Stockholm - din latină Nr.1mia);
71 - Lutețiu (Lutetia - numele antic al Parisului);
Nr. 72 - hafniu (Hafniu - numele antic al capitalei Danemarcei - Copenhaga);
Nr. 97 Berkeley (Berkeley, California, SUA);
Nr. 000 - Dubniy (Dubna, Rusia).
În onoarea țărilor și continentelor:
Nr. 31 - galiu (Gaul - Franța);
Nr. 32 - germaniu (Germania);
44 - ruthenium (latină Ruthtnia - Rusia);
63 - europium (Europa);
69 - Tullia (Thule este o țară semi-legendară, cea mai nordică parte a țării, care corespunde peninsulei scandinave din Europa);
84 - poloniu (Polonia latină - Polonia);
87 - Franța (Franța);
95 - americium (America);
98 - California (nume de stat în SUA - California).
În memoria succeselor astronomiei:
Nr. 2 - heliu (Helios - soarele);
22 - Titan (cel de-al treilea satelit al planetei Uranus, al șaselea satelit -
Nr. 34 - Seleniu (greaca: Selena - luna);
46 - Paladiu (planeta Pallada);
Nr. 52 - Telur (pământ latin);
58 - ceriu (planeta mică Ceres)
92 - Uraniu (planeta Uranus);
93 - Neptun (planeta Neptun);
94 - plutoniu (planeta Pluto).
Nr. 64 - gadoliniu (chimistul finlandez Yu. Gadolin);
Nr. 96 Curium (Marie și Pierre Curie);
Nr. 99 - Einsteinium (Albert Einstein);
Nr. 000 - Nobelium (Alfred Nobel);
Nr. 000 - Lawrence (inventatorul ciclotronului E. Lawrence);
Nr. 000 - Rutherford (Ernst Rutherford);
Nr. 000 - boriu (Niels Bohr).