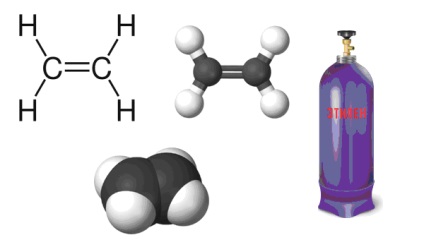
Etilena (etilenă) - hidrocarbură nesaturată, aparținând clasei de alcene și este strămoșul acestei serii omoloage. Atomii de carbon din acest compus sunt în h-hibridizare.
Masa molară este g / mol.
Proprietăți fizice - o substanță gazoasă, insolubilă în apă.
Etilenă se extrage în cantități mari din gazele de cracare și cocsificare.
Proprietăți chimice ale etilenei
- Datorită prezenței unei duble legături pentru etilenă, reacțiile de adiție sunt caracteristice. Hidrogenarea are loc în prezența catalizatorilor (Pd, Pt, Ni):
cerere
Etilena este cea mai importantă materie primă pentru producerea de polimeri, și anume: polietilenă, clorură de polivinil.
Din aceasta, la scară industrială, se produc etanol, antigel, acid acetic.
Exemple de rezolvare a problemelor
Etanolul poate fi obținut prin interacțiunea dintre etilenă și vapori de apă. Determinați efectul termic al acestui proces și înregistrați ecuația termochimică.
Să scriem ecuația termochimică a reacției de obținere în timpul hidratării etilenei:
Pentru a calcula căldura reacției chimice, vom folosi prima consecință a legii lui Hess:
Enthalpiile standard ale formării substanțelor sunt luate din cartea de referință:
.
Substituim valorile găsite în formula pentru calculul căldurii:
Pe baza valorii calculate, se scrie ecuația termochimică completă a reacției inițiale:
S-a obținut etanol din r. Care este soluția teoretică în acest caz? Determinați volumul teoretic al produsului.
Randamentul produsului de reacție chimică este raportul dintre volumul substanței obținute în cursul experimentului și volumul teoretic calculat din ecuația de reacție:
Se scrie ecuația reacției pentru producerea etilenei prin deshidratarea etanolului:
Determinați cantitatea de substanță etanol din raportul dintre masa și masa molară:
Conform acestei probleme, randamentul practic al etilenei este egal cu n, atunci
De la molei ai un pustiu
De la molei ai un pustiu
Plecând de la cantitatea găsită de substanță etilenică, vom găsi volumul ei teoretic: