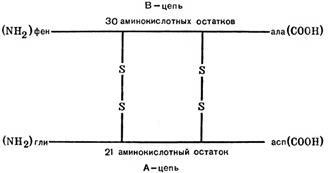
Proteina-peptida natura. Constă din 2 PPC, conectate prin legături disulfidice.
Sintetizată în # Celulele din insulele din Langerhans (pancreas). Sintetizat ca precursor inactiv. Se activează prin proteoliză parțială.
Insulina acționează prin receptori specifici: se pot schimba activitatea enzimei prin fosforilarea sau defosforilarea și / sau induce transcripția și sinteza de noi enzime proteice.
Influența asupra metabolismului
ü Influența principală - împreună cu glucagonul, menține un nivel normal de glucoză în sânge (sânge arterial - 3,5-5,5 mM / l, sânge venos - 6,5).
ü Activează enzimele reglementare ale sintezei de glicogen (glicogen sintază), glicoliza (glucokinază, FPC, piruvat kinaza), PD (glucoza dehidrogenaza-6F).
ü Stimulează depunerea de grăsimi (crește sinteza LP-lipazei)
ü Stimulează sinteza grăsimilor în ficat și țesutul adipos
ü Promovează sinteza grăsimilor din carbohidrați în țesutul adipos (activează GLUT-4)
ü Activează sinteza acizilor grași (acetil-CoA-carboxilază)
ü Activează sinteza colesterolului (HMG-reductază).
ü Stimulează sinteza proteinelor (efect anabolic)
ü Creșterea transportului aminoacizilor în celule
ü Îmbunătățește sinteza ADN și ARN.
Stimulează sinteza glucozei.
Cu vârsta, concentrația de Ca2 + scade și secreția de insulină este afectată.
În sânge, timpul de înjumătățire este de 3-5 minute.
După ce acțiunea este distrusă în ficat sub acțiunea insulinei (scindează lanțul de insulină).
Cu deficit de insulină apare diabetul zaharat.
Diabetul zaharat este o boală asociată cu absența parțială sau completă a insulinei.
Diabet zaharat de tip 1
Diabetul zaharat tip 2
IDDM (diabet zaharat insulino-dependent) Absenta completa a sintezei si secretiei de insulina in celulele pancreatice. Cauze: · Daune celulare autoimune (dezvoltarea anticorpilor la celulele glandei) · Decesele celulelor datorate infecțiilor virale (variolă, rubeolă, rujeolă). Este de 10-30% dintre persoanele cu diabet zaharat. Se manifestă în principal la copii și adolescenți. Se dezvoltă repede.
NIDDM (zaharat non-insulino dependent diabet) încălcare parțială a secreției de insulină sintezai (uneori hormon produs în cantități normale) motive: · activarea Raport · semnalizarea Violarea insulinei în celulele (receptorilor dezordonată) · Sinteza dezavantaj GLUT-4 · predispoziție genetică · obezitate · malnutriției (o mulțime de carbohidrati) · Stilul de viata sedentar · pe termen lung situație stresantă (adrenalina inhibă sinteza de insulină). Se dezvoltă lent.
Manifestări biochimice ale diabetului zaharat
1) Hiperglicemia - consumul de glucoză este perturbat de țesuturile dependente de insulină (grăsime, mușchi). Chiar și cu o concentrație ridicată de glucoză, aceste țesuturi se află într-o stare de foame de energie.
2) Glucozuria - la o concentrație în sânge> 8,9 mM / L, glucoza apare în urină ca o componentă patologică.
3) Cetonemia - glucoza nu intră în țesuturile dependente de insulină, atunci ele sunt activate Oxidarea (acizii grași devin principala sursă de energie). Prin urmare, o mulțime de forme de acetil-CoA, care nu reușesc să fie eliminate în ciclul TCA și este pe sinteza corpilor cetonici (acetona, acetoacetat, # 946; -hidroxibutirat).
4) Cetonuria - apariția corpurilor cetone în urină.
5) Azotemia - cu deficit de insulină, creșteri ale catabolismului proteinelor și aminoacizilor (deaminare), se formează multe NH3.
6) Azoturie - din uree se formează uree, care se excretă mai mult în urină.
7) Poliuria - excreția glucozei în urină conduce la o creștere a eliberării apei (cu diabet zaharat - 5-6 l / zi).
8) Polidipsa - setea a crescut.
Complicațiile diabetului:
R: Complicațiile acute se manifestă sub forma comă (metabolismul afectat, pierderea conștiinței).
Tipuri de comă în care se bazează o acidoză și o deshidratare a țesăturilor:
I - coma ceto-acidoasă - creșterea sintezei organismelor cetone și acidoză;
II - lacto-acidoză comă - circulație sanguină afectată, scăderea funcției hemoglobinei, care cauzează hipoxie. În consecință, catabolismul glucozei se îndreaptă spre glicoliza "anaerobă" pentru a se lacta. Se formează o mulțime de acid lactic, apare acidoza;
III - coma hiperosmolară - datorită hiperglicemiei creșterea presiunii osmotice a sângelui, iar apa este transferată din celule in sange se produce deshidratare. Ca urmare, schimbul de apă-electroliți este perturbat. În consecință, există o scădere a fluxului sanguin periferic (creier și rinichi) și hipoxie.
B: complicații târzii:
cauza principală este hiperglicemia.
Ca rezultat, apare glicozilarea non-enzimatică (spontană) a proteinelor, iar funcția lor este perturbată. Deci, există "picioare" diferite (angio-, neuro-, neuro-, retino-).
De exemplu, glicozilarea hemoglobinei produce hemoglobina glicozilată ("glicată") - HbA1c.
În mod normal, concentrația de HbA1c este de 5%. Cu diabet, până la 50%.
La aceasta, afinitatea la oxigen scade → o hipoxie.
În lentilă, glucoza se alătură cristalinului, ceea ce crește agregarea moleculelor. În consecință, există o înrăutățire a lentilei, ceea ce duce la cataractă.
In diabetul zaharat deranjat sinteza colagenului: Glicozilarea funcției perturbate a membranelor bazale (de exemplu, vasele de sânge), și în consecință perturbat fluxul sanguin și permeabilitatea vasculară (la nivelul membrelor inferioare). Acest lucru duce la picior diabetic și cangrenă.
Aderarea la glucoza apo LDL proteina B100 modifica structura lor, ele sunt capturate de către macrofage ca fiind străine pătrund în endoteliul vascular deteriorat, crescând riscul aterosclerozei.
Tratamentul diabetului zaharat:
· Terapia cu insulină (injectarea insulinei porcine, care diferă de om la un aminoacid);
· Luarea de preparate hipoglicemice:
o derivate de sulfaniluree - stimulează sinteza insulinei în pancreas (manninyl),
o Biguanidele - încetinesc absorbția glucozei în intestine, îmbunătățesc consumul de glucoză prin țesuturi (activează GLUT-4).
Se compune din 39 reziduuri de aminoacizi.
Sintetizată în # 945; - celule ale insulelor din Langerhans (pancreas). Acționează prin receptori cAMP, pe suprafața membranei.
Factorul hiperglicemic (crește nivelul de glucoză din sânge).
Influența asupra metabolismului:
Stimulează defalcarea glicogenului (glicogen fosforilază),
Stimulează gluconeogeneza (fructoză-1,6-bisfosfatază);
Lipid. îmbunătățește mobilizarea grăsimilor din țesutul adipos (activează TAG-lipaza prin fosforilare),
· Întărește Oxidarea acizilor grași (CAT-I),
· Induce sinteza organismelor cetone în mitocondrii.
Derivat de tirozină. De catecolamine.
Sintetizată în medulla suprarenale, sinteză și secreție sub influența sistemului nervos central.
Acționează prin cAMP, receptorii se află pe suprafața membranei (# 945; - și # 946; -adrenergic).
Crește concentrația de glucoză în sânge, tk. activează glicogen fosforilaza în ficat.
În situații de urgență, activează mobilizarea glicogenului în țesutul muscular prin formarea de glucoză pentru mușchi.
Inhibă secreția de insulină.
Este sintetizat din colesterol prin hidroxilare prin pregnenolon și progesteron. Se sintetizează în cortexul glandelor suprarenale.
Receptori din citoplasmă.
Influența asupra metabolismului:
· Stimulează gluconeogeneza (PVK-carboxilază, PEP-carboxinază). La concentrații ridicate crește distrugerea glicogenului, ceea ce duce la o creștere a nivelului glucozei din sânge.
· Inhibă sinteza grăsimilor în membre, stimulează lipoliza, sinteza grăsimilor în alte părți ale corpului.
· In țesuturile periferice (mușchii) inhibă biosinteza proteinelor, stimulează catabolismul aminoacizilor în sus (pentru gluconeogeneza). În ficat stimulează sinteza proteinelor-enzimelor de gluconeogeneză.
Cauzează involuția țesutului limfoid, moartea limfocitelor.
Derivații de cortizol au funcție antiinflamatoare (inhibă fosfolipaza A2, ceea ce duce la scăderea nivelului de prostaglandine - mediatori ai inflamației).
· Creșterea secreției de ACTH (datorată unei tumori) - boala lui Itenko-Cushing;
· Tumorile suprarenale - sindromul Itenko-Cushing.
Ca rezultat al activării gluconeogenezei, descompunerea glicogenului crește concentrația de glucoză în sânge. Există un diabet zaharat steroid (membrele subțiri, burta mare, fața moonului).
T3 și T4 sunt produse în folicul glandei tiroide din tirozina aminoacidului.
Receptorii acestora sunt localizați în nucleu, pot fi în citoplasmă.
Sinteza depinde de consumul de iod cu hrană și apă. Pentru a menține sinteza normală, sunt necesare aproximativ 150 μg iod pe zi (200 μg pentru femeile însărcinate).
1. Tiroglobulina este sintetizată în celule foliculare (conține 115 reziduuri de tirozină).
2. Apoi intră în cavitatea foliculului.
3. Se înregistrează includerea iodului ionizat (I - → I +) sub acțiunea tiroperoxidazei la poziția a treia sau a treia și a cincea a inelului de tirozină. Sunt formate monoiodotirozina (MIT) și diiodotirozina (DIT).
4. Atunci se condensează:
MIT + DIT = T3 (triiodotirozină)
DIT + DIT = T4 (tetraiodotirozină)
T3 și T4 din compoziția de tiroglobulină nu au activitate și pot fi prezente în foliculi înainte de apariția stimulului. Stimul - TTG.
5. Sub influența TSH, se activează enzime (proteaze), care scindează T3 și T4 din tiroglobulină.
6. T3 și T4 intră în sânge. Acolo aceștia comunică cu proteinele purtătoare:
· Globulină care leagă tiroxina (principală)
Cel mai activ este T3. deoarece el are o afinitate pentru receptori de 10 ori mai mare decât cea a T4.
1) Efecte asupra celulelor:
§ crește metabolismul energetic (cu excepția gonadelor și a celulelor creierului)
§ mărește consumul de oxigen de către celule
§ stimulează sinteza componentelor CPE
§ crește numărul de mitocondrii
§ în concentrații mari - decuplare a fosforilării oxidative.
2) Creste metabolismul bazal.
Cu o deficiență a hormonilor tiroidieni, nou-născuții dezvoltă cretinism, la adulți - hipotiroidism, mixedem (edem de mucus), t.p. crește sinteza GAG și a acidului hialuronic, care întârzie apa.
De asemenea, se poate observa: tiroidita autoimună. Gusa endemică. Boala lui Bydova.
Cea mai mare glandă. Efectuează multe funcții:
ü menținerea concentrației normale de glucoză în sânge datorată sintezei și descompunerii glicogenului și gluconeogenezei
ü protecția - sinteza factorilor de coagulare (I, II, V, VII, IX, X)
ü afectează metabolismul lipidic: sinteza acizilor biliari, corpuri cetone, HDL, fosfolipide, 85% colesterol
ü afectează metabolismul proteinelor: ciclul ornitinei, neutralizarea aminelor biogene
ü participă la metabolismul hormonilor
ü efectuează funcția de dezintoxicare (neutralizare).
Substanțe toxice endogene.
Xenobioticele sunt substanțe care nu îndeplinesc funcția de energie și plastic din organism:
· Elemente de activitate vitală (transport, industrie, agricultură)
· Substanțe toxice din parfumerie, vopsele și lacuri
Neutralizarea poate avea loc în două etape:
1 - dacă substanța este hidrofobă, atunci în prima etapă aceasta devine hidrofilă (solubilă în apă)
2 - conjugarea - combinația de substanțe toxice hidrofile cu unele alte → neutralizare.
Neutralizarea poate fi limitată la prima etapă, dacă în prima etapă substanța toxică a dobândit hidrofilitate și devine inofensivă (a doua etapă nu se scurge).
Neutralizarea prin a doua etapă apare numai dacă substanța toxică este hidrofilă (numai conjugarea se realizează).
1 stadiu de dezactivare: hidrofob → hidrofilic
Poate curge prin:
· Hidroxilarea - cel mai adesea (formarea de grupări OH într-o substanță toxică).
Este implicat CPE microzomal. (CPE mitocondrial - funcție energetică, microsomal - plastic).
Microzomii sunt bucăți de EPR netedă.
În CPE microsomale, enzimele pot funcționa:
· Monooxygenaze - se utilizează doar un atom de oxigen
· Dioxigenază - utilizați doi atomi de oxigen = o moleculă de oxigen.
Microsomal monooxygenază CPE
Componenta principală este citocromul P450. Are două situri de legare: una pentru atomul de oxigen, a doua pentru substanța hidrofobă.
Cytochromul P450 are următoarele proprietăți:
· Specificitate largă a substratului (neutralizează o mulțime de substanțe toxice - barbiturice, substanțe medicinale, alcool etc.);
· Inducibilitate = creșterea sintezei prin folosirea substanțelor toxice ("efectul regelui Mithridates", care a luat doze mici de otrăvire pentru a nu fi otrăvit).
P450 a adăugat un atom de oxigen și la introdus în substanța hidrofobă, trebuie activat.
P450 este activat de electroni, deci CPE este scurt.
· NADPH + H + - coenzima din PFP
· Enzima P450-reductază dependentă de NADPH - transportor intermediar; are 2 coenzime FAD și FMN - separă fluxul de H + și e -.
(pe exemplul de indol, care se formează atunci când se descompune triptofanul în intestin).
1. Doi atomi de hidrogen (sub formă de 2e și 2H +) se deplasează la P450-reductaza dependentă de NADPH: mai întâi la FAD, apoi la FMN.
2. Din acesta, 2H + este furnizat la reducerea unui atom de oxigen.
3. 2e - conectați P450, activați-l (P450 *) și împreună cu protonii mergeți la restaurarea H2O.
4. P450 activat atașează la sine cel de-al doilea atom de oxigen într-un centru activ, iar substanța hidrofobă în cealaltă.
5. P450 * introduce oxigen într-o substanță hidrofobă cu formarea unui grup OH.
Formează o substanță hidrofilă, dar totuși toxică.
Unele substanțe după prima etapă pot deveni și mai toxice (paracetamolul poate fi transformat într-o substanță toxică care afectează celulele hepatice).
Pasul 2: conjugarea
Hidrofile Toxice + Altă substanță = Doubt, netoxic, excretat cu bilă
Enzime transferază (clasa II).
O substanță care se alătură unei substanțe toxice
Donatorul substanței care se alătură
Concentrația normală a bilirubinei în sânge este de 8-20 μmol / l.
Acesta este un pigment roșu-brun, format în timpul defalcării hemoglobinei.
Există bilirubină directă și indirectă.
Hiperbilirubinemia - creșterea concentrației de bilirubină poate determina:
· Creșterea hemolizei celulelor roșii din sânge
· Afectarea funcției hepatice
Încălcarea fluxului de bilă.
Hem este un grup protetic de hemoglobină. Eritrocitele peri și sunt distruse după 20 de zile. Hemoglobina eliberată este distrusă (în splină, ficat, măduvă osoasă roșie).
1. Sub acțiunea hemoxygenazei, legătura dintre inelul 1 și 2 este distrusă. Pigmentul verde verdoglobin este format.
2. Fierul este separat spontan de el (cu transferinul intră în ficat unde este depus și folosit în mod repetat) și partea proteică (este clivată la aminoacizii care sunt folosiți în mod repetat). Se formează un pigment galben biliverdin.
3. Biliverdin este redus de biliverdin reductază (coenzima NADPH + H + din PFP).
4. Formele de bilirubină roșu-maroniu. Este toxic, insolubil, indirect (NPBil). Intră în sânge, se combină cu albumină (un purtător de proteine) și intră în ficat.
5. Ficatul îl captează cu ajutorul proteinelor ligandinei (L) și proteinei Z (Z). Defectul lor cauzează icterul ereditar - sindromul Gilbert (# 1006;).
6. În ficat, bilirubina indirectă este conjugată cu 2 molecule de acid glucuronic prin acțiunea UDP-glucuroniltransferazei. Se formează o bilirubină solubilă directă, neutralizată (Pbil).
Defectul UDP-glucuroniltransferazei provoacă sindromul Kriegler-Nayyar (icterul ereditar # 1006;).
7. Bilirubina neutralizată intră în intestin.
8. Sub acțiunea enzimelor, microflora se transformă într-un sterocilinogen incolor.
9. 95% din acesta este excretat cu fecale, unde este oxidat în aer, obținând o culoare maro și se numește sterocilină.
10. 5% prin vena hemoroidală intră în rinichi și se excretă în urină. Oxidat în aer, dobândește o culoare galbenă și se numește urobilinogen.
La o concentrație de bilirubină în sânge de peste 30 mmol / l, poate fi depusă în membranele mucoase și poate fi galben.
Icterul este diagnosticat de sânge, urină și fecale.
În funcție de cauzele icterului pot fi:
1. Extrahepatic = hemolitice.
Motivul - hemoliza crescută a eritrocitelor (cu transfuzia unui grup sanguin incompatibil sau cu un defect al enzimei PFP glucoza-6F-dehidrogenază).
În consecință, funcția hepatică funcționează normal, dar nu are timp să dezinfecteze multe bilirubine indirecte. Prin urmare, imaginea de diagnosticare este următoarea: