Energia de ionizare - energia unei comunicări, sau cum este numit uneori, primul potențial de ionizare (I1), este cea mai mică energia necesară pentru a elimina un electron dintr-un atom liber în starea sa cea mai mică energie (sol), la infinit.
Energia de ionizare este una din caracteristicile principale ale unui atom. din care depind în mare măsură natura și forța legăturilor chimice formate de atom. Proprietățile de reducere a substanței simple corespunzătoare depind, de asemenea, substanțial de energia de ionizare a atomului.
Există, de asemenea concepte pentru a doua atomi multi-electroni, al treilea și așa mai departe. D. Potențialele de ionizare care reprezintă îndepărtarea de electroni de energie din ei cation neexcitat liber cu sarcini de +1, +2, și așa mai departe. D. Aceste potențiale de ionizare, sunt în general mai puțin importante pentru caracteristicile element chimic.
Energia ionizării are întotdeauna o valoare endoenergetică (acest lucru este de înțeles, deoarece este necesar să se aplice energia pentru a rupe electronul departe de atom, nu se poate întâmpla în mod spontan).
Energia de ionizare a unui atom este afectată cel mai mult de următorii factori:
- încărcarea efectivă a nucleului, care este o funcție a numărului de electroni din atom, nucleul de screening și situat în orbite interioare mai profunde;
- distanța radială de la miez la maximul densității de încărcare a electronului exterior, care este cel mai slab legat de atom și care părăsește electronul în timpul ionizării;
- măsura puterea de penetrare a acestui electron;
- repulsia electron-electron în rândul electronilor externi (valenți).
Energia de ionizare este de asemenea afectată de factori mai puțin semnificativi, cum ar fi interacțiunea schimbului cuantic-mecanic. rotația și corelarea încărcării, etc.
Energia de ionizare a elementelor este măsurată într-un Electronvol cu 1 atom sau în Joule pe mol.
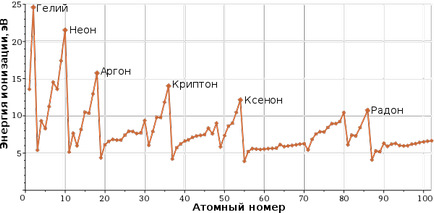
Energia de ionizare a elementelor.