Una dintre cele mai îngrozitoare boli pe care natura "dă naștere" unei persoane este bolile genetice. Puteți lupta cu succes împotriva agenților patogeni de boli - bacterii și viruși, dar dacă problema este în genomul uman de la naștere, este extrem de dificil de a ajuta pacientul. Știința modernă caută persistent posibilitatea de a "repara" genele mutante.

Myodystrofia de la Duchenne este una dintre bolile genetice rare, dar relativ comune. Boala este diagnosticată în vârstă de trei-cinci ani, de obicei, la băieți, apărând la început numai în dificultate în mișcare, la zece ani de care suferă de o distrofie nu poate merge la 20-22 de ani de viata se termina. Este cauzată de o mutație a genei dystrophin, care se află în cromozomul X. Acesta codifică o proteină care leagă membrana celulei musculare cu fibre contractile. Funcțional, acesta este un fel de primăvară, asigurând o contracție și integritate netedă a membranei celulare. Mutațiile din gena duc la distrofia țesutului muscular scheletic, a diafragmei și a inimii. Tratamentul bolii este paliativ și permite doar un pic de atenuare a suferinței. Cu toate acestea, odată cu dezvoltarea ingineriei genetice, lumina a apărut la capătul tunelului.

permit crearea de modele vii ale bolilor genetice grave ale omului. Oamenii ar trebui să fie recunoscători acestor mici creaturi.
Despre război și pace
Terapia genetică este eliberarea în interiorul celulei a unor construcții pe bază de acid nucleic pentru tratamentul bolilor genetice. Cu ajutorul acestei terapii este posibilă corectarea problemei genetice la nivelul ADN și ARN, schimbând procesul de exprimare a proteinei dorite. De exemplu, ADN poate fi transmis celulei cu o secvență corectată, din care se sintetizează o proteină funcțională. Sau, dimpotrivă, este posibil să se elimine anumite secvențe genetice, care vor contribui, de asemenea, la reducerea efectelor dăunătoare ale mutației. În teorie, acest lucru este simplu, dar în practică, terapia genică se bazează pe cele mai complexe tehnologii de lucru cu obiecte din microworld și reprezintă un set de cunoștințe avansate în domeniul biologiei moleculare.
„Dystrophin gena a cărei mutații dau naștere la distrofia musculară Duchenne, o mare - spune directorul de dezvoltare pentru compania de biotehnologie“ Marlin Biotech“, dr, Vadim Zhernovka. - Acesta include 2,5 milioane de perechi de nucleotide, care pot fi comparate cu numărul de scrisori din romanul "Război și pace". Și să ne imaginăm că am scos din epic câteva pagini importante. Dacă aceste pagini descriu evenimente semnificative, atunci înțelegerea cărții ar fi fost dificilă. Dar gena este mai complicată. Găsiți o altă copie a "Războiului și Păcii" este ușor, iar paginile care lipsesc pot fi citite. Dar gena dystrophin este în cromozomul X, iar la bărbați este una. Astfel, în cromozomii de sex, băieții au la naștere doar o copie a genei. Nu este altundeva să-ți iei un prieten.
În cele din urmă, în sinteza proteinelor din ARN, este important să se păstreze cadrul de citire. Cadrul de citire determină ce grup de trei nucleotide este citit ca un codon, care corespunde unui aminoacid din proteină. Dacă există un fragment ADN în gena care nu este un multiplu de trei nucleotide, cadrul de citire se schimbă - modificările de codificare. Acest lucru ar putea fi comparat cu situația în care, după paginile rupte din restul cărții, toate literele se înlocuiesc cu următoarele în ordine alfabetică. Se pare abracadabra. Același lucru se întâmplă și cu o proteină sintetizată incorect. "
Plasterul biomolecular
Una dintre metodele eficiente de terapie genică pentru restabilirea sintezei normale de proteine este sărirea exonilor prin secvențe de nucleotide scurte. În "Marlin Biotech" tehnologia de lucru cu gena dystrophin a fost elaborat cu ajutorul acestei metode. După cum se știe, în timpul transcripției (sinteza ARN) mai întâi a format un ARN așa-numita prematrichnaya cuprinde ambele porțiuni de codificare a proteinei (exoni) și non-codificatoare (intron). Apoi, procesul de îmbinare începe, în timpul căruia intronurile și exonii se separă și formează un ARN "matur" constând doar din exoni. În acest moment, unii exoni pot fi blocați, "înghețați" cu ajutorul unor molecule speciale. Ca rezultat, în ARN matur nu ar regiunile de codificare, din care ar prefera să scape, și, astfel, a restaurat cadrul de citire, proteina este sintetizat.
"Am depistat această tehnologie in vitro", spune Vadim Zhernovkov, adică pe culturi celulare crescute din celulele pacienților cu miodistrofie a lui Duchenne. Dar celulele individuale nu sunt un organism. Invocând procesele din celulă, trebuie să observăm consecințele în direct, dar nu este posibil să implicăm oamenii în încercări din diferite motive, de la etică la cele organizaționale. Prin urmare, a devenit necesar să se obțină un model de miodistrofie a lui Duchenne cu anumite mutații pe baza unui animal de laborator. "
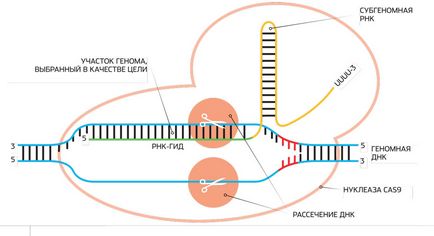
Procesul este prezentat în Schema CRISPR / Cas9, care implica ARNs subgenomice (sgARN), o porțiune a acestuia, funcționează ca un ARN ghid, și proteina nucleazei Cas9, care taie prin ambele catene ale ADN-ului genomic-ARN în poziția de ghidare.
Cum să prind microcosmosul
Animalele transgenice sunt animalele obținute în laborator, în genomul căruia s-au făcut în mod deliberat schimbări intenționate. Încă din anii 1970, a devenit clar că crearea de transgene este cea mai importantă metodă pentru studierea funcțiilor genelor și proteinelor. Una dintre primele metode de obținere a unui organism complet modificat genetic a fost injectarea de ADN în pronucleul ("precursorul nucleului") al zigotului ovulelor fertilizate. Acest lucru este logic, deoarece modificarea genomului animalului este cea mai ușoară la începutul dezvoltării sale.
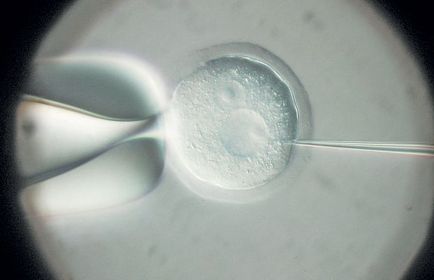
Injecția în nucleul zigotului este o procedură foarte netrivială, deoarece este o microscală. Oul mouse-ului are un diametru de 100 μm, iar pronucleul este de 20 μm. Operația are loc sub microscop, cu o creștere de 400 de ori, dar injecția este cea mai mare care nici nu este manoperă. Desigur, pentru "injectare" se utilizează nu o seringă tradițională, ci un ac special de sticlă cu un canal gol, în interiorul căruia este introdus materialul genetic. Unul din capătul său poate fi ținut în mână, iar celălalt - ultra-subțire și ascuțit - este aproape invizibil cu ochiul liber. Desigur, o astfel de construcție fragilă de sticlă borosilicată nu poate fi stocată mult timp, așa că laboratorul are un set de semifabricate care sunt scoase direct în prealabil pe o mașină specială. Este folosit un sistem special pentru contrastul vizualizării celulelor fără colorare - interferența în pronucleul în sine este traumatizantă și reprezintă un factor de risc pentru supraviețuirea celulelor. Vopseaua ar fi un alt astfel de factor. Din fericire, ouăle sunt destul de tenace, dar numărul de zigoți care dau naștere animalelor transgenice este doar câteva procente din numărul total de ovocite în care a fost injectat ADN.
Următoarea etapă este chirurgicală. Se efectuează o operație de transplantare a zigotului microinjectat în pâlnia oviductului mouse-ului destinatar, care va deveni o mamă surogat pentru transgene viitoare. În plus, animalul de laborator suferă, în mod natural, un ciclu de sarcină și se nasc descendenții. De obicei, aproximativ 20% dintre șoarecii transgenici se găsesc în așternut, ceea ce indică, de asemenea, imperfecțiunea metodei, deoarece conține un element mare de întâmplare. Când este injectat, cercetătorul nu poate controla exact modul în care fragmentele ADN inserate sunt încorporate în genomul viitorului organism. Probabilitatea unor astfel de combinații este ridicată, ceea ce va duce la moartea animalului în stadiul embrionar. Cu toate acestea, metoda funcționează și este destul de potrivită pentru o serie de scopuri științifice.
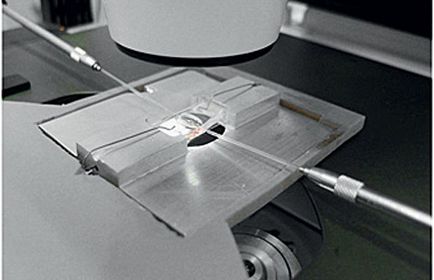
Injectarea ADN în pronucleul zygotic este una dintre cele mai vechi și mai tradiționale tehnologii pentru crearea de transgene. Injectarea se face manual cu ajutorul acelor ultra-subțiri sub microscop cu o creștere de 400 de ori.
Foarfece pentru ADN
Dar există o metodă mai eficientă bazată pe editarea genomului vizat folosind tehnologia CRISPR / Cas9. "Astăzi, biologia moleculară este oarecum asemănătoare cu epoca expedițiilor marine îndepărtate sub pânză", spune Vadim Zhernovkov. - Aproape în fiecare an în această știință există descoperiri semnificative care ne pot schimba viața. De exemplu, acum câțiva ani, microbiologii au descoperit imunitatea la infecțiile virale într-o specie bacteriană aparent studiată. Ca urmare a unor studii suplimentare a relevat faptul că ADN-ul bacterian conține un loci specific (CRISPR), din care fragmentele de ARN sintetizate, capabile sa se leaga cu acizi complementar nucleici ai elementelor străine, cum ar fi virusurile ADN sau ARN. Cu acest ARN, proteina Cas9, care este o enzimă-nuclează, se leagă. ARN servește ca un ghid pentru Cas9 marcând o regiune specifică a ADN-ului în care nucleaza face o tăietură. Aproximativ trei până la cinci ani în urmă, primele documente științifice au apărut, în care tehnologia CRISPR / Cas9 pentru editarea genomului a fost dezvoltată. "
Comparativ cu metoda de introducere a constructelor pentru inserția aleatoare, noua metoda permite de a ridica elemente CRISPR sistem / Cas9 astfel încât să vizeze cu precizie ghidaje ARN pe porțiunile dorite ale genomului și pentru a realiza deleție țintită sau inserția secvenței de ADN dorită. În această metodă, de asemenea, sunt posibile erori (ghid de ARN, uneori, nu au legătură cu porțiunea în care se orientează lui), dar folosind CRISPR eficiența / Cas9 crearea transgenele este deja aproximativ 80%. „Această metodă arată o mare promisiune, nu numai pentru a crea transgenelor, dar și în alte domenii, în special în terapia genică, - spune Vadim Zhernovka. - Cu toate acestea, tehnologia este doar începutul, și să ne imaginăm că corecte oamenii codul genetic va fi folosind CRISPR / Cas9, este destul de dificil, în viitorul apropiat. Deși există o posibilitate de eroare, există și un pericol ca o persoană să piardă o parte importantă de codificare a genomului. "

Dezvoltarea tehnologiilor transgenice face posibilă producerea de proteine animale care sunt solicitate de către industria farmaceutică. Aceste proteine sunt extrase din laptele de caprine și vaci transgenice. De asemenea, există tehnologii pentru obținerea de proteine specifice dintr-un ou de pui.
Medicina de lapte
Compania rusă Marlene Biotech a reușit să creeze un șoarece transgenic, în care mutația care a dus la miodistrofia lui Duchenne a fost complet reprodusă și următoarea etapă va fi testarea tehnologiilor de terapie genică. În același timp, crearea de modele de boli genetice umane bazate pe animale de laborator nu este singura posibilă aplicare a transgenelor. Astfel, în Rusia și laboratoarele occidentale se desfășoară activități în domeniul biotehnologiei, care permite obținerea proteinelor medicinale de origine animală, importante pentru industria farmaceutică. În calitate de producători, vaci sau caprine pot acționa în care aparatul celular de producere a proteinelor conținute în lapte poate fi schimbat. Din lapte, este posibilă extragerea proteinei medicamentoase, care nu se obține chimic, ci cu ajutorul unui mecanism natural, care va crește eficiența medicamentului. În prezent, au fost dezvoltate tehnologii pentru producerea unor astfel de proteine medicinale, cum ar fi lactoferina umană, prourokinaza, lizozima, atrina, antitrombina și altele.
În locul unui tratament atât de complex și încă ineficient, este mai adecvat să nu aibă copii. în avans condamnat la boală. Diagnosticul genetic antenat, cel puțin în cazurile suspectate de a purta o gena defectă. Poate că în viitor va fi posibilă corectarea genei patologice din nou în stadiul prenatal. Sau, ca în cazul de față, să-i desființeze moștenirea. Adică, purtătorul de sex feminin al genei poate da naștere unei fete care va avea un cromozom X matern sănătos, aceasta ar trebui determinată prin diagnostic prenatal. Și nepoții acestei femei vor fi deja asigurate împotriva bolii ducesei
Da, este, dar este necesar să mergem și mai departe - și în detrimentul înțelegerii moderne a UMANITĂȚII de a aboli medicina (din nou în sensul său modern) în general (!) LF lăsă doar, bine, studii preventive ce-fire. Scopul este unul. Salvați genomul pentru care au luptat milioane de ani de SELECTARE NATURALĂ. Altfel, omenirea va degenera foarte repede (câteva mii de ani) din cauza "resturilor genomice". Este obligatoriu să se creeze imense bănci de ADN, care trebuie să treacă fără greș.
Dacă urmați scenariul în cele mai bune tradiții umaniste. apoi statul. nivel pentru a crea programe care interzic nașterea părinților bolnavi, pentru a aplica EVKENIKU peste tot. Dar e mai bine să faci astfel de "experimente pe tine însuți". când mecanismul de selecție naturală va fi pe deplin studiat. Pentru a păstra evoluția prin aplicarea unor probe vechi (deși sănătoase) ale genomului. nu este cea mai bună opțiune ...