Până în prezent, există multe tehnologii diferite pentru obținerea cristalelor de diamante. pentru o mare varietate de aplicații, variind în funcție de dimensiune, culoare și putere.
Diamond nu este nimic mai mult decât carbon pur, cu o latură specială de cristal.
Un alt reprezentant al carbonului pur pe Pământ este cărbunele, grafitul.
Greutatea atomică a carbonului este 12,011;
Numărul de ordine în sistemul periodic al lui Mendeleev 6;
Număr de electroni 6;
valența de bază 4;
La presiunea atmosferică normală, lichidul nu trece;
Când este încălzit la o presiune normală la o temperatură de 3670 ° C, carbon;
trece în gaz, ocolind starea lichidă.
Densitatea este de 3,5 g. cm2;
Refracția luminii 2,42 (sticlă 1, 8);
Duritate de 2 000 000 conv. u (Oțel 30 000, sticlă 40 000 în raport cu pulberea de talc cu duritate = 1);
Temperatura de tranziție în grafit în aer liber este de 1200 0 C;
Temperatura de aprindere într-un mediu cu oxigen pur este de 740 ° C;
Unitățile de diamant sunt carate. Un carat este de 0,2 grame. Diamant, cu dimensiunile de 1 x 1 cm = 17,5 carate;
În diamant, fiecare atom de carbon este conectat la alți 4 atomi de carbon, iar distanța dintre ele este exact aceeași = 1,54 angstromi. Atomii de carbon din diamant sunt situați la colțurile tetraedrului obișnuit al rețelei cristalului atomic.
Amploarea cristalului atomic al unui diamant este un tetraedru
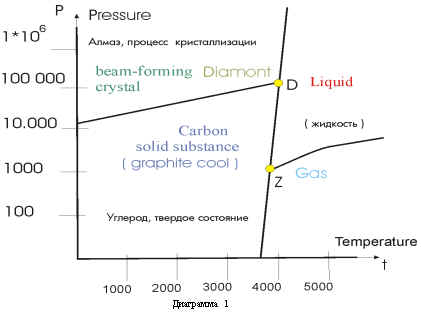
Temperatura de evaporare a cărbunelui este 3670 0 C (diagrama 1), punctul critic (Z) (temperatura 3670 0 С. presiune -120 atm.) Se numește primul punct al stării triple.
În acest moment, este posibilă trecerea carbonului într-o stare solidă, gazoasă sau lichidă.
Odată cu creșterea presiunii și temperaturii, obținem un al doilea punct triplu (D), în care este posibil starea de carbon sub formă de cristale (diamant) în formă lichidă și starea amorfă (grafit).
Cel mai bun rezultat al obținerii de diamante în timpul trecerii de la starea lichidă de carbon la cristalin este scăderea temperaturii, dar, dacă este posibil, lăsând o presiune foarte mare. Caracteristicile de timp ale procesului joacă un rol imens în tehnologia producției de diamante.
După cum sa observat anterior, carbonul nu există în stare lichidă în condiții normale (760 mm Hg și 20 ° C). Carbonul în stare lichidă este posibil și există numai la o presiune de peste 120 atm. și 3740 ° C (diagrama 1).
Dintre proprietățile fizice ale diamantului, trebuie remarcat faptul că temperatura de aprindere în mediul de oxigen este de 670 ° C, în principal diamantul arde fără reziduuri.
Când diamantul este încălzit peste 1200 0 C fără aer, procesul de grafitizare a diamantului începe. acest lucru se întâmplă cu tehnologia greșită a procesului de producție a diamantelor.
Metode de producere a cristalelor de diamante artificiale
Prima metodă de obținere a diamantelor artificiale este o metodă apropiată de apariția naturală a diamantelor naturale. Este o combinație de presiune foarte mare și temperatură ridicată.
Prima metodă este cea mai fiabilă, dar și cea mai sofisticată din punct de vedere tehnologic
Mai jos este una din facilitățile de laborator pentru obținerea cristalelor de diamant cât mai aproape posibil de modelul natural al apariției diamantelor în grosimea pământului - presiune puternică, temperatură înaltă.
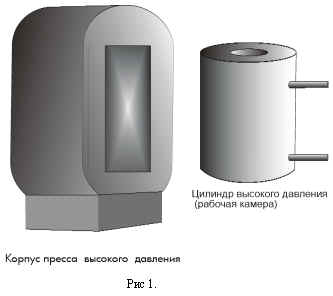
Instalația de laborator pentru producerea de diamante artificiale este o presă de înaltă presiune. Un cilindru de lucru este introdus în carcasa presei.
Acest cilindru asigură forarea circulației agentului frigorific și găuri pentru alimentarea cu apă sub presiune. În acest corp se introduce o cameră din carbură de tantal în care este amplasat un țaglă - grafitul care trebuie transformat într-un diamant.
Se face o prevedere pentru barele de cupru pentru alimentarea curentului electric în camera de lucru.
Tehnologia de obținere a diamantului are loc în mai multe etape.
În primul rând, după instalarea cilindrului într-o presă de înaltă presiune, este furnizată apă și se produce un proces de comprimare preliminară a grafitului prin presiunea apei, până la aproximativ 2-3 mii atmosfere. A doua etapă este agentul frigorific și îngheață apa la minus 12 grade Celsius.
În același timp, o comprimare suplimentară a grafitului are loc până la 20 mii atmosfere datorită extinderii gheții.
În etapa următoare, este alimentat un impuls puternic de un curent electric de 0,3 secunde.
În etapa finală, gheața este dezghețată și diamantele sunt scoase.
Diamantele obținute în acest mod sunt în mare parte de o culoare murdară, au o structură poroasă, forma cristalelor este tetraedrică.
Cele mai multe dintre ele sunt mai puternice decât diamantele naturale și servesc, în principal, în scopuri tehnice.
A doua metodă, posibilă din punct de vedere tehnologic, dar complicată în ceea ce privește echipamentul utilizat, este metoda de creștere a cristalelor de diamant în metan (CH4).
În această metodă, cristalele de diamant sunt încălzite la o temperatură de 1111 ° C și suflate cu metan. Presiunea în camera de lucru poate fi mică, de ordinul a 0,1 atmosfere tehnice. Această presiune este folosită în principal pentru a împiedica intrarea în cameră a oxigenului atmosferic.
Trebuie reținut faptul că pornind de la 1200 ° C, diamantul începe tranziția sa la starea de grafit (fără acces la fracțiunea de oxigen).
Procesul de capacitate cristal de diamant se produce pe suprafața încălzită de diamant prin adăugarea de atomi de carbon în rețeaua cristalină cu cristale de semințe de diamant existente. Cantitatea de carbon (diamant) recuperată este de 0,2% din suprafața cristalului de semințe pe oră.
Forma cristalelor obținute în mod similar este cubică, spre deosebire de tetraedrul natural, culoarea este negru, rezistența este comparabilă cu diamantele naturale. În esența sa, aceasta este carbură pură, dar se numește diamant din cauza durității foarte mari a cristalelor obținute și deoarece diamantele reale sunt folosite ca cristal de sămânță.
A treia metodă de obținere a diamantelor este metoda de explozie
Prin această metodă se produce praf de diamante foarte fin pentru producerea de pietre de șlefuire și abrazivi. Aplicați fie o explozie de exploziv "normal", fie o explozie de sârmă cu un impuls de curent mare.
Pentru a obține o undă densă de detonare, este necesară o membrană care se rupe cu viteza de zgomot în metalul din care este fabricată membrana (pentru fier este 5000 m / sec).
Graful "încălzit", amplasat pe așa-numita "tigaie" în momentul trecerii undei detonante, se transformă într-un cristal de diamant.
Această metodă oferă randamentul produselor mult mai mult în procente din cantitatea de grafit decât metoda de înaltă presiune.
Cristalele se dovedesc a fi apă incoloră, pură, transparentă, dar foarte mică (30-50 microni). Forma cristalelor este o rezistență tetraedală comparabilă cu diamantele naturale.
Esența acestei metode de obținere a diamantelor. Metoda de explozie, este ca sablarea a explozivului în limita val spațiu detonare la impact cu un obstacol în stratul limită, unda de șoc - obstacol, generează atât presiune ridicată și temperatură ridicată. Presiunea poate ajunge la peste 300.000 atm, temperatura fiind zeci de mii de grade. Din păcate (sau din fericire), toate la un moment dat se potrivește în milionimi de secundă, iar dimensiunile (grosime) ale undei de detonare nu depășește 10-30 microni.
În momentul ruperii membranei, undele șocului dobândesc "densitate" și un fel de calitate, cum ar fi - omogenitatea.
Unele cristale de diamant obținute prin această metodă pot avea un diametru de până la 50 microni. O mare importanță în această metodă are o acoperire pe care se află grafitul încălzit și grosimea stratului de lucru.
Experimentele privind presarea "secundară" a diamantelor obținute prin aceeași metodă de explozie sunt interesante, conform principiului metalurgiei pulberilor. În acest caz, în producția de diamante. este posibil să se obțină cristale de diferite dimensiuni și greutăți dintr-o pulbere de diamant. În marea majoritate a cristalelor sunt murdare. Se observă fragilitatea cristalelor diamante secundare rezultate. Puterea este mult mai mică decât puterea naturală, în timp ce prelucrarea este posibilă "surprize". În acest caz, lăcomia poate distruge ideea în sensul cel mai direct al acestei înțelegeri. Grosimea grafitului nu trebuie să depășească 60 de microni.
În a patra metodă de obținere a diamantelor, catalizatorilor
Utilizarea catalizatorilor în producția de diamante contribuie foarte mult la reducerea presiunii și a temperaturii. Cristalele de diamant se formează în stratul de separare dintre grafitul fierbinte și pelicula metalică a catalizatorului. Cu o selecție adecvată de tehnologii, este posibil să se obțină până la 50 de grame de diamante tehnice pe un singur ciclu tehnologic.
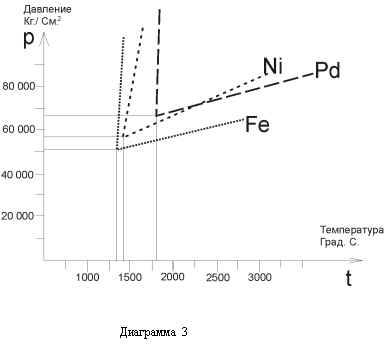
După cum puteți vedea, din diagrama 3. Anexa 3. Cel mai bun catalizator este fier, urmat de nichel, rodiu, paladiu, platină.
Catalizatorul de grafit care apare la limita de tranziție, cristalele de diamant continuă să crească în condiții constante în camera de lucru, atâta timp cât folia de metal catalizator continuă să fie combinată cu grafit.
Anexa 3
Creșterea cristalelor continuă și în cea mai mare parte a dopajului datorită penetrării atomilor de carbon printr-o peliculă subțire de metal.
Diamantele artificiale obținute în acest mod sunt cristale foarte mici (30-200 microni).
Cristalele de diamante obținute la temperaturi scăzute au o formă pătrată de structură de cristale, de culoare neagră, sunt egale în putere sau superioare celor naturale.
Cristalele obținute la temperaturi ridicate și presiuni înalte au o formă octaedrică, culoarea este diferită - cristale galben, albastru, verde, alb, transparent și opac. Ele sunt egale în putere sau superioare diamantelor naturale. Efectul catalizatorilor asupra culorii este evident. Adăugarea de nichel în cristale de diamant dă diamantului un ton verzui, aditivii de beriliu dau diamantelor o nuanță albastră.
Trebuie remarcat că duritatea nu are un diamant mai dur în lume. deși pentru alte proprietăți poate fi inferior anumitor elemente artificiale. Tabelul prezintă elementele care pot oferi o imagine mai completă a unor proprietăți ale diamantului în comparație cu alte elemente terestre.