Celule de combustibil pentru oameni
Bateria Miracle, care lucrează la cel mai comun element chimic din univers - hidrogen, devine o realitate. Un nou tip de catalizator fără platină va reduce în mod semnificativ costul surselor de energie promițătoare ale celulelor de combustie cu hidrogen, cu un domeniu de aplicare de la centralele electrice autonome și vehiculele ecologice la laptopuri și telefoane mobile.
Echipa de cercetare de la Los Alamos National Laboratory (SUA) a spus că ea a reușit să obțină un catalizator ieftin, eficient și durabil fără a utiliza platină scump pentru celule electrochimice de combustibil care rulează pe ciclul de hidrogen-oxigen. Până în prezent, acestea sunt cele mai ecologice dispozitive care asigură o conversie directă a energiei legăturilor chimice de combustibil către cele electrice.
Singurul produs al reacției care apare în elementele de acest tip, pe lângă, desigur, electronii liberi necesari economiei, este apa.
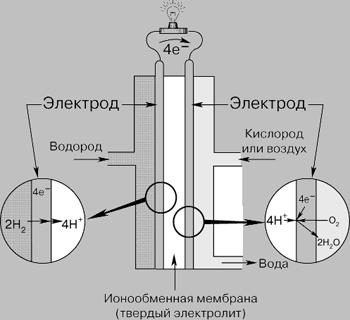
Principiul elementului combustibil electrochimic de tip hidrogen-oxigen // Academic
theregister.co.uk
Nevoia de utilizare a platinei în construcția unei celule de combustibil pe bază de hidrogen este dictată de fizica proceselor care apar în ea. Sarcina principală a unei celule de combustibil electrochimic - să direcționeze electronii liberi care apar în timpul reacției redox, direct comite operație, ocolind etapa de ardere intensă, așa cum apare în generatoarele de energie termică clasice care funcționează pe oxidarea carbonului.
Rezultatul acestei „cutoff termice“ ar trebui sa fie foarte eficient „combustie rece“ (în acest combustie caz hidrogen), la o eficiență mai mare decât randamentul generatoarelor de căldură în cazul în care o mare cantitate de energie este irosit în timpul etapelor intermediare ale încălzirii fluidului de lucru, lucrul mecanic (turbina spinup) sau pur și simplu se disipează în mediul înconjurător.
În celula de combustibil sarcina non-trivială de a realiza "ardere la rece" se realizează în trei etape.
Citește mai mult:
La anodul celulei acoperite cu un strat de catalizator, combustibil (în cazul nostru - hidrogen) disociază rapid, adică dând electronii care intră în circuitul extern pentru a face de lucru, dezintegrează în ioni (protoni). La celălalt capăt al lanțului sunt electroni adecvate la catod, unde, de asemenea, cu ajutorul unui catalizator adaugă comburant - oxigen. După ionul efectuarea stratului electrolitic al ionilor efectiv de la anod la catod unde electronii se recombină cu atomii de hidrogen și - se formează apă.
După cum puteți vedea, eficiența celulei de combustie depinde de două elemente cheie - electrozi cu funcție de catalizatori și electrolit.
Citește mai mult:
Pentru a reduce costurile, pentru a crește eficiența și pentru a extinde fereastra modurilor de lucru sunt acum distribuite de toate forțele principale ale dezvoltatorilor. Astfel, electrolitul lichid a fost deja înlocuit cu membrane speciale de polimer care pot trece numai ioni, permițând astfel elementului să fie redus la valori tranzacționabile atunci când este utilizat în gadgeturi mobile. În mod ideal, o baterie de astfel de elemente trebuie să se potrivească cu mărimea unei cutii de carton cu un cartuș de combustibil înlocuibil sau chiar mai mic.
În ceea ce privește electrozi catalizatori pe care inginerii laboratorului Los Alamos și-au concentrat gândirea inginerie, aici principala piatră de poticnire a rămas platină.
Problema, de fapt, nu a fost metalul care prezintă o stabilitate excelentă și calități catalitice eficiente în condiții de temperatură și umiditate corespunzătoare, iar prețul său, care ajunge până la două mii de dolari o uncie (aproximativ 28 grame), făcând elemente minunate de hidrogen nu este plăcerea populară . În plus, rezervele de platină din lume sunt finite, și că este suficient de utilizarea generală a celulelor de combustibil pentru un maxim de 40-50 de ani.
După ce a trecut prin mai multe exemple de realizare alternative, chimiștii americani gasit inca reteta nonplatinum catalizator - au dovedit a fi o compoziție compozită de cobalt, fier și carbon, obținute prin tehnologii strict specifice care implică polianilina - polimer cu conductivitate electrică datorită legături specifice de azot dintre inele.
Citește mai mult:
catalizator ieftin, democratic, de fapt, sa dovedit a fi un destul de bun ca platina. Mai mult, reacția finală oxidativă pentru a forma apa a fost participarea sa prin mai ciclu complet de oxidare fără ieșire din partea de peroxid de hidrogen pentru membrană polimerică blând este extrem de nedorit. Un alt bonus frumos a fost un comportament stabil de catalizator într-un ciclu de putere al curentului, ceea ce este foarte important, având în vedere modurile în care celulele de combustibil și ar trebui să lucreze, furnizarea de energie toate tipurile de dispozitive mobile.
Rapoartele de succes, cu toate acestea, fapt oarecum innorat că catalizatorul nonplatinum a găsit până în prezent numai unul dintre cei doi electrozi ai celulei de combustibil - ceea ce declanșează reacția finală de oxidare pentru a forma apa. Dar aici nu a fost fără bonus: datorită specificității reacției la acest electrod de platină pentru fabricarea acestuia necesită mult mai mult decât atât pentru descompunerea hidrogenului în protoni care curge mai repede. Prin urmare, economiile rezultate din înlocuirea platină pe componentele ieftine ar fi mai semnificativ.