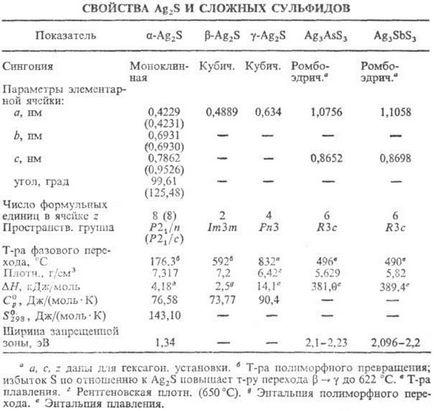
SILVER SULFIDE Ag2 S, cristale gri-negre; există în trei modificări (a se vedea tabelul) - faze cu compoziție variabilă; regiunea de omogenitate pentru b-Ag2S
33,31 - 33,33 la. % S (177 ° C), pentru g-Ag2S, 32,36 - 37,04 la S% (727 ° C). Nici o solubilitate. în apă. org. p-riteley, amoniac de apă. Acesta este descompus de un KCN apoasă sau o vodcă regală. Cu sarcina. În vid, se disociază în perechi de AgB și S, dependența de temperatură a presiunii de vapori S lgp (mm Hg) = - 13082 / T + 9,24. Cu sarcina. în aer se oxidează, a-Ag2 S-semiconductor; fotosensibil; mobilitatea electronului este de 63,5 cm2 / (V · s), găurile fiind de 19,0 cm2 / (V s); r 1000 Ohm · cm; coeficienți. putere termoelectrică -1000 μV / K; conductivitatea termică este de 7,52 W / (cm-K). b-Ag2S are r 10 -3 Ω · cm; coeficienți. puterea termoelectrică este de 60 μV / K
Deoarece sulfura de serebras se găsește în natură sub formă de minerale de acanthită a-Ag2S și argentite b-Ag2S.
Din sorbiul sulfurat sunt reciproc. Ag cu S sau în vid. cutii de cuarț sau topire. sau Ag solid cu perechi S sau cu perechi S în fluxul Ar, N2. precum și precipitarea hidrogenului sulfurat din AgNO3 apoasă.
Sulfurile de argint complex sunt un compus. Ag2S cu sulfuri As, Sb, Bi, Si, Ge, Ga, In și altele. importante sunt Trithioantimonatul Ag3SbS3 (cristale întunecate de culoare închisă) și triatratatul Ag3 AsS3 (cristale roșii); nu solubilitate. în apă și org. p-celeration; sunt obținute prin fuziunea Ag2S cu Sb2S3 (sau As2S3) sau Ag cu S și Sb (As). Acestea se găsesc în mod natural sub formă de minerale de piragit Ag3SbS3 și proliză Ag3 AsS3.
Ag2S este folosit ca o componentă a electroliților solizi. materiale semiconductoare. pentru a precipita Ag + de la șanțul p; Ag3 SbS3 și Ag3 AsS3 - materiale pentru electro-optică. și electro-acustică. dispozitive. Ore. conținând acanthite, argentite, proustite, pirarhirite, -primare pentru producerea Ag.
