Descriere: În scopul de a construi astfel de mașini și a crește CCD, este necesar să se cunoască proprietățile substanței de lucru? abur. Proprietățile de abur sunt utilizate în diferite dispozitive. Studiul proprietăților aburului a condus la posibilitatea de a obține gaze lichefiate și la aplicarea lor largă.
Mărime fișier: 37.75 KB
Lucrarea a fost descărcată: 21 de persoane.
Dacă această lucrare nu vă convine în partea de jos a paginii, există o listă de lucrări similare. De asemenea, puteți utiliza butonul de căutare
TEMA. Formarea aburului și condensarea. Se fierbe. dependență
punctul de fierbere al lichidului din presiune. Punctul de rouă.
1. Formarea aburului și condensarea.
3. Abur saturat și proprietățile sale.
4. În fierbere. Dependența tipului la presiune.
5. Abur supraîncălzit și aplicarea acestuia. Starea critică a materiei.
6. Umiditatea aerului.
1. secolul XIX. numita "vârsta aburului", pentru că la acel moment motoarele termice erau utilizate pe scară largă, substanța de lucru a cărei abur a fost. În prezent, turbinele cu abur sunt utilizate în centrale termice. Pentru a construi astfel de mașini și a crește CCD-ul lor, este necesar să se cunoască proprietățile substanței active # 150; abur.
Proprietățile de abur sunt utilizate în diferite dispozitive. Studiul proprietăților aburului a condus la posibilitatea de a obține gaze lichefiate și la aplicarea lor largă.
Cunoașterea proprietăților vaporilor este necesară și în domeniul meteorologiei.
Astfel, studiul acestui material are o mare importanță practică.
Formarea aburului și condensarea.
Trecerea materiei de la starea lichidă la cea gazoasă se numește vaporizare. și se numește trecerea unei substanțe dintr-o stare gazoasă într-un lichid # 150; condensare.
Formarea aburului este însoțită de U ↑; condensarea este însoțită de U ↓
apare sub formă de fierbere
2. Generarea vaporilor, care apare numai de pe suprafața liberă a unui lichid, care este limita cu un mediu gazos sau cu un vid, se numește evaporare.
Evaporarea are loc la orice temperatură; din suprafața liberă a moleculelor lichide zboară, energia cinetică a căreia este mai mare decât potențiala energie de interacțiune.
E pentru <Е к2> E k1
Pentru a ieși din molecula de lichid trebuie să efectueze lucrările prin reducerea E lor. Lăsați poate doar moleculele de lichid, în care E k> O ieșire (lucru mecanic, care se realizează pentru a depăși forțele de atracție dintre molecule). Deoarece lichidul lasă numai moleculele cu un mare ↑ E k, rămâne cu un mic E la ↓, atunci valoarea medie a energiei E pentru moleculele care rămân în scădere, adică lichidul se răcește. De exemplu. Acest lucru explică frigul atunci când părăsiți apa; dacă sufli în palma mâinii tale.
Împreună cu aceasta, există molecule care se întorc în lichid, transferându-i o parte din energia sa cinetică # 150; E, energia internă a lichidului crește (lichidul se încălzește).
CONDENSAREA EVAPORĂRII SE REALIZEAZĂ DINTRE.
- Dacă predomină evaporarea # 150; lichidul este răcit.
- Dacă condensul predomină # 150; lichidul se încălzește.
Rata de evaporare depinde de:
1. Din tipul de lichid (eter, apă).
2. Din zona suprafeței libere.
3. Cu ↑ T, viteza de evaporare crește.
4. Cu cât este mai scăzută densitatea vaporilor unui lichid deasupra suprafeței sale, cu atât viteza de evaporare este mai mare.
3. Vaporii care saturează și nu saturează spațiul.
a). În vasul deschis procesul de evaporare predomină,
deoarece aburul este o mișcare a aerului.
b). Într-un vas etanșat ermetic, cantitatea
molecule care părăsesc lichidul pe unitate
timpul = numărul de molecule care
reveniți la lichid în același timp
(condensare), adică o dinamică
echilibru. la T = const
Aburul, care se află într-o stare de echilibru dinamic (dinamic) cu lichidul său, se numește abur saturat cu spațiu sau abur saturat.
Această vapori este conținută deasupra suprafeței lichidului într-un vas închis. Presiunea vaporilor saturați depinde numai de temperatură.
Aburul, care este deasupra suprafeței lichidului, atunci când procesul de evaporare predomină asupra procesului de condensare, iar vaporii în absența lichidului se numește vapori nesaturați.
Proprietăți ale vaporilor care saturează spațiul. E PIC. p pereche
1. Presiunea și densitatea vaporilor saturați depind de T.
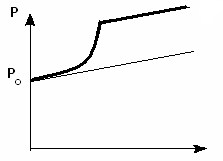
2. Nu respectă legea lui Charles (din moment ce m ≠ const, V = const) și masa vaporilor saturați într-un proces isochoric variază.
3. Nu a fost efectuată Boyle - Mariotte (T = const), la T = cons p ne pereche este independentă de cantitatea de densitate a vaporilor saturați nu este modificată (deoarece schimbarea saturată masei de gaz de vapori).
Proprietăți ale vaporilor, spațiu nesaturat.
Pentru o pereche nesaturată, se pot aplica legile unui gaz ideal numai în cazul în care vaporii sunt departe de saturație.
Aburul saturat poate fi transformat în nesaturat # 150; încălzirea izochorică (expansiune izotermică).
Nesaturate → saturate # 150; prin răcire izochorică (compresie izotermică).
Experimentele arată că, dacă vaporii nu interferează cu lichidul, acesta poate fi răcit sub temperatura la care devine saturată, iar lichidul nu se formează în același timp. O astfel de pereche este numită suprasaturată. Acest lucru se explică prin faptul că pentru formarea de vapori într-un lichid, centrele de condensare sunt necesare. De obicei, particule de praf sau ioni "+", care atrag molecule de abur, ceea ce duce la formarea picaturilor mici.
4. PROCESUL DE CALCARE.
Vaporizarea care are loc în cea mai mare parte a lichidului la o temperatură constantă se numește fierbere.
În timpul fierberii, bulele de vapori cu creștere rapidă se formează în întregul volum al lichidului, care plutește la suprafață. Temperatura rămâne neschimbată (T = const).
Punctul de fierbere # 150; fierberea începe la o temperatură la care presiunea vaporilor saturați din bule este comparată cu presiunea din lichid.
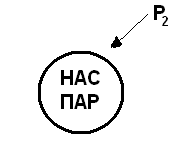
Există întotdeauna un gaz solubil în lichid, care este eliberat în partea de jos și pereții vasului.
Cu creșterea temperaturii, presiunea de vapori crește, bula crește în volum și sub acțiunea F arc apare dacă t a stratului de suprafață a lichidului sub gazul din balon condensează, presiunea scade, bula se prăbușește (explozie micro). Acest lucru explică sunetul apei înainte de a începe să fiarbă.
Când se compară temperatura lichidului, bulele plutesc la suprafață.
DEPENDENȚA T KIP DIN PRESIUNE:
1. Cu cât presiunea externă este mai ridicată, cu atît este mai înaltă temperatura de fierbere.
De exemplu. Cazan de abur: p = 1,6 · 10 6 Pa, iar apa nu se fierbe, chiar la 200 ° C (autoclavă).
2. Reducerea presiunii externe duce la o scădere a T bp.
De exemplu. Munții: h = 7134 m; p = 4,104 Pa; t apă = 70 ° C
3. Fiecare lichid are propriul T. care depinde de presiunea saturată a vaporilor. Cu cât este mai mare presiunea saturată a vaporilor, cu atât mai scăzută este Tg a lichidului corespunzător.
Se numește punctul de fierbere al lichidului la presiune atmosferică normală punctul de fierbere (normele condiției: t = 0 ° C p = 760 mm Hg = 101300 Pa, M aer = 0,029 kg / mol).
Cum se calculează cantitatea de căldură necesară pentru a transforma un lichid în abur.
Q lichid = cm (tib # 150; t 1); Q perechi = m · r; Q = Q lichid + Qn = cm (staniu # 150; t 1) + m-r
r - cantitatea de căldură necesară pentru conversia 1 kg de lichid la vapori (sau vapori de lichid) la o temperatură constantă egală cu temperatura de fierbere numit căldura specifică a vaporizării. (Perechi Q = m · r)
r # 150; Depinde. 1. Din tipul de substanță.
2. Din condițiile externe.
Σ dat = Σ este ecuația de echilibru termic
Abur supraîncălzit și aplicarea acestuia.
Aburul, care este "în cuvă", apoi încălzit la o temperatură ridicată și apoi trimis la o turbină cu aburi, numită uscată sau supraîncălzită. Pe măsură ce presiunea de vapori crește cu temperatura, un abur supraîncălzit se numește un abur de înaltă presiune.
După ce aburul a finalizat lucrările în turbină, acesta are încă o temperatură ridicată și o cantitate mare de energie. Prin urmare, cu (CHP), aburul uzat este transferat întreprinderilor și locuințelor pentru încălzire.
Starea critică a materiei.
Pentru a transforma aburul într-un lichid, este necesar să măriți presiunea și să reduceți temperatura.
Deoarece ρ 1> ρ 2
Pe măsură ce crește temperatura, densitatea scade pentru lichid, iar densitatea vaporilor crește, iar diferența dintre ele devine mai puțin vizibilă. Dacă temperatura este foarte mare, fața va dispărea.
Temperatura critică (t cr) a unei substanțe este temperatura la care densitatea lichidului și densitatea vaporilor saturați devin aceleași.
Este chemată presiunea unei vapori saturate a unei substanțe la t cr presiune critică.
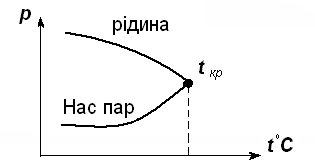
La temperatura critică și proprietățile vaporilor de lichid devin indescifrabile, aceasta înseamnă că, atunci când substanța t kr poate exista numai într-un singur stat, care se numește gaz în acest caz, nici o creștere a presiunii este imposibil să-l transforme în lichid. Dacă substanța este la t cr și p cr. atunci starea sa este numită starea critică.
COMPRESIUNEA GAZELOR ȘI APLICAREA LOR ÎN TEHNICĂ.
Gazul poate fi transformat într-o stare lichidă dacă temperatura sa este sub temperatura critică (Ostan 1908-helium).
În mașinile de comprimare a gazelor, gazele răcite sunt utilizate în timpul extinderii lor adiabatice. În prealabil, gazul este puternic comprimat de compresor, căldura este îndepărtată. În procesul de extindere adiabatică, gazul însuși își desfășoară activitatea și este și mai răcit. Se transformă într-un lichid. Gazele comprimate sunt stocate în vasele Dewar. Este un vas cu pereți dubli între care # 150; vid, pentru a reduce conductivitatea termică a pereților sunt acoperite cu amalgam de mercur. Gazele lichide sunt utilizate pe scară largă în industrie și în experimente științifice.
Proprietățile substanței se schimbă la temperaturi scăzute:
- plumbul devine elastic;
- cauciuc # 150; fragil.
Studiul proprietăților materiei la temperaturi scăzute a dus la descoperirea supraconductivității.
Aerul conține întotdeauna o anumită cantitate de vapori de apă. Dacă există o mulțime de vapori de apă, spunem că aerul este umed, dacă nu este suficient # 150; uscat.
Presiunea, care ar avea vapori de apă, dacă gazele rămase sunt absente, se numește. presiunea parțială a vaporilor de apă.
Umiditatea absolută și relativă a aerului este utilizată pentru cuantificarea umidității aerului.
Umiditatea absolută a aerului este densitatea vaporilor de apă sau presiunea aburului care se află în aer (1 m) la o temperatură dată.
Umiditatea relativă a aerului se referă la raportul dintre presiunea parțială a vaporilor de apă, care este conținută în aer, la presiunea vaporilor saturați de apă la aceeași temperatură.
φ - Umiditatea relativă a aerului arată cât de mult este umiditatea absolută ρ a din densitatea vaporilor de apă ρ n. aer saturat la o anumită temperatură.
ρ a este densitatea vaporilor de apă
ρ n este densitatea saturată a vaporilor
Temperatura la care aerul în timpul răcirii devine saturat cu vapori de apă se numește punctul de rouă.
Aparate pentru determinarea umidității aerului: higrometru și psihometru.
Întrebări pentru auto-control:
1. Oferiți o definiție a proceselor de vaporizare și condensare?
2. Care sunt căile procesului de vaporizare?
3. Explicați principiul răcirii și încălzirii lichidului.
4. Ce depinde de viteza de evaporare a lichidului?
5. Care este echilibrul dinamic?
6. Se fierbe # 150; acest ....
7. În ce condiții începe să fiarbă lichidul?
8. Cum depinde punctul de fierbere al substanței de presiune?
9. Cum pot calcula cantitatea de căldură necesară pentru a transforma un lichid în abur?
10. Umiditatea este ...
11. Cum se calculează umiditatea relativă?
12. Dați definiția punctului de rouă.
2. Vladkova R.A. Dobronravov V.Є. Se citesc cuvintele: Навч. poziția-M. Nauka, 1988.-384 p.
Întrebări pentru rezolvarea subiectului (este inutil să răspundeți)
1. De ce hainele umede, iarba cosita se usuca mai repede in vremea vantului
2. De ce temperatura apei în rezervoarele deschise este întotdeauna mai scăzută în timpul verii
temperatura mediului ambiant?
3. De ce o persoană care a ieșit din apă se simte rece și în vremea vântului
Este acest sentiment mai puternic?
4. Cum să explicați că în haine de cauciuc este greu să îndurați căldura?
Astfel de îmbrăcăminte nu dă umezeala care se formează sub ea, se evaporă
aerul înconjurător, corpul uman se supraîncălzește.
5. Se poate evapora un corp solid?
6. De ce apa stinge incendiul? Care va stinge flacăra mai repede # 150; apă fierbinte sau
7. De ce barometrul "cad" înainte de ploaie
8. Cum se schimbă umiditatea absolută și relativă a aerului la nivelul lui