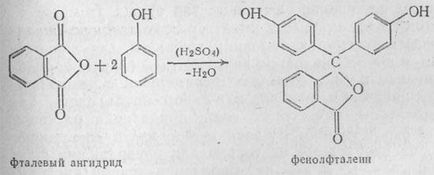
Într-un vas de porțelan amestecat cu atenție și câteva cristale hidroxibenzen (fenol) cu de trei ori cantitatea de anhidridă ftalică. Prin pipetare, adăugăm acid sulfuric prin picurare - până când amestecul este complet impregnat cu lichid. Acum, amestecând continuu cu un subiect baghetă de sticlă conținutul mic flacăra ceașcă arzător, prin încălzire cu ochiuri asbestirovannuyu timp de câteva minute. Când vezi fumul alb, opriți încălzirea pe scurt, altfel vei pierde prea mult de anhidridă ftalică, care fierbe la 131,6 ° C La sfârșitul experimentului, vom vedea că fuziunea dobândește colorarea - de la maro-roșu la portocaliu. Reacția sa încheiat:
Turnăm topitura într-un pahar de apă. Astfel, a precipitat pudră albă, compus în principal din fenolftaleinei, împreună cu unele anhidridă ftalică nereacționat. Am atașat la suspensie restul topiturii din pahar, clătindu-l cu apă. Încă o dată se amestecă energic conținutul paharului cu o baghetă de sticlă, da-l să se stabilească și decantarea (scurgere) separa apa din precipitat.
Se dizolvă colorantul rezultat într-o cantitate mică de alcool. Putem folosi această soluție ca indicator. Dacă adăugarea unei picături de soluție în soluția alcalină provoacă o colorare intensă a zmeurii, care dispare din nou când se adaugă acidul, putem fi siguri că sinteza a avut succes.
Fenolftalina este cel mai simplu colorant ftalic. Sinteza sa, implementată pentru prima dată în 1871 de către chimistul german Bayer, se bazează pe o reacție de condensare în care acidul sulfuric acționează ca agent de îndepărtare a apei.
Fenolftalina nu este adecvată pentru vopsirea fibrelor, deoarece culoarea variază în funcție de aciditatea mediului. Este folosit în principal ca indicator. În plus, fenolftaleina servește ca un laxativ.
Rudele sale apropiate sunt fluoresceine și eozină.
Sursa: E. Grosse, H. Weismannel, "Chimie pentru cei curioși"