Aurul domină mintea omenirii încă de pe vremea Egiptului antic, Mesopotamia, Indochina. De-a lungul timpului, costul este doar în creștere, iar tendința de creștere continuă până în zilele noastre. Acest metal a fost întotdeauna în prețul din cauza rarității sale, frumusețea, și rolul important jucat de proprietățile fizice și chimice ale metalului prețios. De la deschiderea chimiei ca știință, oamenii de știință interesați în formula de aur, ei s-au grăbit să învețe.
Proprietățile chimice și formula
Deci, în tabelul periodic al aurului este de la numărul 79 și se numește Aurum, abrevierea - Au. Elementul este localizat în grupul al unsprezecelea al perioadei a șasea. Numărul grupului indică secvența de încărcare nucleu atomic în creștere cu electroni structură uniformă.
Acest grup este, de asemenea, numit un grup de cupru. Se compune din: cupru, argint, aur și roentgeniu (ununy). Cu cât sunt mai grup de elemente, cu atât mai mult manifestă metalic și proprietăți reducătoare. Aceasta indică perioada de umplere a cochilii exterioare de electroni. Această proprietate este caracterizată prin creșterea proprietăților metalice.
Formula de aur în formă electronică arată astfel: [Xe] 4f14 5d10 6S1. Ca atare, metalul are o formulă chimică, deoarece o compoziție chimică uniformă de aur, adică, de la un tip de atom. Dar de aur a fost dat număr internațional de înregistrare, este scris după cum urmează: CAS: 7440-57-5.
Aurul, ca și alte elemente din tabel, are proprietăți chimice. Metalul este cel mai adesea sub formă de izotop 197 Au. Valența +1 sau +3 metale prețioase. Ca alchimiștii fost întotdeauna interesat în formarea mod artificial de aur. ei au studiat în detaliu toate proprietățile. Și au ajuns la concluzia, așa cum se credea anterior că metalul nu a fost la fel de puternic și inert.
Inainte de aceste experimente, aurul a fost evaluată mai mult, deoarece nu poate fi deteriorat de orice substanță chimică, aceasta nu schimbă aspectul în timp. Material deosebit de puternice, cum ar fi sulf, oxigen nu acționează pe aur, în general. Reacțiile și nu dau următoarele substanțe: hidrogen, azot, fosfor. halogeni Numai formează compuși cu metale prețioase, aur și astfel apare formula chimică AuCl3, AuBr3.
Nu este necesar să contacteze aurul cu soluție de iod-alcool. Aurul este dizolvat în apă regală - un amestec de acid azotic și clorhidric acizi, care sunt utilizate în producția de rafinare, adică, curățarea de aur. Aceasta înseamnă că primul care a ghici alchimistul arab Geber. În timpul acestei operații, se formează cristale de aur, care apoi trebuie încă precipitat, de exemplu, prin utilizarea de sulfat de cupru.
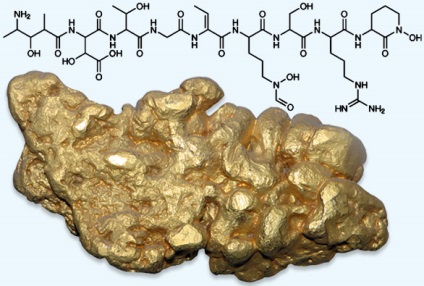
De asemenea, aurul se dizolvă în acid seleniu încălzit. Dar, în procesele de acid sulfuric au loc numai în prezența unor agenți de oxidare cum ar fi dioxid de mangan, acid azotic, sau iod. Rezultat tratat ditsianoauraty da aur pur din minereu.
O autenticitate metalică verificată de acid azotic. Un reactiv se adaugă la cupa, se încălzește pe o plită și apoi se agită, fierbere. În cazul în care se produce nici un răspuns, metalul rămâne în vigoare și nu se dizolvă - atunci este autentic.
Particulele de aur mici nu precipită și forma de materie numite coloizi. Particulele sunt plutesc liber în soluție mai groasă, dându-i o ceață. Coloidul poate fi vopsit. Dacă adăugați soluția de agent reducător de hidrazină capătă o nuanță albastră.
Un amestec coloid, carbonat de potasiu și tanin formează o culoare roșie. Dacă soluția este albastru, se crede că particulele sunt mari și este aspru. O culoare roșie indică faptul că coloidul bine.
Unul dintre principalele avantaje ale aurului în natură, nu într-un laborator, este că, rezistent la coroziune metale prețioase. Produsul este realizat din aur nu schimbă aspectul chiar și după zece ani, aceasta va crește numai în valoare. Această proprietate a făcut posibilă pentru a apela un aur de metal nobil.
Parametrii fizici ai metalului
Din punct de vedere fizica, aurul are mai multe avantaje în comparație cu alte metale. Aurul pur are o saturație luminoase de culoare galbenă. În cazul în care un produs are o culoare, întrebați ce este inclus în ligatură. Adăugarea de cupru dă o nuanță roșiatică, argint sau alt metal alb sub formă de aliaj de aur alb. Natura depozitului de aur, puteți vedea metalul prețios, cu o tentă verde, în funcție de cantitatea de minereu, care este o parte.
Duritatea de aur este considerat un metal moale. Scara criteriilor numit în onoarea Mohs, și cea mai grea substanță de pe pământ este considerat a fi un diamant. El a fost dat numărul 10. Aurul are cifra de 2,5-3,0. Acest lucru se datorează faptului că aurul pur poate fi ușor de tăiat cu un cuțit sau chiar doar o zgârietură. Este din cauza bijutieri nu doresc să facă decorarea 999, deoarece este de scurtă durată, iar produsul va trebui să fie acoperite în continuare cu un strat protector pe partea de sus.
Pentru a determina domeniul de duritate de metal suficient pentru zgâriere cu un obiect ascuțit prin ea. În cazul în care urme rămân, apoi duritatea de mai jos 5. Și în acest fel, în zilele vechi pentru a verifica autenticitatea monedelor. Ei doar musca, iar dacă banii erau urme de pași, aceasta înseamnă că monedele reale.
Aurul este capabil să se disipeze și se dispersează și se estompeze. Prin urmare, moneda de metal pur prețioase rupt repede în jos și a devenit nepotrivit pentru comerț. Poleiala de metal și ușor de utilizat ca un reflector de lumină.
Metalul are o ductilitate ridicată, ductilitate și maleabilitatea. Datorită acestor proprietăți de ornamente de aur și produse realizate din diferite forme. Este posibil chiar și-l rostogolească în foi subțiri din metal. Acest tip de frunze de aur și numit acoperă icoane, produse de interior.
Metal a crea o foarte mică în jetoane chips-uri. Mai mult decât atât, în plus față de ductilitate, aur conduce electricitatea bine, și contactele nu se îndepărtează unul de altul în timp. Aurul poate fi topit la o temperatură de 1063 de grade Celsius, și se fierbe timp - la 2947 grade Celsius. In timpul acestor procese, metalul va pierde culoarea și devin verde pal.
Aceasta ajută căutători o astfel de proprietate de metal, cum ar fi densitatea. E de aur în 19,3 ori mai mare decât cea a apei. De aceea, particulele de aur sunt depuse pe fundul fluxului de apă, deoarece acestea sunt ușor de spălat și curat de impurități.
Utilizarea de aur
Datorită toate proprietățile și caracteristicile metalului utilizate în domenii cum ar fi:
- Electronice (chips-uri, chips-uri);
- medicina (protetica);
- bijuterii de luare (bijuterii);
- producția de piese pentru laborator.
În producția de affinirovaniyu cedat aur, adică purificarea de impurități. Face acest lucru prin metode chimice sau electrochimice folosind galvanizare. Aceste procese pot fi repetate chiar si la domiciliu, în prezența tuturor reactivilor.
Deosebit de interesați în procesul de formare a aurului și alchimiști sale de compoziție. Acești oameni au eclozat ideea de producție de aur de apă și producția sa în laborator. Procesul de formare de aur, înainte de sfârșitul nu este clar, prin urmare, să asigure toate condițiile pentru dezvoltarea de aur este imposibilă.
Cele mai recente rezultate ale biologi de cercetare din Canada au descoperit bacterii care trăiesc și rasa în apele, adică, ionii de aur. Astfel, bacteria produce o substanta numita delfibaktinom. Acest lucru ajută la precipitarea particulelor de aur și formează o pepită.
În ciuda faptului că proprietățile de aur sunt bine stabilite, oamenii de știință încă nu poate rezolva procesul de formare a acestui metal. încă rezultate dovedite. Prin urmare, metalul prețios este încă în creștere în valoare, multi investitori urmați citatul de pe bursă.