Coroziunea aluminiului și a aliajelor sale
Densitatea scăzută și o rezistență mecanică, împreună cu o rezistență satisfăcătoare la coroziune face aluminiu material structural atractiv, care este utilizat pe scară largă în construcții. Cu toate acestea, din punct de vedere chimic din aluminiu - una dintre cele mai reactive metale, care cooperează în mod activ nu numai cu acizi și baze, dar și cu apă! Aparentă contradicție se explică foarte simplu: de oxigen (sau alți oxidanți) suprafață metalică de aluminiu este acoperit cu o peliculă de oxid solid, stabil chimic care protejează metalul de rupere. Acest fenomen se numește pasivare. Metal pasiv, în cazul în care nu se pot schimba, și este activ atunci când agentul agresiv distruge interacțiunea acestuia cu o sursă potențială de coroziune.
Să ne amintim că procesul de distrugere se numește coroziunea metalelor și aliajelor metalice, ca rezultat al acțiunii chimice sau electrochimice a mediului.
rezistent la coroziune, în anumite condiții de metal, se pot descompune în cealaltă. De exemplu, aluminiul este rezistent la coroziunea combustibilului lichid și nu este rezistent la acțiunea de hidroxid de sodiu (așa numitul fenomen de pasiv și activ). oxid de aluminiu creează un strat protector inert chimic, o grosime de 20-100Å. Suprafața de aluminiu este curățat prin folia protectoare poate reacționa cu apa, răspândind hidrogen. Sub influența de oxidare a suprafeței de aluminiu este pasivat, astfel încât oxigenul conținut în aer sau dizolvat în apă, mărește rezistența la coroziune.
Rezistența la coroziune a aluminiului este dependentă în mare măsură de conținutul de impurități ale altor metale. Este cunoscut faptul că la contactul dintre cele două metale sunt imersate într-un mediu electrolit, un cuplu galvanic este format, unde metalul mai activ devine anod, și mai puțin activ - catod. Reacția anod electrochimică este distrusă. Majoritatea impurităților (cu excepția metalelor mai activă decât aluminiul) joacă rolul de catod în raport cu aluminiul, adică, contribuie la distrugerea acestuia. Din acest motiv, de înaltă puritate din aluminiu are o rezistență mai mare la coroziune decât metalul tehnic care, la rândul său, este mai rezistent la coroziune decât aliajele de aluminiu. În plus, rezistența la coroziune a aluminiului este dependentă de caracteristicile mediului și de reacțiile cauzate de mediul din aluminiu.
Mecanismul de coroziune a aluminiului
În prezența de oxidare a suprafeței de aluminiu este acoperit cu un strat protector de oxid de aluminiu. Stratul protector la rândul său, este format din două straturi:
Strat interior 2O 3. care este format prin reacția directă a oxigenului cu metalul. Stratul de oxid interior adiacent metal baze de ferm, iar structura și grosimea acestuia depinde de temperatura de oxidare.
În aer liber format prin reacția stratului interior cu mediul înconjurător, în special apa. Grosimea acestui strat depinde de momentul apariției coroziunii și concentrația substanțelor corozive în mediul înconjurător. Creșterea grosimii stratului exterior datorită oxidării metalului de bază. Stratul exterior este poros, transmite aer și umezeală.
Ca rezultat al proceselor de coroziune pe aluminiu suprafață grosimea totală a stratului de protecție crește, dar grosimea stratului interior, astfel, rămâne constantă.
tipuri de coroziune
coroziunea metalelor pot fi împărțite în chimice și electrochimice.
Coroziunea electrochimică se produce sub acțiunea soluțiilor electrolitice metalic (adică, soluții conținând purtătorii curentului electric - ioni) și însoțite de debutul curentului electric. coroziune chimică are loc atunci când sunt supuse gaze uscate metalice, pulberi și substanțe lichide (fără electrolit) și nu este însoțită de apariția curentului electric. Efectul distructiv al coroziunii începe întotdeauna de la o suprafață metalică. Apoi, coroziunea se extinde în profunzime la o rată în funcție de tipul de metal sau aliaj, compoziția, structura, caracteristicile și compoziția și caracteristicile mediului. Acest proces este adesea însoțită de schimbări în aspectul suprafeței: ea devine plictisitoare, își schimbă culoarea, apar puncte, pete, vezicule etc. Ca rezultat al interacțiunii dintre aluminiu cu materialul de mediu format (produse de coroziune), ale cărei proprietăți influențează foarte mult fluxul .. procesele de coroziune. Luați în considerare posibile variații ale unei astfel de influență:
În procesul de coroziune a produs substanțe volatile sau solubile care sunt îndepărtate ușor și rapid din spațiul de reacție și nu împiedică propagarea coroziunii. Ca rezultat, reacția are loc pe întreaga suprafață metalică disponibilă pentru corodarea și se extinde lin în profunzime.
Pe o suprafață metalică cu un strat subțire, transparent, ferm legat la straturile de metal, care se suprapun accesul reactantul agresiv la substratul metalic. Aceste straturi sunt cauza așa-numita suprafață „pasivare“. O dată cu formarea unui astfel de strat de coroziune este aproape complet oprită, iar procesele reziduale au loc doar pe suprafața exterioară a stratului care se poate dizolva parțial într-un mediu agresiv.
Eterogenitatea rezultatelor stratului de suprafață în manifestarea coroziune neuniformă sau localizate. Un strat de produse de coroziune este distribuit inegal pe suprafața metalului corodare.
În funcție de proprietățile produselor de coroziune pot distinge următoarele tipuri de cele mai recente:
Coroziunea locală sub formă de pete pe suprafața metalică.
coroziune locală sub formă de coroziune care are loc în cazul în care procesul are loc pe suprafața mică suprafață intens și se extinde în metal.
coroziune intergranulară apare atunci când substanța agresivă vine în metal și distruge limita exterioară a cristalelor (granule), care cuprind fuziunea. Produsele de coroziune rămân în interiorul metalului, iar suprafața exterioară nu face nici o schimbare semnificativă. Aceasta este în special forma periculoasa de coroziune în ceea ce privește viteza de proces. În acest caz, materialul generează o limită a granulei, îndeplinește rolul de anod în raport cu granulele, care ocupă o suprafață mare și acționează ca un catod.
Tensiunea la coroziune și o versiune a acestuia - oboseala coroziune apare dacă, în plus față de efectele mediului coroziv al produsului metalic este supus unor sarcini constante sau variabile.
Selectivă (selective) coroziune, în timpul căreia unul sau mai mulți constituenți ai pieselor din aliaj expuse la coroziune, iar aliajul poros de bază păstrează forma originală a produsului.
coroziunii electrochimice
In aluminiu tehnic (sau aliajul acestuia) conține impurități metalice sub formă de incluziuni individuale (magneziu, titan, fier, mangan etc.). Datorită prezenței acestor incluziuni din aliaj, cufundat în electrolit, acesta este un agregat al unui număr mare de electroplacare focare microscopice. Ca urmare a reacției electrochimice care are loc în aceste focare, metal, proeminente în rolul de anod (în acest caz, componentele principale ale aliajului, aluminiu) este dizolvat,, în timp ce hidrogenul este eliberat la microcathodes. Asemenea microsources coroziune sunt celule electrochimice în mod inerent convenționale și caracterizată prin:
1 dimensiune microscopică anod și catod;
2 un aranjament orizontal a electrozilor;
3, conectarea directă a catod și anod.
Procesul coroziunii electrochimice nu este întotdeauna un rezultat al apariției celulelor galvanice microscopice. În unele cazuri, centrele de coroziune sunt „vizibile“ (macroscopic) dimensiune. electromecanic mecanism de distrugere coroziune dimensiuni diferite ale suprafeței catodului (oțel) și anod (aluminiu), prezentat în Fig. 3.
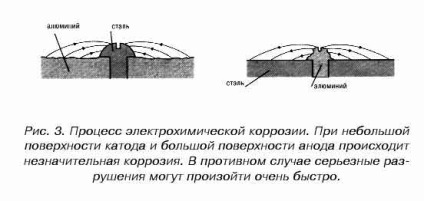
coroziunea atmosferică
coroziunea atmosferică a metalelor este procesul de distrugere a aerului, ca urmare a proprietăților lor chimice care apar de suprafață și a reacțiilor electrochimice. Acesta este cel mai frecvent exemplu de distrugere a metalelor.
Factorii externi includ:
Factorii interni includ:
compoziția chimică a aliajului;
coroziunea atmosferică umedă are loc în stratul electrolitic de grosime mică. Rata de proces depinde de umiditatea aerului, contaminanți atmosferici și produși de coroziune higroscopicitate dacă aceste substanțe reține umezeala de pe suprafața metalică, crește rata de coroziune.
coroziunea atmosferică marină. În regiunile cu climat maritim al atmosferei conține o cantitate mare de săruri pe suprafața picăturilor mici de metal sunt colectate apa de mare, sare și alți contaminanți care accelerează coroziunea.
Reacția aluminiului și a aliajelor sale cu alte metale și aliaje
Mediul electrolit două metale diferite sunt în contact unul cu celălalt sau conectate printr-un conductor pentru a forma celulei electrochimice, în care curentul electric generat. Direcția de mișcare a electronilor în celula determinată de valorile potentialelor de electrod de metale, intensitate coroziune care apar atunci când cele două metale depinde de localizarea lor în seria de tensiune (diferența de potențial), raportul dintre suprafața și nivelul de polarizare a acestora. Cu cât diferența de potențial în celulă, cu atât mai mare tensiune și mai intens anod este distrus. Valorile potențiale indicate în seria de tensiune electrochimică, sunt determinate pentru condiții standard (temperatura de 25 ° C, iar activitatea unitară a ionilor în soluția de electrolit). Rețineți că, în funcție de compoziția electrolitului, aceste valori pot varia. De exemplu, în soluții alcaline aluminiu corodat este mult mai puternic decât acidul. Zinc, care potențial este apropiat de cel al aluminiului pot fi utilizate în contact direct cu aluminiu. Dacă un astfel de contact are loc în mediu neutru și acid, zinc îndeplinește funcția de un anod și un catod, astfel protejează împotriva coroziunii aluminiului. Cu toate acestea, în mediu alcalin, în contrast, activitatea de aluminiu crește, astfel încât zincul accelerează coroziunea aluminiului. La contactul de piese din oțel galvanizat (șuruburi, etc.) și stratul de aluminiu zinc aluminiu oferă protecție inițial, dar după suprafață din oțel zinc ștergere devine deschisă, ceea ce poate duce la coroziunea aluminiului. In contact cu aluminiu se recomandă să se utilizeze metoda de oțel galvanizat, deoarece în acest caz grosimea stratului de acoperire este mai mare decât în galvanizare electrolitică.
În nici un caz nu trebuie să se conecteze din aluminiu cu cupru și aliajele sale, deoarece acest lucru duce la coroziune rapidă a aluminiului (așa-numitele „coroziune catastrofale“). În acest sens, în cadrul structurilor de aluminiu inacceptabile toate tipurile de elemente și cupru suplimentare. Din acest motiv, ar trebui să existe nici un impact asupra apei pluviale din aluminiu, care curge în jos de la acoperișuri și țevi din cupru direct pe structurile de aluminiu, chiar și atunci când conține mici cantități de ioni de cupru.
Acesta ar trebui să evite contactul cu staniu și compușii acestora, în special într-o atmosferă contaminată cu deșeuri industriale. Sărurile de staniu produse în condiții acide, distruge foarte mult suprafețele de aluminiu. oxid roșu de plumb, în prezența umidității cuprinzând acid prezintă un puternic corosive. Prin urmare, atunci când intră în contact cu aluminiu ar trebui să fie evitate elementele din oțel acoperite cu plumb roșu. Mercurul și sărurile sale deja în prezența urmelor de umezeală provoacă coroziune severe de aluminiu. În acest caz, procesul de coroziune este amplificată prin formarea de amalgam: aluminiu amalgamat reacționează rapid cu apa, chiar și în absența acizilor și bazelor! De aceea, în timpul depozitării de profile de aluminiu, chiar cu vapori de mercur (de la becul spart) poate duce la coroziunea instantanee. Compusul din aluminiu sau oțel este acceptabilă în mediul rural, dar în zonele de coastă și oțel industriale accelerează coroziunea aluminiului. Prin urmare, la contactul dintre oțel și aluminiu, pentru a evita contactul direct al acestora, de exemplu, din oțel galvanizat, pictura de aluminiu în timp ce folosind garnituri izolante din materiale sintetice. Când compușii de fier, nichel și crom cu aluminiu se produce diferență de potențial considerabil, astfel încât acestea nu ar trebui să fie conectate direct unul cu altul. Mai mult, aceste săruri metalice (cloruri, sulfați și altele asemenea. D.), care sunt formate ca urmare a coroziunii, contribuie la distrugerea aluminiului.
coroziune chimică.
Procesul are loc coroziunea chimică atunci când este expus la uscat și gaz, electroliti lichizi și alte materiale (inclusiv construcții) din aluminiu.
Ca urmare a atacului chimic pe aluminiu suprafață un strat protector format din produse de coroziune și împiedică interacțiunea agenților agresivi cu metalul. Viteza și tipul procesului de coroziune chimică determină difuzia substanțelor agresive prin stratul protector. Așa cum am menționat mai devreme, un strat de oxid de aluminiu pe suprafața apare ca rezultat al oxidării metalului prin oxigenul din aer. În aer, în absența umidității din grosimea stratului de câteva minute până la 10 Â.